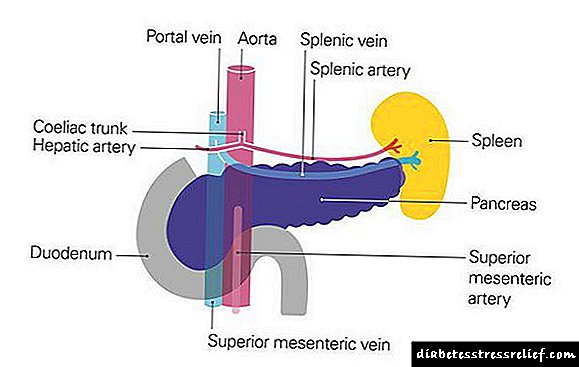
دیابت غیر وابسته به انسولین (NIDDM ، دیابت نوع 2) - بیماری ناهمگن که با اختلال در ترشح انسولین و حساسیت به انسولین در بافتهای محیطی (مقاومت به انسولین) مشخص می شود.
1) وراثت - ژنهای معیوب (در کروموزوم 11 - نقض ترشح انسولین ، بر کروموزوم 12 - اختلال در سنتز گیرنده انسولین ، نقص ژنتیکی در سیستم تشخیص گلوکز توسط سلولهای β یا بافتهای محیطی) که بطور عمده منتقل می شوند ، در هر دو دوقلو یکسان ، NIDDM در 95-100٪ ایجاد می شود. موارد
2) تغذیه و چاقی بیش از حد - غذاهای پر کالری با تعداد زیادی کربوهیدرات ، شیرینی ، الکل و کمبود فیبر گیاهی که به راحتی جذب می شوند ، به همراه سبک زندگی بی تحرک ، به اختلال در ترشح انسولین و ایجاد مقاومت به انسولین کمک می کنند
پاتوژنز NIDDM ناشی از نقض در سه سطح:
1. نقض ترشح انسولین - اولین نقص اصلی NIDDM ، که در اولین و سریع ترین مراحل بیماری تشخیص داده شده است:
الف) تخلفات کیفی- با NIDDM ، سطح انسولین خون ناشتا به میزان قابل توجهی کاهش می یابد ، پروینسولین غالب می شود
ب) اختلالات جنبشی - در افراد سالم ، در پاسخ به تجویز گلوکز ، ترشح انسولین دو فازی مشاهده می شود: اولین قله ترشح بلافاصله پس از تحریک گلوکز شروع می شود ، تا دقیقه 10 به پایان می رسد ، به دلیل آزاد سازی انسولین ذخیره شده از گرانولهای سلولهای β ، و اوج دوم ترشح بعد از 10 دقیقه شروع می شود. با ورودی / در معرفی یا بعد از 30 دقیقه یا بعد از تجویز خوراکی گلوکز ، طولانی مدت ، ترشح انسولین تازه سنتز شده در پاسخ به تحریک سلولهای β با گلوکز را نشان می دهد ، با NIDDM مرحله اول وجود ندارد و مرحله دوم ترشح انسولین صاف می شود
ج) تخلفات کمی - NIDDM با انسولین شدید به دلیل کاهش جرم سلولهای β در جزایر Langvrhans ، رسوب سپرده های آمیلوئید در جزایر مشخص می شود (سنتز شده از آمیلین ، که توسط سلولهای β به همراه انسولین ترشح می شود و در تبدیل پروینسولین به انسولین دخیل است) ، "سمیت گلوکز" اختلالات ساختاری جزایر لانگرهانس و کاهش ترشح انسولین) و غیره
2. مقاومت به انسولین در بافت محیطی:
الف) پیش گیرنده - در ارتباط با محصولات ژنتیکی تعیین شده تغییر یافته ، غیرفعال
مولکولهای انسولین یا تبدیل ناقص پروینسولین به انسولین
ب) گیرنده - همراه با کاهش تعداد گیرنده های انسولین فعال ، سنتز گیرنده های غیر طبیعی غیر فعال ، ظاهر آنتی بادی های ضد گیرنده.
ج) گیرنده - کاهش فعالیت تیروزین کیناز گیرنده انسولین ، کاهش تعداد حمل کننده های گلوکز (پروتئین های موجود در سطح داخلی غشای سلولی که از انتقال گلوکز در داخل سلول اطمینان می کنند) ،
در ایجاد مقاومت به انسولین ، گردش خون آنتاگونیستهای انسولین در خون (آنتی بادی انسولین ، هورمونهای انسولین: هورمون رشد ، کورتیزول ، هورمونهای تیروئید ، تیروتروپین ، پرولاکتین ، گلوکاگون ، CA) نیز حائز اهمیت است.
3. افزایش تولید گلوکز کبد - به دلیل افزایش گلوکونوژنز ، سرکوب تولید گلوکز توسط کبد ، نقض ریتم شبانه روزی تشکیل گلوکز (کاهش در تولید گلوکز در شب) و غیره
تظاهرات بالینی NIDDM:
1. شکایات زیر از نظر ذهنی مشخص است:
- ضعف عمومی و عضلانی (به دلیل کمبود در ایجاد انرژی ، گلیکوژن و پروتئین در ماهیچه ها)
- عطش - در دوره جبران خسارت DM ، بیماران می توانند روزانه 5/5 لیتر یا بیشتر بنوشند ، هیپرگلیسمی بالاتر ، عطش برجسته تر ، خشکی دهان (به دلیل کم آبی و کاهش عملکرد غده بزاقی)
- دفع ادرار مکرر و مفصل چه در شب و چه در شب
- چاقی - اغلب ، اما نه همیشه
- خارش پوست - به ویژه در خانمها در ناحیه تناسلی
2. از نظر عینی وضعیت اندام ها و سیستم ها:
الف) پوست:
- خشکی پوست ، کاهش تراکم و کشش
- ضایعات پوستی پوستی ، فورونکولوزیس مکرر ، هیدروودنیت ، اپیدرموفیتوز پا
- زانتوماس پوستی (پاپول ها و گره های رنگ زرد ، پر از لیپیدها ، واقع در باسن ، پاهای تحتانی ، مفاصل زانو و آرنج ، ساعد) و زانتلاسم (لکه های چربی زرد روی پوست پلک ها)
- روبوز - گسترش مویرگهای پوستی با گرگرفتگی پوست در گونه ها و گونه ها (قرمزی دیابتی)
- نکروبیوز چربی پوست - بیشتر در پاها ، ابتدا گره های متراکم مایل به قرمز یا قهوه ای مایل به زرد یا لکه هایی وجود دارد که توسط یک مرز اریتماتو از مویرگهای گشاد شده احاطه شده است ، پوست بالای آنها بتدریج آتروفی می شود ، صاف ، براق می شود ، با لایزه کردن شدید ("لبه دار") ، گاهی اوقات تحت تأثیر قرار می گیرد. مناطق زخم شده ، خیلی آرام بهبود می یابند و مناطق رنگدانه ای باقی می مانند
ب) دستگاه گوارش:
- بیماری پریودنتال ، شل شدن و ریزش دندان
- پوره آلوئولار ، لثه ، استوماتیت زخم یا آفتی
- گاستریت مزمن ، اثنی عشر با رشد تدریجی آتروفی ، کاهش ترشح آب معده ،
کاهش عملکرد حرکتی معده تا گاستروپارز
- اختلال عملکرد روده: اسهال ، استئاتریا ، سندرم سوء جذب
- هپاتوز کبد چرب ، کوله سیستیت مزمن کلوزه ، دیسکینزی کیسه صفرا و غیره
ج) سیستم قلبی عروقی:
- توسعه زودرس آترواسکلروز و بیماری عروق کرونر قلب با عوارض مختلف (MI با دیابت می تواند بدون درد رخ دهد - سندرم هیستدیس قلبی Parishioner ، اغلب ترنسورال ، دشوار ، همراه با عوارض مختلف)
- فشار خون شریانی (غالباً ثانویه به دلیل نفروژینوپاتی ، آترواسکلروز شریان کلیوی و غیره)
- "قلب دیابتی" - دیستروفی میوکارد دیس متابولیک
گرم) دستگاه تنفسی:
- مستعد ابتلا به سل ریوی با سیر شدید ، تشدید مکرر ، عوارض
- پنومونی مکرر (به دلیل میکروآنژیوپاتی ریه ها)
- برونشیت حاد مکرر و مستعد ابتلا به برونشیت مزمن
ه) دستگاه ادراری: مستعد ابتلا به بیماریهای عفونی و التهابی مجاری ادراری (سیستیتیت ، پیرونفریت) و غیره
تشخیص NIDDM: به سوال 74 مراجعه کنید.
1. رژیم غذایی - باید الزامات زیر را رعایت کند:
- از نظر فیزیولوژیکی در ترکیب و نسبت مواد اصلی (60٪ کربوهیدرات ، 24٪ چربی ، 16٪ پروتئین) ، پوشش کلیه هزینه های انرژی بسته به میزان فعالیت بدنی و اطمینان از حفظ وزن طبیعی "ایده آل" بدن ، با اضافه وزن از وزن بدن یک رژیم غذایی کم فشار خون نشان داده می شود. از محاسبه 20-25 کیلو کالری به ازای هر کیلوگرم وزن بدن در روز
- وعده غذایی 4-5 برابری با توزیع زیر بین کالری روزانه: 30٪ - برای صبحانه ، 40٪ - برای ناهار ، 10٪ - برای میان وعده بعد از ظهر ، 20٪ - برای شام
- از بین بردن کربوهیدرات های قابل هضم ، مصرف الکل ، باعث افزایش محتوای فیبر گیاهی می شود
- چربی های منشأ حیوانی را محدود کنید (40-50٪ چربی ها باید سبزیجات باشند)
رژیم غذایی به شکل تک درمانی انجام می شود تا زمانی که براساس پیش زمینه استفاده از آن ، امکان جبران کامل دیابت وجود داشته باشد.
2. کاهش وزن ، فعالیت بدنی کافی (با وزن بیش از حد بدن ممکن است از بی اشتهایی استفاده شود - یک آماده سازی با فعالیت مرکزی که مانع از جذب مجدد کاتکول آمین ها ، مریدیا (سیبوترامین) 10 میلی گرم 1 بار در روز ، برای 1 ماه کاهش وزن 5/5 کیلوگرم بهینه است
3. دارو درمانی - داروهای هیپوگلیسمی خوراکی (و در بیمارانی که به انسولین نیاز به دیابت نوع 2 دارند + انسولین درمانی با داروهای ترکیبی از عمل ترکیبی: مخلوط -30 ، پروفایل هومولین -3 ، شانه انسولین-25 GT در رژیم تجویز مضاعف قبل از صبحانه و شام)
الف) ترشح - داروهایی که ترشح انسولین تمام شده توسط سلولهای b را تحریک می کنند:
1) مشتقات سولفونیل اوره - کلرپروپامید (نسل اول) 250 میلی گرم در روز در 1 یا 2 دوز ، گلی بن کلامید (مانیل) 1.25-20 میلی گرم در روز ، از جمله اشکال میکرونیدل شده از منیل 1.75 و 3.5 ، گلیپیزید ، گلیکوزلازید (دیابت) 80-320 میلی گرم در روز ، گلیسیدون ، glimepiride (آماریل) 1-8 میلی گرم در روز
2) مشتقات اسیدهای آمینه - بهینه برای تنظیم قند خون پس از مصرف مواد غذایی: نوونورم (رپاگلینید) 0.5-2 میلی گرم قبل از وعده های غذایی تا 6-8 میلی گرم در روز ، استارلیکس (ناتگلینید)
b) biguanides - افزایش حضور انسولین در استفاده محیطی از گلوکز ، کاهش گلوکونوژنز ، افزایش استفاده از گلوکز توسط روده ها با کاهش قند خون از روده ها: N ، N-dimethylbiguanide (سیوفور ، متفورمین ، گلوکوفاژ) 500-850 میلی گرم 2 بار در روز
ج) مهارکننده های گلوکزیداز - کاهش جذب کربوهیدرات ها در دستگاه گوارش: گلوکوبای (آکاربوز) به میزان 150-300 میلی گرم در روز در 3 دوز تقسیم شده با غذا
د) گلیتازون ها (تیوزالدیندینونها ، حساس کننده انسولین) - افزایش حساسیت بافتهای محیطی به انسولین: اکتوس (پیوگلیتازون) 30 میلی گرم 1 بار در روز
4- پیشگیری و درمان عوارض دیررس NIDDM - برای حل موفقیت آمیز مسئله ضروری است:
الف) جبران تخلفات متابولیسم کربوهیدرات به نورموگلیسمی ، آگلیکوزوری با درمان مناسب و مناسب NIDDM
ب) متابولیسم چربی را با درمان مناسب برای کاهش لیپیدها جبران کنید: رژیم غذایی با محدودیت چربی ها ، داروها (استاتین ها ، فیبرات ها ، اسیدهای نیکوتینیک اسید و غیره)
ج) اطمینان از سطح طبیعی فشار خون (داروهای ضد فشار خون ، به ویژه مهار کننده های ACE ، که علاوه بر اینها دارای اثر محافظت کننده هستند)
g) برای اطمینان از تعادل سیستم انعقادی و ضد انعقادی خون
پیشگیری از عوارض دیررس شامل موارد زیر است حفظ جبران مداوم متابولیسم کربوهیدرات برای مدت طولانی و تشخیص زودهنگام مراحل اولیه عوارض دیررس دیابت:
1) رتینوپاتی دیابتی - لازم است به طور مرتب 5 سال اول یک بار در سال معاینه فوندوس انجام شود و سپس هر 6 ماه یک بار با نئوپلاسم رگهای شبکیه ، انعقاد لیزر مشخص شود
2) نفروپاتی دیابتی - لازم است که میکروآلبومینوری را هر 6 ماه یک بار مشخص کنید ، هنگامی که علائم نارسایی مزمن کلیوی ظاهر می شود - رژیم غذایی با محدودیت پروتئین حیوانی (حداکثر 40 گرم در روز) و کلرید سدیم (حداکثر 5 گرم در روز) ، استفاده از مهار کننده های ACE ، سم زدایی و همراه با بدتر شدن عملکرد کلیه ها - همودیالیز و سایر عوارض.
پیشگیری از NIDDM: یک شیوه زندگی سالم (جلوگیری از هیپودینامیا و چاقی ، سوء استفاده از الکل ، سیگار کشیدن و غیره ، تغذیه منطقی ، از بین بردن استرس) + اصلاح کافی و مداوم با رژیم یا قسمت اول ابتلا به چربی خون ، و به دنبال آن نظارت بر دوره ای سطح قند خون.
عوارض دیررس (مزمن) دیابت: میکروآنژیوپاتی (رتینوپاتی دیابتی ، نفروپاتی دیابتی) ، ماکروآنژیوپاتی (سندرم پای دیابتی) ، پلی نوروپاتی.
آنژیوپاتی دیابتی - ضایعه عروقی عمومی در دیابت ، گسترش در عروق کوچک (میکروآنژیوپاتی) و شریان های کالیبر بزرگ و متوسط (ماکروآنژیوپاتی).
میکروآنژیوپاتی دیابتی - ضایعه خاص دیابت قارچی عروق کوچک (شریانی ، مویرگ ، ونول ها) ، که با تغییر در ساختار آنها (ضخیم شدن غشای زیرزمین ، تکثیر اندوتلیال ، رسوب گلیکوزآمینوگلیکان ها در دیواره رگ ، عروق دیواره شریانی ، میکروترومبوزها ، توسعه میکروآنوریسم ها) با افزایش شدید در نفوذپذیری مشخص می شود :
1. رتینوپاتی دیابتی - علت اصلی نابینایی در بیماران مبتلا به دیابت ، عدم تکثیر (وجود میکروآنوریسم ها ، خونریزی ، ورم ، اگزودات های جامد در شبکیه) ، پیش آگهی (+ تغییر در رگ های شبکیه: وضوح ، تورم ، حلقه ها ، برداشتن ، نوسان عروق خونی) و پرولیفراتیو (+ ظاهر عروق جدید) ، خونریزی های مکرر در شبکیه با جدا شدن آن و تشکیل فشرده بافت همبند) اشکال ، شکایات بالینی از مگس های سوسو زدن ، لکه ها ، احساس مه ، اشیاء تار که پیشرفت کمتری دارند ها حدت بینایی.
غربالگری برای رتینوپاتی دیابتی.
"استاندارد طلایی" عکاسی رنگ آمیزی استریوسکوپی از فوندوس ، آنژیوگرافی فلورسانس شبکیه و افتالموسکوپی مستقیم در دسترس در حال حاضر برای غربالگری است.
معاینه اول بعد از 1.5-2 سال از تاریخ تشخیص دیابت ، در صورت عدم وجود رتینوپاتی دیابتی ، معاینه حداقل 1 بار در 1-2 سال ، در صورت وجود - حداقل 1 بار در سال یا بیشتر اوقات ، با ترکیبی از رتینوپاتی دیابتی با بارداری ، AH ، CRF - یک برنامه معاینه فردی ، با کاهش ناگهانی در بینایی - معاینه فوری توسط چشم پزشک.
اصول درمان رتینوپاتی دیابتی:
1. داروهای درمانی: حداکثر جبران سوخت و ساز بدن کربوهیدرات (داروهای کاهش دهنده قند خوراکی ، انسولین درمانی) ، درمان عوارض همزمان ، آنتی اکسیدان ها (نیکوتین آمید) برای رتینوپاتی دیابتی غیر تکثیر کننده با لیپیدهای خون بالا ، هپارین های با وزن کم مولکولی در مراحل اولیه فرآیند
2- فتوكولاژي عروق شبكيه در مراحل اوليه رتينوپاتي ديابتي (محلي - کانون هاي انعقاد ليزر در ناحيه فرآيند پاتولوژيك يا خونريزي پره اترنتال اعمال مي شود ، منعكس هاي كانوني در چند رديف در نواحي paramacular و parapapillary ، panretinal - مورد استفاده براي رتينوپاتي پروليفراتيك ، از 1200 تا 1200 استفاده مي شود) کانونها در یک الگوی checkerboard روی شبکیه استفاده می شوند ، همه راه ها از مناطق paramacular و parapapillary تا منطقه استوایی شبکیه).
3. Cryocoagulation - برای بیماران مبتلا به رتینوپاتی دیابتی پرولیفراتیو ، پیچیده شده توسط خونریزی مکرر در بدن زجاجیه ، افزایش خشن در نواحی عروقی و بافت پرولیفراتیو ، مشخص می شود که ابتدا در نیمه تحتانی چشم چشم انجام می شود ، و پس از یک هفته در نیمه فوقانی ، امکان بهبود یا تثبیت بینایی باقی مانده ، برای جلوگیری از دید کامل را فراهم می آورد. نابینایی
4- ویتراکتومی - برای خونریزی مکرر زجاجیه با توسعه بعدی تغییرات فیبروتیک در زجاجیه و شبکیه بیان شده است
2. نفروپاتی دیابتی - به دلیل نفروژانسواسکلروز گره ای یا پراکنده گلومرول کلیوی.
تظاهرات بالینی و آزمایشگاهی نفروپاتی دیابتی.
1. در مراحل اولیه ، تظاهرات ذهنی وجود ندارد ، در یک مرحله از نظر بالینی ، افزایش پروتئینوری ، فشار خون بالا شریانی ، سندرم نفروتیک ، کلینیک پیشرونده نارسایی مزمن کلیه مشخصه است.
2. میکروآلبومینوری (دفع آلبومین ادرار ، بیش از مقادیر طبیعی ، اما نرسیده به درجه پروتئینوری: 30-300 میلی گرم در روز) - اولین علامت نفروپاتی دیابتی ، با ظهور میکروآلبومینوریای مداوم ، مرحله بالینی بیان شده بیماری در 5-7 سال بروز خواهد کرد.
۳- چربی خون (GFR> ۱۴۰ میلی لیتر در دقیقه) - نتیجه اولیه تأثیر قند خون بر عملکرد کلیه در دیابت ، به آسیب کلیوی کمک می کند ، با افزایش مدت زمان دیابت ، GFR به تدریج به نسبت افزایش پروتئینوری و شدت درجه فشار خون بالا کاهش می یابد.
در اواخر نفروپاتی دیابتی پروتئینوری مداوم ، کاهش در GFR ، افزایش آزوتمی (کراتینین و اوره خون) ، تشدید و تثبیت فشار خون بالا و ایجاد سندرم نفروتیک مشخصه است.
مرحله توسعه نفروپاتی دیابتی:
1) عملکرد بیش از حد کلیه ها - افزایش GFR> 140 میلی لیتر در دقیقه ، افزایش جریان خون کلیوی ، هیپرتروفی کلیوی ، آلبومینوری طبیعی
آنچه را که می خواستید پیدا نکردید؟ استفاده از جستجو:
بهترین گفته ها:دانش آموز شخصی است که دائماً اجتناب ناپذیری را کنار می گذارد. 10160 - | 7206 - یا همه چیز را بخوانید.
اتیوپاتوژنز و تشخیص دیابت
به گفته کارشناسان WHO (1999) ، دیابت به عنوان یک اختلال متابولیکی از دلایل مختلف توصیف می شود ، که با افزایش قند خون مزمن همراه با اختلال کربوهیدرات ، چربی و متابولیسم پروتئین همراه با نقص در ترشح انسولین ، اثرات انسولین یا هر دو مشخص می شود.
نقص اصلی متابولیک در دیابت ، اختلال در انتقال گلوکز و اسیدهای آمینه از طریق غشای سیتوپلاسمی به بافتهای وابسته به انسولین است. مهار حمل و نقل متابbrane از این مواد باعث تغییر سایر متابولیک ها می شود.
در سال های اخیر ، این ایده بالاخره شکل گرفته است که دیابت از نظر ژنتیکی و پاتوفیزیولوژیکی یک سندرم ناهمگن قند خون مزمن است که اشکال اصلی آن دیابت نوع I و II است. غالباً عوامل بیماری شناختی و عوامل مؤثر در ایجاد بیماری قابل تشخیص نیستند.
از آنجا که با تظاهرات بالینی آشکار دیابت با پارامترهای بیوشیمیایی تأیید شده در بخش بالغ جمعیت ، فرکانس بالایی از عوارض عروقی دیررس (توسعه آن با مدت زمان اختلالات متابولیکی بیش از 5-7 سال رخ می دهد) آشکار می شود ، بنابراین در سال 1999 متخصصان WHO طبقه بندی جدیدی از این بیماری و جدید را پیشنهاد کردند. معیارهای تشخیصی آزمایشگاهی دیابت (جدول 33.1).
غلظت گلوکز ، میلی مول در لیتر (mg / dl) | خون کامل | پلاسما |
| وریدی | مویرگی | وریدی | مویرگی |
| دیابت قندی: |
| روی شکم خالی | > 6,1(> 110) | > 6,1(> 110) | > 7,0 (> 126) | > 7,0 (> 126) |
| یا 2 ساعت بعد از بارگیری گلوکز یا هر دو | > 10,0 (> 180) | > 11,1 (> 200) | > 11,1 (> 200) | > 12,2 (> 220) |
| تحمل گلوکز مختل شده |
| روی شکم خالی | 6.7 (> 120) و 7.8 (> 140) و 7.8 (> 140) و 8.9 (> 160) و 5.6 (> 100) و 5.6 (> 100) و 6 ، 1 (> 110) و 6.1 (> 110) و 6.1 (> 110) تا 7.0 میلی مول در لیتر (> 126 میلی گرم در دسی لیتر) باید با تعیین مجدد میزان گلوکز در روزهای دیگر تأیید شوند. بنابراین ، معیارهای بیوشیمیایی دقیق تری برای اختلال در متابولیسم کربوهیدرات معرفی شده است. در صورت وجود علائم بالینی خفیف ، تشخیص دیابت همیشه باید با آزمایشات مکرر در روز دیگر تأیید شود ، در صورت عدم وجود قند خون آشکار با جبران فشار حاد متابولیک یا علائم بارز دیابت. افرادی که سطح قند خون / پلاسمای ناشتا را بالاتر از حد طبیعی دارند اما پایین تر از سطح تشخیصی هستند ، برای تشخیص نهایی دیابت ، اندازه گیری های کنترل را انجام می دهند یا تست تحمل گلوکز (PTH). PTH براساس زمینه رژیم غذایی طبیعی و فعالیت بدنی در صبح انجام می شود ، نه زودتر از 10 ساعت و نه بعد از 16 ساعت بعد از آخرین وعده غذایی. 3 روز قبل از آزمایش ، بیمار باید حداقل 250 گرم کربوهیدرات در روز دریافت کند و در این مدت نباید داروهای مؤثر بر گلوکز پلاسما (گلوکوکورتیکواستروئیدها ، ضد بارداری های هورمونی ، داروهای ضد التهابی و کاهش دهنده قند ، غیر استروئیدی ، داروهای ضددردنده ، برخی از آنتی بیوتیک ها ، دیورتیک های تیازید) مصرف کند. . در مورد PTH ، شاخص های زیر شاخص های شروع هستند: 1) تحمل گلوکز نرمال با سطح گلیسمی 2 ساعت پس از بارگیری گلوکز از 7.8 میلی مول در لیتر (> 140 میلی گرم در لیتر) مشخص می شود ، اما زیر 11.1 میلی مول در لیتر (> 200 میلی گرم در دسی لیتر) به شما امکان تشخیص دیابت را می دهد ، که باید با مطالعات بعدی تأیید شود. بنابراین ، دیابت را می توان با افزایش قند خون ناشتا> 7.0 میلی مول در لیتر (> 126 میلی گرم در لیتر) و در کل خون> 6.1 میلی مول در لیتر (> 110 میلی گرم در دسی لیتر) تشخیص داد. طبقه بندی دیابتبه همراه معیارهای جدید تشخیصی دیابت ، کارشناسان WHO طبقه بندی جدیدی از دیابت را پیشنهاد کردند (جدول 33.2). جدول 33.2. طبقه بندی اتیولوژیکی اختلالات گلیسمی (WHO ، 1999) 2. دیابت نوع 2 (از نوعی مقاومت به انسولین غالب با کمبود انسولین نسبی به نوع با کمبود ترشحی غالب با یا بدون مقاومت به انسولین) 3. سایر مشخصات دیابت
- نقص ژنتیکی در عملکرد سلولهای b
- نقص ژنتیکی در فعالیت انسولین
- بیماری های لوزالمعده اگزوکرین
- غدد درون ریز
- دیابت ناشی از داروها یا مواد شیمیایی
- عفونت
- اشکال غیرمعمول دیابت با واسطه ایمنی
- سایر سندرمهای ژنتیکی که گاهی با دیابت همراه هستند 4- دیابت حاملگی
|
توجه: اشکال از نقص حاملگی تحمل گلوکز و دیابت حاملگی گنجانده شده است.پیشنهاد می شود از اصطلاحات "دیابت وابسته به انسولین" و "غیر وابسته به انسولین" استفاده نکنید و فقط اسامی "دیابت نوع I و II" باقی نماند. این به دلیل پاتوژنز این اشکال است و عدم توجه به درمان مداوم. علاوه بر این ، امکان انتقال یک فرم مستقل از انسولین به وابستگی کامل به آن می تواند در مراحل مختلف زندگی بیمار رخ دهد (جدول 33.3).
جدول 33.3. اختلالات گلیسمی: انواع اتیولوژیک و مراحل بالینی (WHO ، 1999)
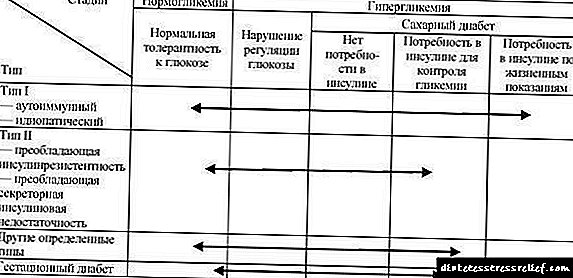
شایع ترین انواع دیابت I و II ، که بیش از 90٪ کل موارد دیابت را تشکیل می دهد.
دیابت نوع 1 شامل اختلالات متابولیسم کربوهیدرات مرتبط با تخریب سلولهای β سلولهای جزایر لوزالمعده در افراد مستعد ژنتیکی و در پس زمینه اختلالات ایمونولوژیکی است.
بیماران با سن تا 30 سال ، کمبود انسولین مطلق ، تمایل به ketoacidosis و نیاز به تجویز انسولین اگزوژن مشخص می شوند.
در مواردی که تخریب و کاهش تعداد سلول های b در اثر یک فرآیند ایمنی یا خود ایمنی ایجاد می شود ، دیابت خود ایمنی در نظر گرفته می شود. دیابت نوع اول با وجود انواع مختلفی از آنتی بادی ها مشخص می شود.
مستعد ابتلا به آن با ژنهای HLA پیچیده DR3 ، DR4 یا DR3 / DR4 و آللهای خاصی از محل HLA DQ ترکیب شده است. تأکید می شود که دیابت نوع یک (خود ایمنی) می تواند بدون نیاز به تجویز انسولین برای نابودی کامل سلول های ب ، مراحل رشدی را از طریق هنجارگلیسمی طی کند. کاهش یا از بین رفتن کامل سلولهای b منجر به وابستگی کامل به انسولین می شود ، بدون آن بیمار تمایل به کتواسیدوز ، کما ایجاد می کند. اگر علت و پاتوژنز ناشناخته باشد ، در چنین مواردی از دیابت نوع I به دیابت "ایدیوپاتیک" گفته می شود.
دیابت نوع II شامل اختلالات متابولیسم کربوهیدرات است که با درجات مختلفی از ارتباط بین شدت مقاومت به انسولین و نقص در ترشح انسولین همراه است. به عنوان یک قاعده ، در دیابت نوع II ، این دو عامل در پاتوژنز بیماری دخیل هستند ، در هر بیمار با نسبت متفاوت مشخص می شوند.
دیابت نوع II معمولاً بعد از 40 سال تشخیص داده می شود. بیشتر اوقات ، این بیماری به آرامی ، به تدریج و بدون کتواسیدوز دیابتی خود به خود بروز می کند. به طور معمول ، درمان برای نجات جان نیاز به تجویز سریع انسولین ندارد. در ایجاد دیابت نوع II (تقریباً 85٪ از کل موارد دیابت) ، فاکتور ژنتیکی (خانوادگی) از اهمیت بالایی برخوردار است.
بیشتر اوقات ، وراثت چندوجهی در نظر گرفته می شود. شیوع دیابت در بیماران دارای وزن ارثی با افزایش سن افزایش می یابد ، و در افراد بالاتر از 50 سال به 100٪ نزدیک می شود.
بیماران مبتلا به دیابت نوع II غالباً با انسولین به دلیل قند خون بالا درمان می شوند ، اما با برداشت انسداد انسداد کتواسیدوز خود به خود عملا رخ نمی دهد.
سندرم متابولیک
در پیدایش دیابت نوع II ، نقش تحریک آمیز مهمی توسط چاقی خصوصاً از نوع شکمی ایفا می شود.
این نوع دیابت با هیپرینسولینمی ، افزایش مقاومت به انسولین در بافت ، افزایش تولید گلوکز کبد و نارسایی پیشرونده سلولهای سلول همراه است.
مقاومت به انسولین در بافتهای حساس به انسولین ایجاد می شود ، که شامل عضله اسکلتی ، بافت چربی و کبد می شود. رابطه بین انسولین و چاقی کاملاً مشخص است.
در شرایط پرفشاری خون در چاقی ، افزایش سطح خون سوماتوستاتین ، کورتیکوتروپین ، اسیدهای چرب آزاد ، اسید اوریک و سایر عوامل ضد بارداری مشاهده شد که از یک سو روی سطح گلوکز و انسولین در پلاسمای خون تأثیر می گذارد و از طرف دیگر شکل گیری یک احساس "فیزیولوژیکی" گرسنگی این منجر به تسلط لیپوژنز بر لیپولیز می شود. مقاومت انسولین در بافت چاقی با افزایش سطح انسولین پلاسما غلبه می کند.
هیچ ماده غذایی خاص دیابوژنیک وجود ندارد ، اما افزایش مصرف چربی های اشباع و مصرف کافی فیبر در رژیم غذایی به کاهش حساسیت به انسولین کمک می کند.
کاهش وزن بدن 5-10٪ ، حتی اگر چاقی هنوز ادامه یابد ، منجر به اصلاح نقایص گیرنده ، کاهش غلظت انسولین در پلاسما ، کاهش سطح گلیسمی ، لیپوپروتئینهای آتروژنیک و بهبود وضعیت عمومی بیماران می شود.
پیشرفت دیابت در برخی از بیماران چاق با افزایش کمبود انسولین از نسبت به مطلق پیش می رود. بنابراین ، چاقی از یک طرف یک عامل خطر برای ابتلا به دیابت و از طرف دیگر تظاهرات اولیه آن است. دیابت نوع II از نظر بیماری زا ناهمگن است.
گزارش WHO در سال 1999 مفهوم سندرم متابولیک را به عنوان یک عامل مهم در عوارض عروقی معرفی کرد.
با وجود عدم تعریف توافق شده در مورد سندرم متابولیک ، مفهوم آن شامل دو یا چند مؤلفه زیر است:
- اختلال در متابولیسم گلوکز یا وجود دیابت ،
- مقاومت به انسولین ،
- افزایش فشار خون بیش از 140/90 میلی متر RT. هنر
- افزایش تری گلیسیرید و یا کلسترول پایین لیپوپروتئین با چگالی کم(LDL),
- چاقی ،
- میکروآلبومینوری بیش از 20 میکروگرم در دقیقه.
استفاده از اقدامات دقیق رژیم غذایی با هدف کاهش وزن بدن در بیماران چاق ، قرار گرفتن در معرض عوامل خطر سندرم متابولیک اغلب منجر به عادی یا کاهش قند خون و کاهش دفعات عوارض می شود.
عوارض دیابت
تعدادی از بیماران (تقریباً 5٪) مستقل از عوارض ، بدون توجه به میزان جبران سوخت و ساز کربوهیدرات ، مستعد ابتلا به این عوارض هستند ؛ در بخش دیگری از بیماران (20-25٪) عوارض به ندرت به دلیل مستعد ژنتیکی پایین مشاهده می شود.
در بیشتر بیماران (70-75)) ، درجه تمایل ژنتیکی می تواند متفاوت باشد ، و در این بیماران است که حفظ جبران خوب متابولیسم کربوهیدرات تأثیر مهاری در روند آنژیوپاتی و نوروپاتی دارد.
آنژیوپاتی دیابتی (کلان و میکروآنژیوپاتی) و نوروپاتی فارغ از نوع آن ، شدیدترین تظاهرات دیابت هستند. در ایجاد این اختلالات ، آنها به گلیکولاسیون پروتئین ها (اتصال آنها به یک مولکول گلوکز در نتیجه یک واکنش غیر آنزیمی و در مرحله آخر ، واکنش شیمیایی غیرقابل برگشت پذیر از تغییر عملکرد سلول در بافتهای وابسته به انسولین) و تغییر در خصوصیات رئولوژیکی خون اهمیت زیادی می دهند.
گلیکوزی شدن پروتئین های هموگلوبین منجر به اختلال در حمل و نقل گاز می شود. علاوه بر این ، ضخیم شدن غشاهای زیرزمین به دلیل نقض ساختار پروتئین های غشایی وجود دارد. در بیماران مبتلا به دیابت ، یک فرایند افزایش اختلاط گلوکز در پروتئین های سرم خون ، لیپوپروتئین ها ، اعصاب محیطی و ساختار بافت پیوندی تشخیص داده شد.
درجه گلیکاسیون مستقیم با غلظت گلوکز متناسب است. تعیین هموگلوبین گلیکوزیله شده (HbA1b ، HbA1c) به عنوان درصد کل محتوای هموگلوبین به یک روش استاندارد برای ارزیابی وضعیت جبران سوخت و ساز بدن از متابولیسم کربوهیدرات در بیماران مبتلا به دیابت تبدیل شده است. با وجود قند خون ثابت و بسیار زیاد ، حداکثر 15-20٪ از کل هموگلوبین می تواند تحت عمل گلیکاسیون قرار گیرد. اگر محتوای HbA1 از 10 درصد تجاوز کند ، توسعه رتینوپاتی دیابتی نتیجه نهایی است.
همچنین مسئول رشد آنژیو و نوروپاتی نیز جذب بیش از حد گلوکز در سلولهای بافتی مستقل از انسولین محسوب می شود. این منجر به تجمع در آنها الکلی حلقوی سوربیتول می شود ، که فشار اسمزی در سلول ها را تغییر می دهد و از این طریق به پیشرفت ورم و عملکرد اختلال کمک می کند. تجمع داخل سلولی سوربیتول در بافت های سیستم عصبی ، شبکیه ، لنز و دیواره عروق بزرگ اتفاق می افتد.
مکانیسم های بیماری زای تشکیل میکروتروبی در دیابت اختلالات هموستاز ، ویسکوزیته خون ، میکروسیرکولاسیون است: افزایش تجمع پلاکت ها ، ترومبوکسان A2 ، سنتز پروستاسیکلین ضعیف و فعالیت فیبرینولیتیک خون.
بیشتر بیماران مبتلا به دیابت دچار نفروپاتی می شوند. این بیماری شامل گلومرولوسکلروز دیابتی ، نفروژینوسکلروز ، پیرونفریت و غیره است. در سالهای اخیر رابطه روشن بین وجود پروتئین در ادرار و سرنوشت نهایی کلیه ها در بیماران مبتلا به دیابت مشاهده شده است.
مهم است که میکروآلبومینوری تشخیص داده شود ، به استثنای بیماریهای همزمان. میزان دفع آلبومین بیش از 20 میکروگرم در دقیقه یک علامت تشخیصی میکروآلبومینوری است ، نسبت آلبومین و میزان کراتینین بیش از 3 به شما امکان می دهد سطح قابل توجهی دفع شبانه بیش از 30 میکروگرم در دقیقه را پیش بینی کنید.
تغییرات در اندام تحتانی در سندرم پای دیابتی متمایز است. قطع عضو در اندام تحتانی در بیماران مبتلا به دیابت 15 برابر بیشتر از جمعیت انجام می شود.
بروز سندرم پای دیابتی با سن ، طول مدت بیماری ، گلیسمی ، سیگار کشیدن ، شدت فشار خون شریانی ارتباط دارد. سندرم پای دیابتی نه تنها با میکروآنژیوپاتی همراه با پلینیروپاتی ، آترواسکلروز از بین بردن عروق بزرگ و متوسط اندام تحتانی (ماکروآنژیوپاتی) یا با ترکیبی از این عوامل همراه است.
جبران طولانی مدت دیابت روند بیماریهای همزمان را بدتر می کند ، منجر به کاهش ایمنی ، بروز فرایندهای عفونی و التهابی و مزمن بودن آنها می شود.
لازم به ذکر است که بسیاری از پزشکان دیابت نوع II ، بیماری یک دوره خفیف تر را درک می کنند. دفتر اروپایی فدراسیون بین المللی دیابت شناسان و دفتر جهانی WHO اروپا در سال 1998 معیارهای جدیدی را برای جبران متابولیسم و خطر عوارض در بیماران مبتلا به دیابت نوع II پیشنهاد دادند که در جدول آورده شده است. 33.4
جدول 33.4. معیارهای جبران خسارتدیابت قندینوع دوم
گلوکز پلاسما خون وریدی بر روی معده خالی / قبل از غذا mmol / L (mg / dL) 6.1 (> 110)> 7.0 (> 126)
اتیولوژی بیماری
دیابت نوع 1 یک بیماری ارثی است ، اما یک پیش بینی ژنتیکی پیشرفت آن را تنها با یک سوم تعیین می کند. احتمال آسیب شناسی در کودک مبتلا به مادر دیابتی بیش از 1-2٪ نخواهد بود ، یک پدر بیمار - از 3 تا 6٪ ، خواهر و برادر - حدود 6٪.
یک یا چند نشانگر هومورال ضایعات لوزالمعده ، که شامل آنتی بادی های جزایر لانگرهانس است ، در 85-90٪ بیماران قابل تشخیص است:
- آنتی بادی های گلوتامات دکربوکسیلاز (GAD) ،
- آنتی بادی های تیروزین فسفاتاز (IA-2 و IA-2 بتا).
در این حالت ، مهمترین عامل در تخریب سلولهای بتا به عوامل ایمنی سلولی است. دیابت نوع 1 معمولاً با هاپلوتیپ HLA مانند DQA و DQB همراه است.
اغلب این نوع آسیب شناسی با سایر اختلالات خود ایمنی غدد درون ریز همراه است ، به عنوان مثال بیماری آدیسون ، تیروئیدیت خود ایمنی. اتیولوژی غیر غدد درون ریز نیز نقش مهمی ایفا می کند:
- ویتیلیگو
- آسیب شناسی روماتیسمی ،
- آلوپسی
- بیماری کرون.
پاتوژنز دیابت
 دیابت نوع 1 وقتی یک فرآیند خود ایمنی 80 تا 90 درصد سلولهای بتا لوزالمعده را از بین ببرد ، احساس دیابت می کند. علاوه بر این ، شدت و سرعت این روند پاتولوژیک همیشه متفاوت است. بیشتر اوقات ، در دوره کلاسیک این بیماری در کودکان و جوانان ، سلولها کاملاً سریع از بین می روند و دیابت به سرعت آشکار می شود.
دیابت نوع 1 وقتی یک فرآیند خود ایمنی 80 تا 90 درصد سلولهای بتا لوزالمعده را از بین ببرد ، احساس دیابت می کند. علاوه بر این ، شدت و سرعت این روند پاتولوژیک همیشه متفاوت است. بیشتر اوقات ، در دوره کلاسیک این بیماری در کودکان و جوانان ، سلولها کاملاً سریع از بین می روند و دیابت به سرعت آشکار می شود.
از زمان شروع بیماری و اولین علائم بالینی آن تا بروز کتواسیدوز یا کما کتواسیدوتیک ، بیش از چند هفته نمی تواند بگذرد.
در موارد دیگر ، بسیار نادر ، در بیماران مسن تر از 40 سال ، این بیماری می تواند به طور پنهانی ادامه یابد (دیابت خود ایمنی پنهان نه تنها لادا).
علاوه بر این ، در این شرایط ، پزشکان دیابت نوع 2 را تشخیص داده و به بیماران خود توصیه می کنند که در این روش می توانند کمبود انسولین را با داروهای سولفونیل اوره جبران کنند.
با این حال ، با گذشت زمان ، علائم کمبود هورمون مطلق شروع می شود:
- کتونوریا
- کاهش وزن
- هایپرگلیسمی آشکار در پس زمینه استفاده منظم از قرص ها برای کاهش قند خون.
پاتوژنز دیابت نوع 1 مبتنی بر کمبود مطلق هورمون است. به دلیل عدم امکان دریافت قند در بافتهای وابسته به انسولین (عضله و چربی) ، کمبود انرژی ایجاد می شود و در نتیجه لیپولیز و پروتئولیز شدیدتر می شوند. یک روند مشابه باعث کاهش وزن می شود.
با افزایش قند خون ، هیپراسمولاری رخ می دهد ، همراه با دیورز اسمزی و کم آبی. با کمبود انرژی و هورمون ، انسولین ترشح گلوکاگون ، کورتیزول و هورمون رشد را مهار می کند.
با وجود قند خون در حال رشد ، گلوکونوژنز تحریک می شود. تسریع لیپولیز در بافتهای چربی باعث افزایش چشمگیر در حجم اسیدهای چرب می شود.
اگر کمبود انسولین وجود داشته باشد ، توانایی لیپوسنتز کبد سرکوب می شود و اسیدهای چرب آزاد به طور فعال در کتوژنز دخیل هستند. تجمع کتون ها باعث ایجاد کتوز دیابتی و پیامد آن - کتواسیدوز دیابتی می شود.
در برابر پیش زمینه افزایش تدریجی کم آبی و اسیدوز ، یک اغما ایجاد می شود.
در صورت عدم معالجه (کافی انسولین درمانی و تجویز مجدد) ، تقریباً در 100٪ موارد منجر به مرگ خواهد شد.
علائم دیابت نوع 1
این نوع آسیب شناسی بسیار نادر است - بیش از 1.5-2 all از کل موارد بیماری. خطر بروز در طول زندگی 0.4٪ خواهد بود. اغلب ، فرد در سن 10 تا 13 سالگی به چنین دیابت مبتلا می شود. بخش عمده ای از تظاهرات آسیب شناسی تا 40 سال رخ می دهد.
اگر مورد معمولی باشد ، به ویژه در کودکان و نوجوانان ، این بیماری به عنوان علائم واضح ظاهر می شود. در چند ماه یا چند هفته می تواند توسعه یابد. عفونت ها و سایر بیماری های همزمان می توانند جلوه دیابت را تحریک کنند.
علائم مشخصه انواع دیابت است:
- پولیوریا
- خارش پوست ،
- پولییدپسی
این علائم به ویژه با بیماری نوع 1 ظاهر می شوند. در طول روز ، بیمار می تواند حداقل 5-10 لیتر مایعات بنوشاند و دفع کند.
خاص برای این نوع بیماری ، کاهش شدید وزن است که طی 1-2 ماه می تواند به 15 کیلوگرم برسد. علاوه بر این ، بیمار از:
- ضعف عضلانی
- خواب آلودگی
- کاهش عملکرد.
 در همان آغاز ، او ممکن است از افزایش غیر منطقی اشتها ناراحت شود ، که با افزایش کتواسیدوز با بی اشتهایی جایگزین می شود. بیمار بوی مشخصه استون از حفره دهان را تجربه می کند (ممکن است بو میوه ای وجود داشته باشد) ، حالت تهوع و شبه عمل جراحی - درد شکمی ، کم آبی شدید ، که می تواند باعث اغما شود.
در همان آغاز ، او ممکن است از افزایش غیر منطقی اشتها ناراحت شود ، که با افزایش کتواسیدوز با بی اشتهایی جایگزین می شود. بیمار بوی مشخصه استون از حفره دهان را تجربه می کند (ممکن است بو میوه ای وجود داشته باشد) ، حالت تهوع و شبه عمل جراحی - درد شکمی ، کم آبی شدید ، که می تواند باعث اغما شود.
در بعضی موارد ، اولین علامت دیابت نوع 1 در کودکان مبتلا به آگاهی با اختلال پیش رونده خواهد بود. می توان آنقدر تلفظ کرد که در پس زمینه آسیب شناسی های همزمان (جراحی یا عفونی) کودک ممکن است در حالت اغما قرار بگیرد.
این نادر است که یک بیمار بالاتر از 35 سال از بیماری دیابت رنج می برد (با دیابت خود ایمنی پنهان) ، بیماری ممکن است آنقدر احساس روشن نکند ، و در طی یک آزمایش معمول قند خون کاملاً تصادفی تشخیص داده می شود.
شخص دچار کاهش وزن نخواهد شد ، پولیوریا و پولییدپسی متوسط خواهد بود.
ابتدا پزشک می تواند دیابت نوع 2 را تشخیص داده و با کاهش دارو قند را در قرص ها شروع کند. این امر پس از مدتی جبران قابل قبول بیماری را تضمین می کند. با این وجود ، بعد از گذشت چند سال ، معمولاً بعد از 1 سال ، بیمار علائم ناشی از افزایش کمبود انسولین در کل را نشان می دهد:
- کاهش وزن چشمگیر
- کتوز
- کتواسیدوز
- عدم توانایی در حفظ سطح قند در حد لازم.
معیارهای تشخیص دیابت
با توجه به اینکه نوع 1 این بیماری با علائم واضح مشخص است و یک آسیب شناسی نادر است ، یک مطالعه غربالگری برای تشخیص سطح قند خون انجام نمی شود. احتمال ابتلا به دیابت نوع یک در بستگان نزدیک حداقل است ، که به همراه عدم وجود روشهای مؤثر برای تشخیص اولیه بیماری ، نامناسب بودن یک مطالعه دقیق از نشانگرهای ایمونوژنتیک پاتولوژی را در آنها تعیین می کند.
تشخیص این بیماری در بخش عمده ای از موارد براساس تعیین مقدار قابل توجهی از قند خون در بیمارانی که علائم کمبود انسولین مطلق دارند ، خواهد بود.
آزمایش خوراکی برای تشخیص بیماری بسیار نادر است.
آخرین مکان تشخیص افتراقی نیست. تأیید تشخیص در موارد مشکوک ، یعنی تشخیص قند خون متوسط در صورت عدم وجود علائم واضح و واضح دیابت نوع 1 ، به ویژه با تظاهر در سنین جوانی ، ضروری است.
هدف از چنین تشخیصی ممکن است تمایز بیماری از سایر انواع دیابت باشد. برای این کار ، روش تعیین سطح پایه پپتید C و 2 ساعت بعد از خوردن غذا استفاده کنید.
معیار ارزش تشخیص غیرمستقیم در موارد مبهم ، تعیین نشانگرهای ایمونولوژیک دیابت نوع 1 است:
- آنتی بادی های مجتمع جزایر پانکراس ،
- دکربوکسیلاز گلوتامات (GAD65) ،
- تیروزین فسفاتاز (IA-2 و IA-2P).
رژیم درمانی
درمان هر نوع دیابت مبتنی بر 3 اصل اساسی خواهد بود:
- کاهش قند خون (در مورد ما ، انسولین درمانی) ،
- رژیم غذایی
- آموزش بیمار
درمان با انسولین برای آسیب شناسی نوع 1 ماهیت جایگزینی دارد. هدف آن به حداکثر رساندن تقلید از ترشح طبیعی انسولین به منظور دستیابی به معیارهای جبران پذیرفته شده است. انسولین درمانی فشرده تولید فیزیولوژیکی هورمون را از نزدیک نزدیک می کند.
نیاز روزانه این هورمون با میزان ترشح پایه آن مطابقت دارد. 2 تزریق یک داروی با میانگین مدت زمان قرار گرفتن در معرض یا 1 تزریق انسولین طولانی گلارژین می تواند انسولین بدن را فراهم کند.
حجم کل هورمون بازال نباید بیش از نیمی از نیاز روزانه دارو باشد.
ترشح انسولین (تغذیه ای) انسولین با تزریق هورمون انسانی با مدت زمان کوتاه یا فوق العاده کوتاه از قرار گرفتن در معرض قبل از غذا جایگزین می شود. در این حالت ، دوز بر اساس معیارهای زیر محاسبه می شود:
- مقدار کربوهیدرات که قرار است در طول وعده های غذایی مصرف شود ،
- میزان قند خون موجود ، قبل از تزریق انسولین تعیین می شود (اندازه گیری شده با استفاده از گلوکومتر).
بلافاصله پس از تظاهرات دیابت نوع 1 و به محض شروع درمان آن برای مدت زمان کافی ، نیاز به آماده سازی انسولین ممکن است اندک باشد و کمتر از 0.3-0.4 U / kg باشد. این دوره "ماه عسل" یا مرحله بهبودی مداوم نامیده می شود.
پس از مرحله ای از قند خون و کتواسیدوز ، که در آن تولید انسولین با بقای سلول های بتا سرکوب می شود ، نقص هورمونی و متابولیک با تزریق انسولین جبران می شود. این داروها عملکرد سلولهای لوزالمعده را ترمیم می کنند ، که در نتیجه حداقل انسولین ترشح می کنند.
این دوره می تواند از دو هفته تا چند سال ادامه یابد. در نهایت ، با این حال ، به عنوان یک نتیجه از بین رفتن خود ایمنی باقیمانده سلول بتا ، مرحله بهبودی به پایان می رسد و نیاز به درمان جدی است.
دیابت قند غیر وابسته به انسولین (نوع 2)
این نوع آسیب شناسی زمانی ایجاد می شود که بافت های بدن قادر به جذب کافی قند یا انجام آن در حجم ناقص نیستند. یک مشکل مشابه نام دیگری دارد - نارسایی خارج از بدن. علت این پدیده ممکن است متفاوت باشد:
- تغییر در ساختار انسولین با ایجاد چاقی ، پرخوری ، شیوه زندگی بی تحرک ، فشار خون شریانی ، در سن و حضور اعتیاد ،
- نقص در عملکرد گیرنده های انسولین به دلیل نقض تعداد یا ساختار آنها ،
- تولید ناکافی قند توسط بافتهای کبدی ،
- آسیب شناسی داخل سلولی ، که در آن انتقال یک ضربه به اندام های سلولی از گیرنده انسولین دشوار است ،
- تغییر در ترشح انسولین در پانکراس.
طبقه بندی بیماری ها
بسته به شدت دیابت نوع 2 ، به موارد زیر تقسیم می شود:
- درجه خفیف این ویژگی با توانایی جبران کمبود انسولین ، منوط به استفاده از داروها و رژیمهای غذایی است که می تواند قند خون را در مدت زمان کوتاهی کاهش دهد ،
- درجه متوسط شما می توانید تغییرات متابولیکی را جبران کنید به شرطی که حداقل 2-3 دارو برای کاهش گلوکز استفاده شود. در این مرحله ، یک نارسایی متابولیک با آنژیوپاتی همراه خواهد بود ،
- مرحله شدید برای عادی سازی شرایط نیاز به استفاده از چندین وسیله کاهش قند و تزریق انسولین است. بیمار در این مرحله اغلب از عوارض رنج می برد.
دیابت نوع 2 چیست؟
تصویر بالینی کلاسیک دیابت شامل 2 مرحله است:
- مرحله سریع تخلیه فوری انسولین انباشته در پاسخ به گلوکز ،
- مرحله آهسته ترشح انسولین به منظور کاهش قند خون باقیمانده کند است. این کار بلافاصله پس از مرحله سریع شروع به کار می کند ، اما منوط به تثبیت کافی کربوهیدرات ها است.
اگر آسیب شناسی سلولهای بتا وجود داشته باشد که نسبت به اثرات هورمون پانکراس حساس نشوند ، عدم تعادل در میزان کربوهیدرات های خون به تدریج ایجاد می شود. در دیابت نوع 2 ، مرحله سریع به سادگی وجود ندارد ، و مرحله آهسته غالب است. تولید انسولین ناچیز است و به همین دلیل تثبیت فرآیند امکان پذیر نیست.
 هنگامی که عملکرد گیرنده انسولین یا مکانیسم های پس از گیرنده کافی نباشد ، هیپرینسولینمی ایجاد می شود. بدن با داشتن انسولین زیاد در خون ، مکانیسم جبران خسارت خود را شروع می کند که هدف از آن تثبیت تعادل هورمونی است. این علامت مشخصه حتی در همان ابتدای بیماری مشاهده می شود.
هنگامی که عملکرد گیرنده انسولین یا مکانیسم های پس از گیرنده کافی نباشد ، هیپرینسولینمی ایجاد می شود. بدن با داشتن انسولین زیاد در خون ، مکانیسم جبران خسارت خود را شروع می کند که هدف از آن تثبیت تعادل هورمونی است. این علامت مشخصه حتی در همان ابتدای بیماری مشاهده می شود.
تصویری آشکار از آسیب شناسی بعد از چند سال پرکاری قند خون مداوم ایجاد می شود. قند خون بیش از حد بر سلولهای بتا تأثیر منفی می گذارد. این امر به دلیل کاهش تولید و انسولین آنها می شود و باعث کاهش تولید انسولین می شود.
از نظر بالینی ، کمبود انسولین با تغییر در وزن و تشکیل کتواسیدوز آشکار می شود. علاوه بر این ، علائم دیابت از این نوع عبارتند از:
- پولییدپسی و پولیوریا. سندرم متابولیک به دلیل قند خون ، که باعث افزایش فشار خون اسمزی می شود ، ایجاد می شود. برای عادی سازی روند ، بدن شروع به از بین بردن فعالانه آب و الکترولیت ها می کند ،
- خارش پوست. خارش پوست به دلیل افزایش شدید اوره و کتون در خون ،
- اضافه وزن
مقاومت به انسولین باعث ایجاد عوارض زیادی ، اعم از اولیه و ثانویه خواهد شد. بنابراین ، گروه اول پزشکان عبارتند از: هایپرگلیسمی ، کاهش سرعت تولید گلیکوژن ، گلوکوزوری ، مهار واکنش های بدن.
دسته دوم عوارض شامل موارد زیر است: تحریک ترشح لیپیدها و پروتئین برای تبدیل آنها به کربوهیدرات ها ، جلوگیری از تولید اسیدهای چرب و پروتئین ها ، کاهش تحمل نسبت به کربوهیدراتهای مصرفی ، اختلال در ترشح سریع هورمون پانکراس.
دیابت نوع 2 به اندازه کافی شایع است. به طور کلی ، شاخص های واقعی شیوع بیماری می تواند از حداقل رسمی 2-3 برابر فراتر رود.
علاوه بر این ، بیماران فقط پس از شروع عوارض جدی و خطرناک به دنبال کمک پزشکی هستند. به همین دلیل ، غدد درون ریز اصرار دارند که مهم است که معاینات منظم پزشکی را فراموش نکنید. آنها به شناسایی هر چه سریعتر مشکل کمک می کنند و به سرعت شروع به درمان می کنند.
|


 دیابت نوع 1 وقتی یک فرآیند خود ایمنی 80 تا 90 درصد سلولهای بتا لوزالمعده را از بین ببرد ، احساس دیابت می کند. علاوه بر این ، شدت و سرعت این روند پاتولوژیک همیشه متفاوت است. بیشتر اوقات ، در دوره کلاسیک این بیماری در کودکان و جوانان ، سلولها کاملاً سریع از بین می روند و دیابت به سرعت آشکار می شود.
دیابت نوع 1 وقتی یک فرآیند خود ایمنی 80 تا 90 درصد سلولهای بتا لوزالمعده را از بین ببرد ، احساس دیابت می کند. علاوه بر این ، شدت و سرعت این روند پاتولوژیک همیشه متفاوت است. بیشتر اوقات ، در دوره کلاسیک این بیماری در کودکان و جوانان ، سلولها کاملاً سریع از بین می روند و دیابت به سرعت آشکار می شود. در همان آغاز ، او ممکن است از افزایش غیر منطقی اشتها ناراحت شود ، که با افزایش کتواسیدوز با بی اشتهایی جایگزین می شود. بیمار بوی مشخصه استون از حفره دهان را تجربه می کند (ممکن است بو میوه ای وجود داشته باشد) ، حالت تهوع و شبه عمل جراحی - درد شکمی ، کم آبی شدید ، که می تواند باعث اغما شود.
در همان آغاز ، او ممکن است از افزایش غیر منطقی اشتها ناراحت شود ، که با افزایش کتواسیدوز با بی اشتهایی جایگزین می شود. بیمار بوی مشخصه استون از حفره دهان را تجربه می کند (ممکن است بو میوه ای وجود داشته باشد) ، حالت تهوع و شبه عمل جراحی - درد شکمی ، کم آبی شدید ، که می تواند باعث اغما شود. هنگامی که عملکرد گیرنده انسولین یا مکانیسم های پس از گیرنده کافی نباشد ، هیپرینسولینمی ایجاد می شود. بدن با داشتن انسولین زیاد در خون ، مکانیسم جبران خسارت خود را شروع می کند که هدف از آن تثبیت تعادل هورمونی است. این علامت مشخصه حتی در همان ابتدای بیماری مشاهده می شود.
هنگامی که عملکرد گیرنده انسولین یا مکانیسم های پس از گیرنده کافی نباشد ، هیپرینسولینمی ایجاد می شود. بدن با داشتن انسولین زیاد در خون ، مکانیسم جبران خسارت خود را شروع می کند که هدف از آن تثبیت تعادل هورمونی است. این علامت مشخصه حتی در همان ابتدای بیماری مشاهده می شود.