دیابت مرکزی insipidus - درک فعلی از تشخیص و درمان
دیابت بیضه (ND) (دیابت لاتین insipidus) - بیماری ناشی از نقض سنتز ، ترشح یا عمل وازوپرسین ، که با دفع مقدار زیادی ادرار با چگالی نسبی پایین (پلی اوریای هیپوتونیک) ، کم آبی و تشنگی بروز می کند.
اپیدمیولوژی. شیوع ND در جمعیت های مختلف از 0.004 to به 0.01 aries متغیر است. یک روند جهانی به سمت افزایش شیوع ND وجود دارد ، به ویژه به دلیل شکل اصلی آن ، که با افزایش تعداد مداخلات جراحی انجام شده بر روی مغز و همچنین تعداد صدمات کرانیوسر مغزی همراه است ، که در این موارد موارد توسعه ND حدود 30 درصد است. اعتقاد بر این است که ND به همان اندازه بر زنان و مردان نیز تأثیر می گذارد. بروز اوج در سن 30-20 سالگی رخ می دهد.
نام پروتکل: دیابت بیضه
کد (کدها) مطابق با ICD-10:
E23.2 - دیابت بیضه
تاریخ توسعه پروتکل: آوریل 2013
اختصارات مورد استفاده در پروتکل:
ND - دیابت مایع
PP - پولییدپسی اولیه
MRI - تصویربرداری با رزونانس مغناطیسی
HELL - فشار خون
دیابت قندی
سونوگرافی - سونوگرافی
دستگاه گوارش
NSAIDs - داروهای ضد التهابی غیر استروئیدی
CMV - سیتومگالوویروس
رده بیمار: زنان و مردان 20 تا 30 سال ، سابقه صدمات ، مداخلات جراحی مغز و اعصاب ، تومورها (کرانیوفارنژما ، میکروبوز ، گلیوما و غیره) ، عفونت ها (عفونت مادرزادی CMV ، توکسوپلاسموز ، آنسفالیت ، مننژیت).
کاربران پروتکل: پزشک منطقه ، غدد درونریز پلی کلینیک یا بیمارستان ، جراح مغز و اعصاب بیمارستان ، جراح تروما در بیمارستان ، متخصص اطفال.
طبقه بندی
طبقه بندی بالینی:
رایج ترین آنها:
1. مرکزی (هیپوتالاموس ، هیپوفیز) ، به دلیل اختلال در سنتز و ترشح وازوپرسین.
2. نفروژنیک (کلیوی ، مقاوم به وازوپرسین) ، که با مقاومت کلیوی در برابر وازوپرسین مشخص می شود.
3. پولیسپسی اولیه: اختلال در هنگام تشنگی پاتولوژیک (پلی پپسی دیپوژنیک) یا یک فشار اجباری برای نوشیدن (روان پریشی روانی) و مصرف بیش از حد آب در آن باعث مهار ترشح فیزیولوژیکی وازوپرسین می شود و در نتیجه علائم مشخصی از بیماری دیابت بی حس کننده ایجاد می شود ، در حالی که سنتز وازوپرس منجر به کم آبی می شود. در حال ترمیم است
سایر انواع نادر دیابت بیضه نیز مشخص می شوند:
1- پروژستوژن همراه با افزایش فعالیت آنزیم جفت - آرژنین آمینوپپتیداز ، که وازوپرسین را از بین می برد. بعد از زایمان ، وضعیت عادی می شود.
2- کارکردی: در کودکان سال اول زندگی رخ می دهد و به دلیل عدم بلوغ مکانیسم غلظت کلیه ها و افزایش فعالیت فسفودی استراز نوع 5 ایجاد می شود که منجر به غیرفعال شدن سریع گیرنده برای وازوپرسین و مدت زمان کوتاهی از عمل وازوپرسین می شود.
3. Iatrogenic: استفاده از داروهای مدر.
طبقه بندی ND با توجه به شدت دوره:
1. خفیف - ادرار تا 6-8 لیتر در روز بدون درمان ،
2. متوسط - خروج ادرار تا 8-14 لیتر در روز بدون درمان ،
3. شدید - ادرار بیش از 14 لیتر در روز بدون درمان.
طبقه بندی ND با توجه به میزان جبران خسارت:
1. جبران خسارت - در درمان تشنگی و پولیورا زحمت نمی کشند ،
2. کم هزینه - در طول درمان قسمت هایی از تشنگی و پلیوریا در طول روز وجود دارد ،
3. جبران خسارت - عطش و پولیوریا ماندگار است.
تشخیصی
لیست اقدامات اساسی و تشخیصی اضافی:
اقدامات تشخیصی قبل از بستری در بیمارستان:
- تجزیه و تحلیل کلی ادرار ،
- تجزیه و تحلیل بیوشیمیایی خون (پتاسیم ، سدیم ، کلسیم کل ، کلسیم یونیزه شده ، گلوکز ، پروتئین کل ، اوره ، کراتینین ، اسمولالیته خون) ،
- ارزیابی دیورز (> 40 میلی لیتر در کیلوگرم در روز ،> 2 لیتر در مترمربع در روز ، اسمالی بودن ادرار ، تراکم نسبی).
اقدامات اصلی تشخیصی:
- نمونه با خوردن خشک (تست کم آبی) ،
- تست با دسموپرسین ،
- MRI ناحیه هیپوتالاموس-هیپوفیز
اقدامات تشخیصی اضافی:
- سونوگرافی کلیه ،
- آزمایش عملکرد دینامیک کلیه
معیارهای تشخیصی:
شکایات و بیهوشی:
تظاهرات اصلی ND پلی اوریای شدید (خروج ادرار بیش از 2 لیتر در مترمربع در روز یا 40 میلی لیتر در کیلوگرم در روز در کودکان بزرگتر و بزرگسالان) ، پولییدپسی (3-18 لیتر در روز) و اختلالات مربوط به خواب است. اولویت برای آب سرد / یخ معمولی مشخص است. ممکن است پوست خشک و غشاهای مخاطی ، کاهش بزاق و تعریق وجود داشته باشد. معمولاً اشتها کاهش می یابد. شدت علائم بستگی به میزان نارسایی عصبی و عصبی دارد. با کمبود جزئی وازوپرسین ، علائم بالینی ممکن است به وضوح مشخص نباشد و در شرایط محرومیت از نوشیدن یا از بین رفتن بیش از حد مایعات ظاهر شود. در هنگام جمع آوری بیهوشی ، لازم است مدت و ماندگاری علائم در بیماران ، وجود علائم پولیپسی ، پلی اوری ، دیابت در بستگان ، تاریخچه جراحات ، مداخلات عصبی ، تومورهای (کرانیوفارنژیوما ، germinoma ، گلیوما و غیره) ، عفونت ها (عفونت مادرزادی CMV) مشخص شود. ، توکسوپلاسموز ، آنسفالیت ، مننژیت).
در نوزادان و نوزادان ، تصویر بالینی این بیماری با بزرگسالان متفاوت است ، زیرا آنها نمی توانند تمایل خود را برای افزایش مصرف مایعات ابراز کنند ، که تشخیص به موقع را پیچیده می کند و می تواند منجر به ایجاد صدمه غیر قابل برگشت مغز شود. چنین بیمارانی ممکن است کاهش وزن ، پوست خشک و کم رنگ ، عدم وجود اشک و تعریق و افزایش درجه حرارت بدن را تجربه کنند. آنها ممکن است شیر مادر را به آب ترجیح دهند و بعضی اوقات بیماری فقط بعد از شیر دادن به کودک علامت دار می شود. اسمولالیته ادرار کم است و بندرت از 150-200 mmol / kg تجاوز می کند ، اما پلی اوریا فقط در صورت افزایش مصرف مایعات کودک ظاهر می شود. در کودکان در این سن کم ، هایپرناترمیا و بیش فعالی خون با تشنج و اغما بسیار سریع و به سرعت ایجاد می شوند.
در کودکان بزرگتر ممکن است تشنگی و پولیوریا در علائم بالینی ظاهر شود ، با مصرف ناکافی مایعات ، قسمت هایی از هیپرناترمیا اتفاق می افتد که می تواند به حالت اغما و گرفتگی پیش رود. کودکان ضعیف رشد می کنند و افزایش وزن می یابند ، در هنگام خوردن غذا اغلب دچار استفراغ می شوند ، عدم اشتها ، شرایط هیپوتونیک ، یبوست ، عقب ماندگی ذهنی مشاهده می شود. کمبود آشکار هیپرتونیک فقط در موارد عدم دسترسی به مایعات رخ می دهد.
معاینه جسمی:
در معاینه ممکن است علائم کم آبی بدن وجود داشته باشد: خشکی پوست و غشاهای مخاطی. فشار خون سیستولیک طبیعی است یا کمی کاهش یافته است ، فشار خون دیاستولیک افزایش می یابد.
تحقیقات آزمایشگاهی:
با توجه به تجزیه و تحلیل کلی ادرار ، آن را تغییر رنگ می دهد ، هیچ عنصر پاتولوژیکی ، با چگالی نسبی پایین (1000-1005) ندارد.
برای تعیین توانایی غلظت کلیه ها ، آزمایش مطابق زیمیتسکی انجام می شود. اگر در هر بخشی از وزن مخصوص ادرار بالاتر از 1.010 باشد ، می توان از تشخیص ND خارج شد ، اما باید به خاطر داشت که وجود قند و پروتئین در ادرار ، وزن مخصوص ادرار را افزایش می دهد.
بیش فعالی پلاسما بیش از 300 مومول بر کیلوگرم است. به طور معمول ، اسمولالیته پلاسما 280-290mmol / kg است.
کمبود ادرار (کمتر از 300 مومول بر کیلوگرم).
هایپرناترمیا (بیش از 155 meq / l).
با فرم مرکزی ND ، کاهش سطح وازوپرسین در سرم خون مشاهده می شود و با فرم نفروژنیک ، طبیعی یا کمی افزایش یافته است.
تست کم آبی (آزمایش با خوردن خشک). پروتکل تست کم آبی G.I. رابرتسون (2001).
فاز دهیدراسیون:
- از نظر اسمولالیته و سدیم خون بگیرید (1)
- جمع آوری ادرار برای تعیین حجم و اسمولالیته (2)
- اندازه گیری وزن بیمار (3)
- کنترل فشار خون و ضربان قلب (4)
متعاقباً ، در فواصل زمانی برابر ، بسته به شرایط بیمار ، مراحل 1-4 را بعد از 1 یا 2 ساعت تکرار کنید.
مجاز به نوشیدن بیمار نیست ، همچنین توصیه می شود که غذا را محدود کنید ، حداقل در 8 ساعت اول آزمایش. هنگام تغذیه غذا نباید حاوی آب زیادی باشد و کربوهیدرات های قابل هضم آسان ، تخم مرغ آب پز ، نان دانه ، گوشت کم چرب ، ماهی ترجیح داده می شود.
نمونه متوقف می شود که:
- از دست دادن بیش از 5٪ از وزن بدن
- عطش غیرقابل تحمل
- وضعیت عینی جدی بیمار
- افزایش میزان سدیم و اسمولالیته خون بالاتر از حد طبیعی.
تست دسموپرسین. این آزمایش بلافاصله پس از پایان آزمایش کم آبی بدن ، در صورت رسیدن به حداکثر امکان ترشح / عمل وازوپرسین درون زا انجام می شود. به بیمار 1/0 میلی گرم قرص دسموپرسین قرص زیر زبان داده می شود تا زمان جذب کامل یا 10 میکروگرم به صورت داخل رحمی به صورت اسپری انجام شود. میزان اسمولالیت ادرار قبل از دسموپرسین و 2 و 4 ساعت بعد از آن اندازه گیری می شود. در طول آزمایش ، بیمار مجاز به نوشیدن ، اما بیش از 1.5 برابر حجم دفع ادرار ، در آزمایش کم آبی بدن نیست.
تفسیر نتایج آزمایش با دسموپرسین: پولییدپسی معمولی یا اولیه منجر به غلظت ادرار بالای 600-700 مومول بر کیلوگرم ، اسمولالیته خون و سدیم در حد طبیعی باقی می ماند ، بهزیستی به طور قابل توجهی تغییر نمی کند. دسموپرسین عملاً باعث افزایش اسمولالیت ادرار نمی شود ، زیرا حداکثر غلظت آن در حال حاضر رسیده است.
با وجود ND مرکزی ، اسمالی بودن ادرار در هنگام کمبود آب از اسمزیت خون تجاوز نمی کند و در کمتر از 300 مومول بر کیلوگرم ، افزایش اسمولالیسم خون و سدیم ، افزایش عطش مشخص شده ، غشاهای مخاطی خشک ، افزایش یا کاهش فشار خون ، تاکی کاردی باقی می ماند. با معرفی دسموپرسین ، میزان اسمالی بودن ادرار بیش از 50٪ افزایش می یابد. با ND نفروژنیک ، میزان اسم خون بودن خون و سدیم افزایش می یابد ، میزان اسمولیته ادرار کمتر از 300 مومول بر کیلوگرم مانند ND مرکزی است ، اما پس از استفاده از دسموپرسین ، اسمالی بودن ادرار عملا افزایش نمی یابد (افزایش تا 50٪).
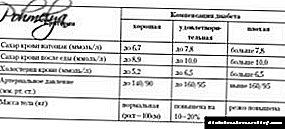
تفسیر نتایج نمونه ها در برگه خلاصه می شود. .
اسمولالیت ادرار (مومول / کیلوگرم) | تشخیص | |
| تست کم آبی | تست دسموپرسین | |
| >750 | >750 | نرمال یا PP |
| >750 | ND مرکزی | |
| نفروژنیک ND | ||
| 300-750 | ND مرکزی جزئی ، ND جزئی نفروژنیک ، PP | |
تحقیقات ابزاری:
ND مرکزی یک نشانگر پاتولوژی منطقه هیپوتالاموس-هیپوفیز در نظر گرفته می شود. MRI مغز روش انتخابی در تشخیص بیماری های ناحیه هیپوتالاموس-هیپوفیز است. با استفاده از ND مرکزی ، این روش نسبت به CT و سایر روشهای تصویربرداری مزایای بسیاری دارد.
از MRI مغز برای شناسایی دلایل ND مرکزی (تومورها ، بیماریهای نفوذی ، بیماریهای گرانولوماتوز غده هیپوتالاموس و غده هیپوفیز و غیره) استفاده می شود .در مورد دیابت نفروژنیک بیضه: آزمایش های پویا از وضعیت عملکرد کلیه و سونوگرافی کلیه ها استفاده می شود.در صورت عدم وجود تغییرات پاتولوژیکی طبق MRI ، این مطالعه توصیه می شود. در دینامیک ، از آنجا که مواردی وجود دارد که ND مرکزی چند سال قبل از تشخیص تومور ظاهر می شود
نشانه های مشاوره متخصص:
اگر تغییرات پاتولوژیک در ناحیه هیپوتالاموس هیپوفیز مشکوک باشد ، مشاوره با جراح مغز و اعصاب و چشم پزشک نشان داده می شود. اگر آسیب شناسی سیستم ادراری تشخیص داده شود - یک متخصص اورولوژی ، و هنگام تأیید نوع روانی پولیپسی ، مشاوره با روانپزشک یا روانپزشک عصبی لازم است.
سنتز و ترشح هورمون ضد دیورتیک
وازوپرسین هورمون ضد دیورتیک در هسته های فوق مغزی و فوق سنگین هیپوتالاموس سنتز می شود. با تماس با نوروفیزین ، این مجتمع به صورت گرانول به پسوندهای انتهایی آکسونهای نوروفیزیس و ارتفاع متوسط منتقل می شود. در آکسون که در تماس با مویرگها به پایان می رسد ، تجمع ADH اتفاق می افتد. ترشح ADH بستگی به اسمولالیته پلاسما ، گردش خون و گردش خون دارد. سلول های حساس به اسمزی که در قسمت های بطنی نزدیک هیپوتالاموس قدامی واقع شده اند ، نسبت به تغییرات در ترکیب الکترولیت خون واکنش نشان می دهند. افزایش فعالیت osmoreceptors با افزایش اسمولالیته خون ، سلولهای عصبی وازوپرسینرژیک را تحریک می کند ، که از انتهای آن وازوپرسین در جریان خون عمومی رها می شود. در شرایط فیزیولوژیکی ، اسمولالیسم پلاسما در محدوده 282-300 mOsm / kg است. به طور معمول ، آستانه ترشح ADH اسمولالیته پلاسما خون از 280 mOsm / kg است. مقادیر کمتری برای ترشح ADH در دوران بارداری ، روانپزشکی حاد و بیماریهای انکولوژیکی مشاهده می شود. کاهش اسمولالیته پلاسما ناشی از جذب مقدار زیادی مایعات باعث ترشح ترشح ADH می شود. با سطح اسمولالیته پلاسما بیش از 295 mOsm / kg ، افزایش ترشح ADH و فعال سازی مرکز تشنگی ذکر شده است. مرکز فعال تشنگی و ADH که توسط اسمورسپتورهای عروق خلفی قسمت قدامی هیپوتالاموس کنترل می شود ، از کمبود بدن جلوگیری می کند.

تنظیم ترشح وازوپرسین نیز به تغییر در حجم خون بستگی دارد. با خونریزی ، گیرنده های حجمی واقع در دهلیز چپ تأثیر معنی داری بر ترشح وازوپرسین دارند. در عروق ، فشار خون از طریق سلولهای عضله صاف رگهای خونی واقع می شود. اثر انقباض عروق وازوپرسین در هنگام از دست دادن خون به دلیل كاهش لایه عضله صاف رگ است كه از افت فشار خون جلوگیری می كند. با کاهش فشار خون بیش از 40٪ ، افزایش سطح ADH ، 100 برابر بیشتر از غلظت پایه آن 1 ، 3 وجود دارد. بارورسپتورهای واقع در سینوس کاروتید و قوس آئورت به افزایش فشار خون پاسخ می دهند ، که در نهایت منجر به کاهش ترشح ADH می شود. علاوه بر این ، ADH در تنظیم هموستاز ، سنتز پروستاگلاندین ها نقش دارد و باعث آزاد سازی رنین می شود.
یون های سدیم و مانیتول محرک قوی ترشح وازوپرسین هستند. اوره تاثیری در ترشح هورمون ندارد و گلوکز منجر به مهار ترشح آن می شود.
مکانیسم عمل هورمون ضد دیورتیک
ADH مهمترین تنظیم کننده احتباس آب است و هموستاز مایع را در رابطه با هورمون ناتریورتیک دهلیزی ، آلدوسترون و آنژیوتانسین II فراهم می کند.
اثر فیزیولوژیکی اصلی وازوپرسین تحریک جذب مجدد آب در لوله های جمع آوری قشر کلیه و مدولا در برابر گرادیان فشار اسمزی است.
در سلولهای توبولهای کلیوی ، ADH از طریق (گیرنده های وازوپرسین نوع 2) عمل می کند ، که در غشای پایه سلولهای توبول های جمع کننده قرار دارند. تعامل ADH با منجر به فعال شدن آدنیلات سیکلاز حساس به وازوپرسین و افزایش تولید مونوفسفات آدنوزین حلقوی (AMP) می شود. AMP حلقوی پروتئین کیناز A را فعال می کند ، که به نوبه خود باعث اختلاط پروتئین های کانال آب در غشای آپیکال سلول ها می شود. این امر انتقال آب از لامپ لوله های جمع آورنده به داخل سلول و موارد دیگر را تضمین می کند: از طریق پروتئین های کانال های آبی که در غشای پایه قرار گرفته اند و آب به فضای بین سلولی و سپس به رگ های خونی منتقل می شود. در نتیجه ، ادرار غلیظ با اسمولالیته بالا تشکیل می شود.

غلظت اسمزی غلظت کل ذرات حل شده است. می توان آن را به عنوان اسمولاریته تفسیر کرد و در اسمول در لیتر یا اندازه گیری اسمولالیت در اسمول / کیلوگرم اندازه گیری کرد. تفاوت اسمولاریته و اسمالی بودن در روش به دست آوردن این مقدار نهفته است. برای اسمولاریته ، این یک روش محاسبه غلظت الکترولیتهای اساسی در مایع اندازه گیری شده است. فرمول محاسبه اسمولاریته:
اسمولاریته = 2 x اسمولالیته پلاسما ، ادرار و سایر مایعات بیولوژیکی فشار اسمزی است که به میزان یون ها ، گلوکز و اوره بستگی دارد که با استفاده از دستگاه اسمومتر مشخص می شود. از نظر فشار تورمی میزان اسمولالیته کمتر از اسمولاریته است. با ترشح عادی ADH ، اسمولاریته ادرار همیشه بالاتر از 300 mOsm / l است و حتی می تواند تا 1200 mOsm / L و بیشتر شود. با کمبود ADH ، اسمولالیته ادرار زیر 200mm / l 4 ، 5 است. از جمله دلایل اصلی ابتلا به LPC ، یک شکل خانوادگی ارثی از بیماری منتقل می شود که توسط یا نوع ارث منتقل می شود. وجود این بیماری در چند نسل قابل ردیابی است و می تواند تعدادی از اعضای خانواده را تحت تأثیر قرار دهد ، این به دلیل جهش هایی است که منجر به تغییر در ساختار ADH (سندرم DIDMOAD) می شود. نقایص مادرزادی آناتومیک در ایجاد اواسط و دیانسفالون نیز می تواند علل اصلی ایجاد بیماری مغزی کم فشار باشد. در 50-60 cases از موارد ، علت اصلی درد کم فشار نمی تواند مشخص شود - این به اصطلاح دیابت ایدیوپاتیک insipidus است. از جمله دلایل ثانویه که منجر به ایجاد سیستم عصبی مرکزی می شود ، تروما (ضربه مغزی ، آسیب دیدگی چشم ، شکستگی پایه جمجمه) تروما نامیده می شود. ایجاد NSD ثانویه ممکن است با شرایط پس از انجام عمل جراحی transcranial یا transsphenoidal روی غده هیپوفیز برای تومورهای مغزی مانند کرانیوفارنژیوما ، pinealoma ، germinoma همراه باشد و منجر به فشرده سازی و آتروفی غده هیپوفیز خلفی شود. همچنین تغییرات التهابی در هیپوتالاموس ، دستگاه فوق حاد ، فشار خون ، قیف ، پاها ، لوب خلفی غده هیپوفیز نیز از علل ثانویه ایجاد فشار خون پایین هستند. عامل اصلی در بروز شکل ارگانیک بیماری عفونت است. از جمله بیماری های عفونی حاد ، آنفولانزا ، آنسفالیت ، مننژیت ، لوزه تب ، اسکارال ، سرفه بزرگ ، از جمله بیماری های عفونی مزمن - سل ، تب مالت ، سفلیس ، مالاریا ، روماتیسم 9 ، 10 است. از جمله دلایل عروقی دیسپلازی عصبی کم فشار می توان به سندرم Skien ، اختلال در خونرسانی به نوروفیپوفیز ، ترومبوز و آنوریسم اشاره کرد. بسته به محل آناتومیک ، LPC می تواند دائمی یا گذرا باشد. با آسیب رسیدن به هسته های ماوراء بنفش و paraventricular ، عملکرد ADH بهبود نمی یابد. توسعه ND نفروژنیک مبتنی بر گیرنده مادرزادی یا اختلالات آنزیمی لوله های دیستال کلیه ها است و منجر به مقاومت گیرنده ها در برابر عملکرد ADH می شود. در این حالت ، محتوای ADH درون زا می تواند طبیعی یا بالا باشد و مصرف ADH علائم بیماری را از بین نمی برد. نفروژنیک ND می تواند در عفونتهای مزمن طولانی مدت دستگاه ادراری ، urolithiasis (ICD) و آدنوم پروستات رخ دهد. ND نفروژنیک علامتدار می تواند در بیماریهایی همراه با آسیب به لوله های دیستال کلیه ها مانند کم خونی ، سارکوئیدوز ، آمیلوئیدوز ایجاد شود. در شرایط هیپرکلسمی ، حساسیت به ADH کاهش می یابد و جذب مجدد آب کاهش می یابد. پلیدیپسی روانی در سیستم عصبی عمدتاً در زنان در سن یائسگی ایجاد می شود (جدول 1). بروز اولیه عطش ناشی از اختلالات عملکردی در مرکز عطش است. تحت تأثیر مقدار زیادی مایع و افزایش حجم پلاسما در گردش ، کاهش ترشح ADH از طریق مکانیسم بارورسپتور اتفاق می افتد. آزمایش ادرار طبق زیمیتسکی در این بیماران کاهش تراکم نسبی را نشان می دهد ، در حالی که غلظت سدیم و اسمولاریته خون خون طبیعی و یا کاهش می یابد. هنگام محدود کردن مصرف مایعات ، بهزیستی بیماران رضایت بخش می ماند ، در حالی که مقدار ادرار کاهش می یابد ، و میزان اسمولاریت آن تا حد فیزیولوژیکی بالا می رود. برای تظاهرات ND ، لازم است که توانایی ترشح عصبی هیپوفیز 85٪ 2 ، 8 کاهش یابد. علائم اصلی ND ادرار بیش از حد و تشنگی شدید است. اغلب حجم ادرار از 5 لیتر فراتر می رود ، حتی می تواند به 8-10 لیتر در روز برسد. بیش فعالی خون پلاسما باعث تحریک مرکز تشنگی می شود. بیمار بدون مصرف مایعات بیش از 30 دقیقه نمی تواند انجام دهد. مقدار مایعات مست با نوعی خفیف بیماری معمولاً به 3-5 لیتر می رسد ، با شدت متوسط - 5-8 لیتر ، با فرم شدید - 10 لیتر یا بیشتر. ادرار از بین رفته است و تراکم نسبی آن 1000-1003 است. در شرایط مصرف بیش از حد مایعات در بیماران ، اشتها کاهش می یابد ، معده بیش از حد کشیده می شود ، ترشحات کاهش می یابد ، تحرک دستگاه گوارش کند می شود ، یبوست ایجاد می شود. هنگامی که ناحیه هیپوتالاموس تحت تأثیر یک فرآیند التهابی یا آسیب زا قرار دارد ، همراه با ND ، اختلالات دیگری نیز مشاهده می شود ، از جمله چاقی ، آسیب شناسی رشد ، گالاکتوره ، کم کاری تیروئید ، دیابت قندی (DM) 3 ، 5. با پیشرفت بیماری ، دهیدراته شدن منجر به خشکی پوست و غشاهای مخاطی و کاهش بزاق می شود. - و تعریق ، ایجاد استوماتیت و نازوفارنژیت. با کم آبی شدید ، ضعف عمومی ، تپش قلب افزایش می یابد ، کاهش فشار خون ذکر می شود ، سردرد به سرعت تشدید می شود ، حالت تهوع ظاهر می شود. بیماران تحریک پذیر می شوند ، ممکن است توهم ، تشنج ، حالت کولاپوئید وجود داشته باشد.عوامل اتیولوژیک دیابت مرکزی insipidus
تصویر بالینی دیابت مرکزی insipidus