تأیید اثربخشی دارو Milgamma Compositum در نوروپاتی دیابتی و الکلی
R.A. MANUSHAROVA ، دکتر ، استاد ، D.I. CHERKEZOV
گروه غدد درون ریز و دیابت با دوره جراحی غدد درون ریز
GOU DPO RMA PO وزارت بهداشت اجتماعی ، مسکو ، روسیه
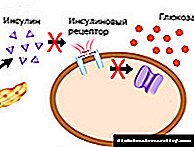
در بیماران مبتلا به دیابت عوارض قلبی و عروقی بسیار بیشتر از افراد فاقد دیابت است. با این حال ، حفظ ثبات سطح گلوکز و پیشگیری / درمان زودرس به کاهش مرگ و میر و بهبود کیفیت زندگی کمک می کند بیماران دیابتی. با افزایش دیابت ، بروز عوارض میکروواسکولار افزایش می یابد. می توان فرض کرد که با افزایش شیوع دیابت ، که در حال حاضر مشاهده می شود ، نقش عوارض میکروواسکولار نیز در آینده افزایش می یابد. فراوانی بروز چنین عوارض ریز عروقی مانند نوروپاتیبسته به روشهای تشخیصی بسیار متفاوت است. بنابراین ، میزان نوروپاتی هنگام در نظر گرفتن علائم بالینی تنها 25٪ است ، و هنگام انجام یک مطالعه الکترومیوگرافی ، تقریباً در کلیه بیماران مبتلا به دیابت مشاهده می شود.
نوروپاتی دیابتی به طور قابل توجهی کیفیت زندگی بیماران را کاهش می دهد و یک عامل خطر برای ایجاد زخم های پا ، گانگرن است. بنابراین ، تشخیص به موقع و درمان پلی نوروپاتی دیابتی.
سیستم عصبی انسان از یک سیستم عصبی مرکزی ، محیطی و مستقل تشکیل شده است. سیستم عصبی مرکزی از مغز و نخاع تشکیل شده است. سیستم عصبی محیطی توسط الیاف عصبی تشکیل می شود که به قسمت های فوقانی و تحتانی ، تنه ، سر می روند. در دیابت قندی عمدتاً آسیب به سیستم عصبی محیطی رخ می دهد و به همین دلیل این عارضه را پلی نوروپاتی محیطی می نامند. بیشتر اوقات ، با پلی نوروپاتی دیابتی ، اعصاب حساس مبتلا می شوند. بیماران نگران سوزن سوزن شدن ، بی حسی ، سردی پاها یا احساس سوزش ، درد در اندام هستند. چندین سال است که این پدیده ها عمدتاً در حالت استراحت ذکر می شوند ، در خواب شبانه تداخل می کنند و متعاقباً یک شخصیت ثابت و شدید را فرض می کنند.
در حال حاضر در ابتدای ظهور این عارضه ، اغلب می توان کاهش حساسیت (درد ، لمس ، دما ، لرزش) نوع "جوراب" و "دستکش" ، تضعیف رفلکس ها و اختلالات حرکتی را مشاهده کرد. درد شدید ، سوزش ، متقارن است. اغلب درد همراه با افسردگی ، اختلال در خواب و اشتها است. این دردها برعکس درد با آسیب به رگ های محیطی فروکش می کنند.
اختلالات حساس به تدریج از پاهای دیستال به سمت پروگزیمال پخش می شود ، سپس دست ها نیز در این فرآیند درگیر می شوند. هنگامی که اعصاب محیطی در بیماران مبتلا به دیابت متاثر می شوند ، عملکرد حمل و نقل آکسون به طور عمده رنج می برد ، که توسط جریان آکسوپلاسمی حمل تعدادی ماده بیولوژیکی لازم برای عملکرد سلول های عصبی و ماهیچه ای در جهت از نورون حرکتی به عضله و بالعکس انجام می شود. آکسونوپاتی ها با پیشرفت تدریجی فرآیندهای پاتولوژیک کند می شوند. ترمیم عملکرد اعصاب محیطی با آکسونوپاتی از پیدایش های مختلف به آرامی و جزئی انجام می شود ، زیرا بخشی از آکسون ها به طور دائمی می میرد.
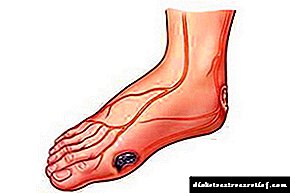
یک عارضه وحشتناک DPN زخم عصبی پا است که عمده دلایل شکل گیری آن از دست دادن حساسیت به درد و میکروتراوما پوست است.
عدم تعادل بین فلکسورها و اکستنسورهای اندام تحتانی فعالیت عضلات "کوچک" پا را کاهش می دهد که منجر به تغییر در معماری پا و ایجاد تغییر شکل پا می شود. در این حالت ، مناطقی از افزایش فشار بارگذاری در نواحی خاصی از سطح پلانتار ظاهر می شوند. فشار مداوم روی این مناطق با یک روند التهابی بافت های نرم و تشکیل زخم های پا همراه است. در مقابل زمینه کاهش حساسیت به درد و تمایل به پوکی استخوان و همچنین افزایش جریان خون که منجر به جذب استخوان در دیابت می شود ، میکروتروما می تواند منجر به شکستگی استخوان و آسیب مفاصل (پوسیدگی مفصل ، تخریب و تکه تکه شدن استخوان ها) شود. پا تغییر شکل می یابد ، راه رفتن تغییر می کند. نقض عملکرد اسکلتی عضلانی منجر به شکل گیری بیشتر نقایص زخمی می شود.
درمان طولانی مدت نوروپاتی دیابتی شامل رویکردهای بیماری زا و علامتی است. مؤثرترین داروها با اثرات بیماری زا و علامت دار شامل ویتامین های گروه B - تیامین و پیریدوکسین - در دوزهای زیاد است که باعث بهبود روند انجام تکانه های آکسون می شود.
ویتامین های گروه B در دوزهای بالا دارای اثرات متابولیکی و کلینیکی زیادی هستند ، بنابراین به طور سنتی در درمان پلی نوروپاتی دیابتی و نوروپاتی های دژنراتیو از طبیعت متفاوت استفاده می شود. تیامین (ویتامین B1) به عنوان یک کوآنزیم مجتمع دهیدروژناز چرخه Krebs ، چرخه پنتوز فسفات را تنظیم می کند ، بنابراین فرآیندهای استفاده گلوکز را کنترل می کند.
در غلظت های بالا ، تیامین قادر است فرآیندهای گلیکاسیون پاتوبیووشیمیایی پروتئین ها را کاهش دهد ، که این برای بیماران دیابتی بسیار مهم است. Thiamine با شرکت در انجام یک تکانه عصبی ، حمل و نقل آکسون ، در فرآیندهای بازسازی بافت عصبی ، مدولاسیون انتقال عصبی و عضلانی در گیرنده های n-cholinergic دارای یک اثر عصبی است.
بنفوتیامین
یک ماده لیپوفیلی منحصر به فرد با فعالیت مانند تیامین ، یک داروی بسیار مؤثر و قابل تحمل است که تقریباً 100٪ قابلیت دسترسی زیستی دارد. تیامین محلول در آب در مقادیر فیزیولوژیکی با حمل و نقل وابسته به سدیم جذب می شود. هنگامی که غلظت قابل توجهی در روده حاصل می شود ، این مکانیسم تخلیه می شود و انتشار منفعل کمتری فعال می شود. حداکثر جذب تیامین بیش از 10٪ نیست. سینتیک بنفوتیامین تفاوتهای معناداری دارد. هنگامی که در دستگاه گوارش جذب می شود ، هیچ اثر اشباع وجود ندارد. فراهمی زیستی دارو 8-10 برابر بیشتر از تیامین است ، زمان رسیدن به حداکثر غلظت 2 برابر کمتر است ، میانگین غلظت بنفوتیامین در خون بسیار طولانی تر حفظ می شود ، که به تجمع شدیدتر دارو در سلول ها کمک می کند.
این ماده سمیت کمی دارد. مطالعه سمیت بنفوتیامین در دوزهای 100 میلی گرم بر کیلوگرم وزن بدن (در موشهای صحرایی) نشان داد که تحمل خوبی برای این دارو و عدم وجود تفاوت معنی داری در مقایسه با شاهد وجود دارد. هنگام استفاده از دارو در دوزهای درمانی متوسط ، عوارض جانبی مشاهده نشده است. علائم استفاده از بنفوتیامین در ترکیب داروی Milgamma Compositum ، پلی ونوروپاتی ها به دلیل دیابت قندی و کمبود ویتامین B1 است.
پیریدوکسین (ویتامین B6)
فرم فعال فیزیولوژیکی - پیریدوکسالفسفات ، دارای کوآنزیم و اثر متابولیکی است. فسفات پیریدوکسال به عنوان کوآنزیم ، نقش مهمی در متابولیسم تعدادی از اسیدهای آمینه بویژه تریپتوفان ، اسیدهای آمینه حاوی گوگرد و اسیدهای آمینه هیدروکسی دارد و در فسفولاسیون گلیکوژن نقش دارد ، که برای بیماران دیابتی بسیار مهم است. پیریدوکسالفسفات در ترکیب واسطه ها - کاتکول آمین ها ، هیستامین ، آمینوبوتیریک اسید دخیل است ، که منجر به بهینه سازی سیستم عصبی می شود.
پیریدوکسین همچنین ذخایر منیزیم موجود در سلول را افزایش می دهد ، که یک عامل متابولیک مهم درگیر در فرآیندهای انرژی و فعالیت عصبی است ، دارای یک اثر جدا شده است و در روند خون سازی نقش دارد. جذب پیریدوکسین در دستگاه گوارش اثر اشباع ندارد و بنابراین غلظت آن در خون به محتوای روده بستگی دارد. پیریدوکسالفسفات به سرعت از دستگاه گوارش جذب می شود و از طریق کلیه ها دفع می شود. از طریق سد جفت عبور کرده و در شیر مادر دفع می شود.
کوآنزیم ویتامین B6
خاصیت متابولیکی دارد ، غلظت کلسترول و لیپیدها را کاهش می دهد ، میزان گلیکوژن موجود در کبد را افزایش می دهد ، خاصیت سم زدایی آن را بهبود می بخشد ، در متابولیسم هیستامین شرکت می کند. فرآیندهای متابولیک را در پوست و غشاهای مخاطی تحریک می کند.
پیریدوکسالفسفات معمولاً به خوبی تحمل می شود. واکنش های آلرژیک ، افزایش اسیدیته آب معده امکان پذیر است.
در درمان پلی نوروپاتی دیابتی ، یکی از بهترین داروها Milgamma Compositum است که شامل 100 میلی گرم بنفوتیامین و 100 میلی گرم پیریدوکسین است. این دارو به شکل دراژیون موجود است که راحتی بیشتری را در هنگام مصرف و عدم تعامل اجزا فراهم می کند. بنفوتامین به دلیل حلالیت در چربی ، قابلیت دسترسی فراتر از 8-10 برابر بیشتر را نسبت به نمک های تیامین محلول در آب دارد. با تجویز خوراکی ، سطح بنفوتیامین در مایع مغزی نخاعی به چنین مقادیری می رسد که فقط با تجویز تزریق نمک های محلول در آب تیامین می توان به دست آورد. بنفوتامین باعث فعال شدن آنزیم سم زدایی ترانسکتولاز می شود ، که منجر به مهار ناشی از هایپرگیکمی مکانیسم های متابولیکی مانند مسیر هگزوزامین می شود. Milgamma کامپوزیت به صورت خوراکی با دوز 150-900 میلی گرم در روز ، هم به صورت تک درمانی و هم در ترکیب با سایر داروها مصرف می شود.
علاوه بر داروی مشخص شده برای DPN ، از محلول تزریق Milgamma استفاده می شود ، حاوی دوزهای درمانی ویتامین های گروه B و یک لیدوکائین بی حسی موضعی:
- تیامین هیدروکلراید - 100 میلی گرم.
- پیریدوکسین هیدروکلراید - 100 میلی گرم.
- هیدروکلراید سیانوکوبالامین - 1000 میلی گرم.
- لیدوکائین - 20 میلی گرم.
این دارو اثر ضد درد دارد ، گردش خون را بهبود می بخشد و باعث احیای سیستم عصبی می شود. ویتامین های با دوز بالا B که در این فرآورده موجود است ، همانطور که در بالا ذکر شد ، در بیماری های التهابی و دژنراتیو اعصاب و دستگاه حرکتی تأثیر مفیدی دارد. در دوزهای زیاد ، اثر ضد درد به خوبی نشان داده می شود ، کار سیستم عصبی و روند خونریزی طبیعی می شود. توجه به این نکته ضروری است که وجود لیدوکائین و حجم کمی از محلول تزریق شده باعث می شود تزریق ها عملاً بدون درد باشد و این باعث افزایش پایبندی بیمار به درمان می شود.
Milgamma و Milgamma ترکیب کامپوزیت برای بیماری های سیستم عصبی با منشاء مختلف:
- نوروپاتی (دیابتی ، الکلی و غیره) ،
- نوریت و پلی ادراری ، از جمله نوریت مغزی ،
- پاریس محیطی (از جمله عصب صورت) ،
- نورالژی ، شامل اعصاب سه قلو و عصب بین قشر ،
در دوره نوزادی و با حساسیت شدید به دارو ، داروها را نمی توان با اشکال شدید و حاد فعالیت قلبی جبران شده مصرف کرد.
درمان نوروپاتی دیابتی مناطق زیر را شامل می شود:
- جبران دیابت قندی (تشدید درمان کاهش دهنده گلوکز).
- درمان پاتوژنتیک ساختارهای عصبی آسیب دیده (آماده سازی Milgamma به شکل تزریق و Milgamma Compositum به شکل قرص برای تجویز خوراکی یا اسیدهای لیپوئیک اسید + Milgamma Compositum).
- علائم درمانی درد.
Sachse G. و Reiners K. (2008) درمان منطقی نوروپاتی دیابتی را به شرح زیر توصیه می کنند:
مرحله سوم
درمان ترکیبی (تیوکتیک اسید + بنفوتیامین):
- تیوگامما - به صورت داخل وریدی قطره 600 میلی گرم در روز
- Milgamma Compositum - 1 قرص 3 بار در روز
- دو دارو به مدت 4-6 هفته.
بسیاری از مطالعات بالینی داخلی و خارجی اثربخشی و ایمنی Milgamma و Milgamma compositum در درمان نوروپاتی دیابتی را تأیید می کنند.
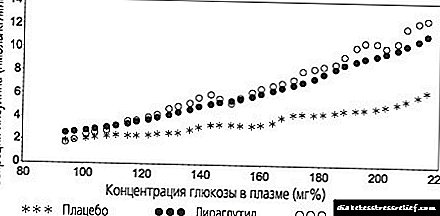
در کار ما از اولین رژیم درمانی در 20 بیمار مبتلا به نوروپاتی دیابتی (تزریق Milgamma 10 ، سپس Milgamma Compositum به مدت 6 هفته) استفاده کردیم و پویایی مثبت تصویر بالینی DPN را یادداشت کردیم که با تمایل به بهبود پارامترهای الکتروفیزیولوژیکی همراه بود و این نشانگر ترمیم عملکرد آکسون است. مطابق ادبیات ، اثر بخشی Milgamma کامپوزیت در نوروپاتی قلبی در بیماران مبتلا به دیابت گزارش شده است.
ما 20 بیمار مبتلا به دیابت نوع 2 را مشاهده کردیم ، میانگین سنی بیماران 58 سال ، مدت دیابت 9 سال و مدت زمان نوروپاتی 3 سال بود.
تمام بیمارانی که مشاهده کردیم دارای علائم نوروپاتی محیطی دیابتی با درد بودند. در 7 بیمار علائم حاد بود و در بیماران باقیمانده علائم پلینوروپاتی دیابتی متوسط بود. در حالت اول ، درمان با تزریق Milgamma 2 میلی لیتر روزانه به صورت عضلانی (10 تزریق) شروع شد ، و سپس به قرص خوراکی قرص Milgamma Compositum 1 3 بار در روز حداقل به مدت 4-6 هفته منتقل شد. در بیماران با علائم متوسط DPN ، درمان با قرص Milgamma Compositum 1 3 بار در روز به مدت 4-6 هفته انجام شد. این روش درمانی نه تنها برای بیمار و خانواده وی راحت و سنگین نیست ، بلکه ارزان تر نیز می باشد ، زیرا نیازی به بستری شدن ندارد ، که این امر هزینه درمانی را به میزان قابل توجهی کاهش می دهد. به منظور جلوگیری از عود DPN ، دوره های مکرر درمان 6-12 ماه پس از دوره اولیه در مقابل زمینه حداکثر جبران ممکن برای اختلالات متابولیک انجام شد.
در نتیجه درمان ، کاهش حساسیت به درد و پویایی مثبت از همه علائم دیگر حاصل شد. پلی نوروپاتی دیابتی در اکثریت قریب به اتفاق (در 17 مورد) بیماران. متوسط شدت درد روزانه 60-70 درصد کاهش یافته است ، و معلوم شد که اثر استفاده از Milgamma و Milgamma کامپوزیت کاملاً سریع رشد کرده است - در حال حاضر 2 هفته پس از شروع درمان. هنگام مصرف داروی مشخص شده به صورت ترکیبی (تزریق و داروی خوراکی) علائم زیر کاهش یافته است: درد سوزش ، تیراندازی و بخیه. در گروه بیمارانی که دردهای شبانه در آنها مشاهده شده است ، کاهش شدت آنها مشاهده شده است. دردهای شبانه عمدتاً دلیل کاهش کیفیت زندگی بیماران است ، بنابراین ، پس از درمان ، بیماران به دلیل کاهش در روز و به خصوص دردهای شبانه ، بهبود کیفیت زندگی را تجربه می کنند. تأثیر دارو Milgamma Compositum در طول دوره درمان افزایش یافته است ، که 4-6 هفته به طول انجامید.
این مطالعه نشان داد Milgamma تحمل و ایمنی خوبی دارد. عوارض جانبی در ابتدای دارو و عمدتاً به صورت تهوع ، سرگیجه مشاهده شد. این اثرات از نظر طبیعت خفیف یا متوسط بوده و تمایل به تضعیف یا به طور کامل ناپدید شدن پس از 10 روز از مصرف دارو دارد.
بنابراین ، پلی نوروپاتی در دیابت قندی پیچیده است و عمدتا به دلیل اختلالات در سیستم عصبی محیطی است. پیشرفت در مطالعه پاتوژنز امکانات جدیدی را برای جستجوی داروهایی ایجاد می کند که مستقیماً بر مکانیسم های پاتوفیزیولوژیک DPN تأثیر می گذارند ، که شامل Milgamma و Milgamma کامپوزیت است ، با یک اثر پیچیده منجر به بهبود خونرسانی ، تحریک بازسازی بافت عصبی ، افزایش سرعت تکانه عصبی و داشتن اثر ضد درد .این دارو جایگاه مهمی در درمان پیچیده نوروپاتی دیابتی دارد.