لوزالمعده: بافت شناسی ، نقش در بدن
معماری لوزالمعده. لوزالمعده در ساختار آن به رده غدد آلوئول پیچیده تعلق دارد. لوبول های لوزالمعده توسط لایه هایی از بافت همبند سست از هم جدا می شوند که از طریق آن خون و رگ های لنفاوی ، اعصاب و مجاری دفع کننده عبور می کند. در این لایه ها سلول های چربی وجود دارد ، که گاه تعدادشان زیاد است. لوزالمعده با یک کپسول نازک بافت همبند پوشانده شده است.
مجرای اصلی ترشح کننده ، که بارها شاخه می شود ، به مجاری کوچک دفع بین لوبولار شکسته می شود. مجرای بزرگ دفع کننده که در جنین به عنوان بیرون ریز مخاط مخاطی روده ایجاد می شود ، مانند این لوله ، با یک اپیتلیوم استوانه ای تک لایه بالا روکش شده است ، که در آن سلول های مخاطی به شکل اجنه پراکنده می شوند. در جاهایی ، نتایج حاصل از این پوشش اپیتلیال باعث ایجاد غدد مخاطی کوچک یا کپورها می شود که در مجرای اصلی دفع کننده در نزدیکی محل خروج آن به داخل اثنی عشر اتفاق می افتد. در خارج ، مجرای ترشحی اصلی توسط لایه ای از بافت پیوندی متراکم سرشار از الیاف کلنیک و الاستیک احاطه شده است ، که به آن چگالی کافی می بخشد ، به لطف آن ، با اشغال یک موقعیت محوری در لوزالمعده ، تا حدی نقش میله ای را که از لکه بینی لطیف این ارگان پشتیبانی می کند ، ایفا می کند.
مجرای ترشح کننده اصلی شاخه های جانبی جانبی (مجاری بین لوبولار) را که از لایه های بافت پیوندی ضخیم تر عبور می کند ، عبور می دهد و مانند مجرای اصلی با اپیتلیوم استوانه ای روبرو می شود. مجاری بین لوبولی به شاخه داخل مغز (کالیبر کوچک) شاخه می شوند که اپیتلیوم آن قبلاً مکعب است. مجرای کوتاه داخل شکمی سرانجام به بخش های بین میانی منتقل می شوند ، که مستقیماً با جلوی اسیلین ختم می شوند. بخش های درج توسط اپیتلیوم سنگفرشی تشکیل می شوند.
میکروسکوپ الکترونی نشان می دهد که سطح آپیکال سلولهای اپیتلیال مجاری کوچک دفع کننده ، روبروی لومن آنها ، در میکروویلی از اشکال و اندازه های مختلف کشیده شده است. سیتوپلاسم این سلولها بصورت الکترونیکی سبک ، کمی ساختار یافته است. Ergasto-plasma ضعیف بیان شده و توسط واکوئل ها و گلوله های کوچک Pelida نشان داده می شود. میتوکندری ها به شکل کمی ، گرد یا بیضی شکل هستند. در مکان هایی که در سیتوپلاسم وجود دارد ، تعداد وکیل بزرگ و بزرگتری وجود دارد. هر لوبول از چندین acini تشکیل شده است ، که محکم به یکدیگر فشار می یابند و فقط توسط لایه های کمی از بافت شبکیه جدا می شوند ، که در امتداد آن یک شبکه مویرگی شاخه های acini را بافته می کند. acini دارای شکل کروی ، بیضی شکل یا کمی کشیده است و از یک لایه سلولهای اپیتلیال غده تشکیل شده است ، به شکل حلقه ای که روی یک غشای پایه نازک قرار دارد. اتصال acini با بخش های درج ، که آغاز مجرای های دفع کننده است ، می تواند به روش های مختلفی رخ دهد. گاهی اوقات قسمت درج در انتهای آن مستقیماً به داخل سینوس منبسط می شود ، اما در بیشتر موارد ، انتهای دیستال بخش درج به داخل حفره سینوس رانده می شود. در چنین مواردی سلولهای اپیتلیال کوچکی در وسط اسکینوس یافت می شوند که در قسمت بالای سلولهای استین قرار دارند اما متعلق به بخش درج هستند. این سلولهای کوچک به نام سانتریاژین شناخته می شوند ؛ آنها یکی از مشخصه های ساختاری پانکراس را نشان می دهند. سرانجام ، مواردی وجود دارد که پوست سر در مجاورت لبه جانبی مجرای ترشح کننده قرار دارد و سپس سطح مقطع این تصور را می دهد که لومن acinus از یک طرف توسط سلولهای acinar و از طرف دیگر سلولهای مجرای دفع کننده (گریز از مرکز) محدود است.
جزایر لانگرهان در پارانشیم لوزالمعده به شکل خوشه های سلولی ایستاده اند ، که به دلیل رنگ پررنگ آنها از ناحیه acini اطراف به شدت متفاوت است. اندازه جزایر بسیار متفاوت است. بعضی اوقات جزایر فقط از چند سلول تشکیل شده است ، اما ، به عنوان یک قاعده ، آنها تشکیل دهنده های بزرگی را تشکیل می دهند ، اغلب به قطر 175 متر یا بیشتر از آن می رسند و در هر صورت ، به طور قابل توجهی از اندازه acini اطراف آن فراتر می روند. شکل جزایر کم و بیش گرد (کروی) است ، اما اغلب آنها طرح های زاویه ای نامنظم یا برآمدگی ها و تورفتگی های سطح آنها دارند.
این جزایر می توانند به دلیل توانایی درک برخی از لکه های فوق حاد انتخابی تر از بقیه لوزالمعده پانکراس شناخته شوند. اگر یک لوزالمعده تازه را از طریق شریانهای آن با یک محلول ضعیف از جنس خنثی قرمز یا سبز خنثی می کنید ، در برابر زمینه کلی یک پارانشیم رنگ پریده ، جزایر لانگرهانس با رنگ قرمز تیره تر یا آبی-سبز تیزتر ایستادگی می کنند. تعداد جزایر لانگرهانس بسیار متغیر است ، زیرا آنها به راحتی دوباره ، حتی در یک ارگانیسم بالغ تشکیل می شوند. با این حال ، آنها به وضوح در دم لوزالمعده غالب هستند. تعداد جزایر موجود در لوزالمعده انسان از 208000 تا 1760،000 متغیر است. تغییرات مربوط به سن در جزایر به دلیل تغییرپذیری شدید آنها نمی تواند با دقت کافی ایجاد شود. ظاهراً با افزایش سن ، تعداد نسبی آنها به تدریج افزایش می یابد و پس از 25 سال شروع به کاهش تدریجی می کند. کپسول تزئین شده در اطراف جزایر وجود ندارد ، و آنها فقط از طریق یک غشای رتیکول ظریف از پارانشیم آکینار اطراف جدا می شوند.
سلولهای غده ای از جزایرها خوشه های جمع و جور یا تارهای شاخه ای از اشکال نامنظم هستند. این بندها توسط لایه های بافت همبند جدا می شوند ، که در آن مویرگ های گسترده - سینوئیدها - عبور می کنند. استرومای جزیره از الیاف شبکیه در ارتباط با این لایه ها تشکیل شده است.
سرانجام ، در پارانشیم لوزالمعده ، لوله های کور کوچک با قطر 12-25 سانتیمتر وجود دارد که بین خود آنها را تحریک می کند. این لولهها توسط یک اپیتلیوم تک لایه با سلولهای مکعب کوچک تشکیل شده است که در بین آنها ، گاهی سلولهای جامد و سلولهایی که دارای گرانولهای مخاطی در سیتوپلاسم هستند ، یافت می شوند. لوله ها گاهی اوقات در جزایر لانگرهان ، بویژه بزرگ ، پایان می یابند ، در انتهای دیگر آنها می توانند با مجاری ارتباط داشته باشند. ظاهراً توبولها بقایای رشته های اپیتلیال هستند که باعث ایجاد جزایر لانگرهان در جنین زایی ، بدون تمایز باقی مانده و در ارگانیسم بالغ آنها از هر نظر احتمالاً منشأ شکل گیری جزایر جدید و احتمالاً acini هستند.
Acini و چرخه ترشحی آنها. سلولهای Acinar (اگزوکرین) شکل کمابیش مخروطی دارند و با انتهای آپیکال لومن اسکینوس روبرو می شوند. لومن اگزینوس که در دوره استراحت عملکردی ، لوزالمعده کوچک است ، در مراحل ترشح فعال افزایش می یابد ، که توسط ترشح مایع ترشح شده از سلول ها کشیده می شود. قسمتهای بالای سلولهای آکینار با یک غشای آپیکال نازک پوشیده شده است ، و مویرگهای ترشحی که گاهی اوقات به داخل لومن استین باز می شوند ، گاهی اوقات بین سطوح جانبی سلولهای تماسی قابل مشاهده است. هسته به پایه سلول acinar نزدیکتر است. قسمت آپیکال (فوق هسته ای) سیتوپلاسم پر از دانه های ترشح (زیموژن) است که مقدار آن در مرحله دفع کمی است ، اما در مرحله استراحت عملکردی ، گرانول ها بطور متراکم کل قسمت بالای سلول آکینار را پر می کنند. در همان منطقه فوق هسته ای ، با پردازش بافت شناسی مناسب ، یک شبکه Golgi حجیم و با شکاف انشعاب آشکار می شود ، در تماس نزدیک با شاخه هایی که گرانولهای بلوغ راز پنهان شده اند.
قسمت پایه سلول acinar به دلیل همگن بودن آن با اپیکال به شدت متفاوت است. این ماده بر خلاف گرانولهای اسیدوفیلیک قسمت آپیکال به شدت با رنگهای پایه رنگ آمیزی می شود. بازوفیلی قسمت پایین به دلیل تجمع فراوان اسید ribosonucleic (ribosonucleoproteins) است که بدیهی است با سنتز پروتئین فشرده همراه است و منجر به تشکیل گرانولهای ترشحی می شود. میتوکندری ها ، معمولاً طولانی و نازک ، اغلب چین دار یا پیچ خورده ، همچنین در قسمت های پایه سلول های اسکارین قرار دارند.
هسته های بزرگ گرد سلولهای آکینار حاوی نسبتاً زیادی کروماتین و 1-2 هسته ای اکسیفیلیک هستند. میتوز در سلولهای اسکارین بسیار نادر است.
سلولهای Acinar یک ارگاستوپلاسم به خوبی توسعه یافته دارند. استفاده از میکروسکوپ الکترونی نشان می دهد که کل سیتوپلاسم سلول acinar توسط غشاهای وزیکول مسطح متعدد مسطح تشکیل شده است که تقریبا سلول را به طور کامل پر می کنند ، به استثنای ناحیه کوچک گلژی ابرقابل هسته ای. سطح بیرونی a-cytomembranes با تعداد زیادی هسته هسته ریبوز (گرانول Pelida) نشسته است ، وفور آن تعیین کننده بازوفیلی مشخصه یک سلول acinar است. دانه های ریبوزونوکلئیک نیز در امتداد سیتوپلاسم بین غشاها پراکنده اند. غشاهای حبابی شکل ارگاستوپلاسم به طور موازی در اطراف هسته یک سلول acinar لایه بندی می شوند. در بخش مقطع ، ارگاستوپلاسما ظاهر زنجیره ها ، شکاف ها و حباب های کوچک را دارد که گاه تا حدودی گسترش می یابد. فراوانی گرانول های روبوسونوکلئین باعث می شود که به طور فشرده سنتز محصولات پروتئینی انجام شود و منجر به تشکیل گرانول های زیموژن ترشحی شود که در قسمت بالای سلول acinar جمع می شوند.
راز فقط در هنگام هضم ترشح می شود ، بنابراین قسمتهای بالای سلولهای acinar از لوزالمعده در حیوانات گرسنه با گرانولهای زیموژن پر می شوند. در ميان هضم ، انحلال بسيار سريع دانه هاي ترشحي اتفاق مي افتد و ترشح آنها در لومن پوست و حتي داخل سيستم مجاري هاي ترشحي لوزالمعده مي شود.
در سلول آكینار لوزالمعده ، كه ترشح ماهیت پروتئینی ایجاد می كند ، بستر فرآیندهای بیوسنتز فشرده ، صفحات ارگاستوپلاسما بسیار پیشرفته و بخصوص گرانول های ریبوسوكلیك فراوان است كه هر دو روی این آسم مایع ها نشسته و بین آنها پراكنده شده اند.
با استفاده از روش راز آماده سازی ، قسمت اگزوکرین لوزالمعده متعلق به غدد معمولی موروکرین است که راز آن به صورت حل شده توسط انتشار از طریق غشای آپیکال ترشح می شود و باعث حفظ صداقت آن می شود. برای جدا کردن راز ، تحریک عصبی یا هورمونی خاصی لازم است ، بنابراین راز لوزالمعده فقط در ارتباط با مصرف مواد غذایی به روده ترشح می شود. در نتیجه ، دوره های فعال شدن لوزالمعده (یعنی دوره های ترشح شدید) به طور متناوب با مدت زمان کم و بیش استراحت عملکردی ، هنگامی که محصولات ترشحی در سلولهای acinar سنتز می شوند ، گرانولهای آن در قسمتهای بالای این سلولها جمع می شوند. بنابراین ، ترشح میوکرین لوزالمعده دارای ویژگی ترشح متناوب یا پراکنده است.
همانطور که در بالا ذکر شد ، جزایر لوزالمعده از نظر اندازه و فرکانس توزیع آنها در پارانشیم بسیار متفاوت است. معمولاً آنها شکلی کم و بیش گرد دارند و با چیدمان نسبتاً جمع و جور سلول ها به شکل رشته های نادرست شاخه دار مشخص می شوند. سلولهای جزایر خاص توسط دو گونه اصلی نشان داده می شوند. بیشتر سلولهای جزایر حاوی گرانولهای کوچک ، محلول در الکل هستند ، اما در محلولهای آبی نگهدارنده هستند. برعکس ، گرانول سلولهای دیگر در آب حل می شوند ، اما توسط فیکساتورهای الکل حفظ می شوند. سلولهای گروه اول سلولهای B (سلولهای P) نامیده می شوند ، در حالیکه سلولهای نوع دوم با گرانولهای مقاوم در برابر آلکانول به عنوان سلولهای A (سلولهای a) تعیین می شوند. به عنوان یکی از روشهای متداول برای تمایز سلول های جزایر ، معمولاً از کرومات Gomori هماتوکسلین و رنگ آمیزی فلوکسین استفاده می شود (O.Soshop ، 1941). علاوه بر این ، گرانولهای سلولهای A ، آرگیروفیلیای مشخصی را آشکار می کنند ، به طور انتخابی با نقره آمونیاک سیاه می شوند.
توزیع سلولهای A و B بر روی جزایر ممکن است متفاوت باشد. سلولهای B در بندهای فشرده قرار دارند و در تماس مستقیم با مویرگها قرار دارند. این سلول ها شکل کمابیش منشوری دارند و از نزدیک در همدیگر قرار دارند. هسته آنها گرد یا کمی بیضی شکل است و نسبتاً غنی از کروماتین هستند. سلولهای A گرد یا زاویه دار ، اندازه بزرگتر از سلولهای B ، در بعضی موارد در خوشه های نامنظم در حاشیه جزایر (در جوندگان) قرار دارند ، در برخی دیگر در سراسر جزایر پراکنده می شوند و در گروه های کوچک در مرکز جزایر (در انسان ، شکارچیان) جمع می شوند. ) هسته سلولهای A از جنس وزیکولار ، بزرگ ، رنگ آمیزی سبک ، دارای یک هسته بزرگ اکسیفیلیک است.
علاوه بر سلولهای A- و B ، که بخش عمده ای از جزیره را تشکیل می دهند ، تعداد کمی نیز شامل سلولهای فاقد گرانول (سلولهای به اصطلاح C) هستند. در کنار آنها ، بعضی اوقات سلولهای نوع B شناسایی می شوند که در هنگام استفاده از رنگ آمیزی با توجه به مالوری یا به روش آزان ، از رنگ آبی کمرنگ دانه ها متمایز می شوند ، از اهمیت عملکرد سلولهای C و B ناشناخته است. این امکان وجود دارد که سلولهای C نشانگر ذخیره ، مراحل کمی متفاوت از رشد سلولهای B باشد و سلولها با توجه به سلولهای A مقدار مشابهی نسبت داده شوند ، زیرا ، مانند دومی ، آنها برخی از argyrophilia سیتوپلاسمی را نشان می دهند.
سلولهای جزایر در ساختار سازندهای ارگونوپلاسمی آنها به شدت از سلولهای acinar متفاوت است. در حالی که سلولهای acinar با توسعه فراوان از acitomembranes مشخص می شوند ، که بطور متراکم کل سیتوپلاسم را در ردیف های موازی پر می کنند ، در سلولهای جزایر ارگاستوپلاسما ("رتیکولوم آندوپلاسمی") توسط وزیکولهای نسبتاً کوچکی نشان داده می شوند که ترتیب قابل توجهی ندارند و در قسمت بیرونی با دانه های ریبوزونوکلئیک قرار دارند. علاوه بر این ، در سلول های B ، چنین عناصر ارگاستوپلاسم تا حدودی قوی تر توسعه می یابد ، گاهی اوقات گروه بندی موازی اتی تاممبران ها حتی در مناطق جداگانه سیتوپلاسم مشاهده می شود. سلولهای A ارگاستوپلاسما A کمیاب تر هستند ، و وزیکول های آن ، به طور نامنظم و با اندازه های مختلف ، پراکنده پراکنده هستند.
گرانولهای خاص سلولهای B و A از نظر الکترونیکی بسیار مشابه هستند. آنها در داخل وزیکول های ارگاستوپلاسم قرار دارند و توسط غشاهای آن احاطه شده اند.
کندروموزوم ها در سلول های جزایر ، بر خلاف ویژگی میتوکندری رشته ای طولانی سلول های آکینار ، دارای شکل میله های کوتاه ، اغلب به شکل نامنظم بوده و از چگالی الکترونی-نوری نسبتاً بالایی برخوردار هستند. سلولهای جزایر جزایر جزایر به سلولهای مجاری سلولهای مجرا نزدیک می شوند. در سلولهای B ، کندریوزومها بیشتر از سلولهای A هستند. شبکه Golgi در سلولهای جزایر کمتر از سلولهای acinar توسعه یافته است. این است که به طور عمده توسط یک سیستم از خلاء بزرگ نشان داده شده است ، در حالی که صفحات دوتایی (y-cytomasmbranes) ضعیف بیان شده است. شبکه Golgi در آن قسمت از سلول جزیره ای قرار دارد که رو به مویرگی است. گاهی اوقات ، در سلولهای A با لکه های معمولی ، ساختار حلقوی (ماکولا) یافت می شود که نشان دهنده تصویری منفی از شبکه Golgi است.
در دیواره مویرگها که در جزایر انشعاب می شوند ، میکروسکوپ الکترونی منافذ عجیب و غریب را نشان می دهد که به لایه اندوتلیال نفوذ می کند و با یک غشای نازک پوشیده شده است. بین سلولهای جزیره مویرگی و مجاور ، یک فضای شکاف آزاد باریک مانند باقی مانده است.
اهمیت فیزیولوژیکی سلولهای B و A. در حال حاضر از این واقعیت است که انسولین را می توان از لوزالمعده با الکل اسید شده استخراج کرد ، و گرانول های سلول B بصورت انتخابی در الکل حل می شوند ، می توان نتیجه گرفت که این سلول ها انسولین تولید می کنند.با بار طولانی مدت حیوان مورد آزمایش با گلوکز ، افزایش نیاز به انسولین در اولین لحظه با آزاد شدن سریع دانه ها از سلول های B و سپس هیپرتروفی و هایپرپلازی آنها وقتی دوباره پر از دانه های خاص می شوند ، بروز می یابد. سرانجام ، شواهد قاطع ناشی از استفاده از آلوکسان است. این ماده فقط باعث ایجاد نکروز انتخابی سلولهای B می شود (سلولهای A نرمال باقی می مانند) و همزمان همزمان هیپوگلیسمی کوتاه مدت اتفاق می افتد (با توجه به این واقعیت که کل عرضه انسولین موجود در آنها بلافاصله از سلولهای B نابود شده رها می شود) و پس از آن هایپرگلیسمی مداوم و گلیکوزوری. برعکس ، تحت عمل مواد کاهش دهنده قند مصنوعی گروه سولفانیل آمید (B 255 ، نادیسان ، اکستون) ، هیپرتروفی جزایر و هایپرپلازی مشاهده می شود که همراه با تورم سلول های B ، افزایش تعداد میتوز در آنها و آزاد سازی گرانول های آنها است که نشان دهنده افزایش فعالیت ترشحی آنها است. فقط با استفاده طولانی مدت از این داروهای ضد دیابتی می توان تخلیه سلولهای B را ایجاد کرد و منجر به تخریب آبگریز آنها شد. بنابراین ، اهمیت سلولهای B به عنوان تولیدکننده انسولین با اطمینان کامل مشخص شده است.
لوزالمعده گاو حاوی حدود 150 میلی گرم بر کیلوگرم انسولین است. طبق گفته های بارنت و کارمندان وی ، تولید کل انسولین در انسان به حدود 2 میلی گرم در روز می رسد.
مشخص شد برای احیای سطح طبیعی قند خون در حیوانات در معرض آلوکسان ، مقادیر بیشتری انسولین نسبت به عادی سازی منحنی قند در یک حیوان فرسوده نیاز است. از این رو نتیجه می گیرد که در لوزالمعده ، که سلول های B را از دست داده است ، ماده خاصی تولید می شود که اثرات قند خون ، یعنی اعمال می کند. عمل مخالف انسولین. محصول مورد نظر ("عامل گلیکوژنولیتیک قند خون" یا "NOG") توسط مرلین از لوزالمعده جدا شد و نام گلوکاگون را دریافت کرد. آماده سازی گلوکاگون قند خون را افزایش می دهد.
درست همانطور که سلولهای B به طور انتخابی تحت تأثیر آلوکسان قرار می گیرند ، سلولهای A نیز حساسیت مشابهی به کبالت و خصوصاً نمکهای کادمیوم دارند که باعث آزاد شدن دانه های تجمع شده ترشح از این سلولها می شود. در این حالت ، کاهش قند خون تشخیص داده می شود. تجویز طولانی مدت سولفات کادمیوم با افزایش تعداد سلولهای A و قند خون همراه است. این داده ها نشانگر اتصال سلول های A با تشکیل گلوکاگون است. از طرف دیگر ، تزریق گلوکاگون اگزوژن منجر به آتروفی انتخابی سلولهای A در حالی که سلولهای B را سالم نگه می دارد ، که نتیجه گیری در مورد فعالیت تشکیل دهنده گلوکوکاگون سلولهای A را تأیید می کند.
بنابراین ، جزایر Langerhans در تنظیم متابولیسم کربوهیدرات ها شرکت می کنند ، و تولید دو هورمون - انسولین گلوکاگون - با یک اثر ضد خصمانه. هریک از این هورمون ها توسط سلول های تخصصی خاص تولید می شوند. بنابراین ، نسبت کمی بین سلولهای A و B باید برای تنظیم قند خون ضروری باشد. به طور معمول ، در بزرگسالان ، این نسبت تا حدودی متفاوت است ، اما به طور متوسط در حدود 1: 3.5-1: 4 باقی می ماند. بنابراین ، سلول B به طور قابل توجهی از نظر کمی غالب است. در جنین زایی ، در بعضی از حیوانات ، سلولهای A برای اولین بار از هم متمایز می شوند ، در بعضی دیگر سلولهای B ابتدا در جنین ها و نوزادان ظاهر می شوند. اعداد
لوزالمعده: ساختار و نقش آن در بدن
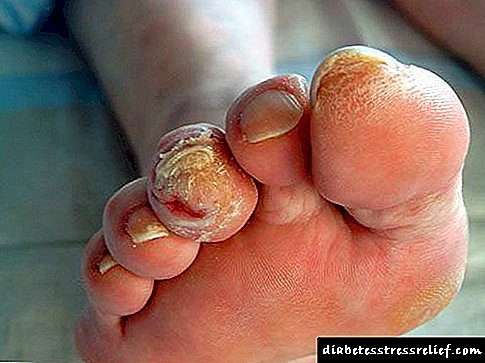
همه می دانند که چنین غده ای به نام لوزالمعده وجود دارد. به محض شروع به انجام نادرست نقش خود ، فرد دچار بیماری هایی مانند پانکراتیت ، احتمالاً حتی دیابت می شود.
علیرغم این واقعیت که اینها بیماریهای کاملاً متفاوتی هستند و علل بروز آنها نیز ممکن است متفاوت باشد ، اما همه چیز حول لوزالمعده می چرخد. به دلیل ساختار خاص و نقش دوگانه در بدن ، قادر است به موقع غذا را هضم کرده و انسولین را در خون آزاد کند.
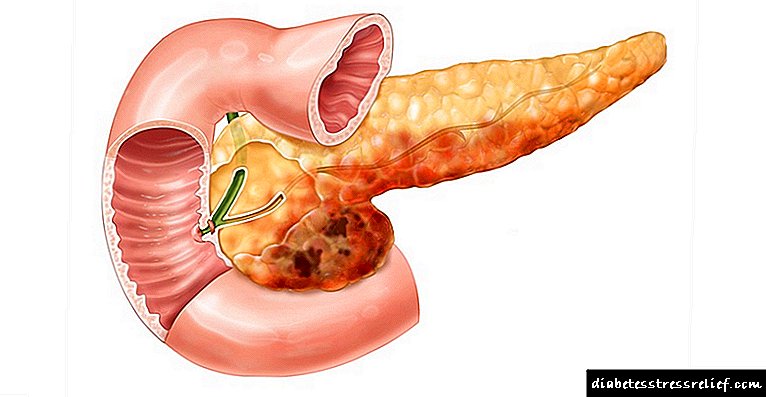
لوزالمعده به طور قابل اعتماد در حفره شکمی قرار دارد و بین خود معده و روده کوچک قرار دارد. این وزن به میزان قابل توجهی کم ، تنها 80 گرم است ، اما نقش بسیار مهمی در بدن دارد.
اول از همه ، این یک غده مخلوط است - غدد درون ریز و برونگرای بدن ، و در هنگام هضم غذا آنزیم ها و هورمون های لازم را برای انسان تولید می کند. بنابراین ، در بدن برای انجام نقش زیر عمل می کند:
- در طی فرآیند هضم غذا ، لوزالمعده آنزیم هایی را تولید می کند ، که سپس برای پردازش بیشتر وارد اثنی عشر 12 می شوند.
- عملکرد طبیعی لوزالمعده به مقدار کافی انسولین و گلوکاگون به بدن می بخشد.
همانطور که قبلاً نیز اشاره شد ، این بخش از سیستم جامع بدن از دو بخش ساختار و کارکرد کاملاً متفاوت - Endo - و Exocrine تشکیل شده است. هر کدام نقش مهم خود را انجام می دهند.
- غدد درون ریز - عملکرد ترشحی را در داخل انجام می دهد.
- اگزوکرین یک عملکرد ترشحی خارجی است.
از نظر خارجی ، عملکرد ترشح در تولید آب لوزالمعده است. و حاوی چنین آنزیم هایی است - نوکلئاز ، آمیلاز ، لیپاز ، استاپسین ، پروتئیناز. با کمک این آنزیم ها ، تمام مواد غذایی به معده می روند ، در ذرات کوچک تجزیه می شوند. هر یک از این آنزیم ها همچنین مسئول برخی ترکیبات ، چربی ها هستند و به شما امکان می دهد همه چیز را به خوبی پردازش کنید.
در نتیجه تمام مراحل موجود در دستگاه گوارش ، آب لوزالمعده تولید می شود. عواملی مانند نوع غذا ، بوی آن ، روند جویدن و بلع قادر به ترشح آن هستند. در یک کلام ، تخصیص آب لوزالمعده به طور مستقیم به میزان مصرف غذا بستگی دارد.
و همچنین هورمونهای غده تیروئید ، غدد فوق کلیوی و مغز می توانند بر دفع آنزیمهای لوزالمعده تأثیر بگذارند. اگر در این زنجیره تغییراتی یا تخلفاتی رخ داده باشد ، این بلافاصله این کار روی کار لوزالمعده تأثیر می گذارد.
عملکرد غدد درون ریز یا همانطور که از آن به عنوان "جزایر لانگرهانس" نیز یاد می شود ، هورمونهای لازم را به بدن می دهد - انسولین ، سماتوستاتین ، پلی پپتید. انسولین توسط سلولهای گلوکز جذب می شود. این روند بر روی عضله و بافت چربی تأثیر می گذارد. این هورمون قادر به تبدیل گلوکز به گلیکوژن است که در سلول های کبدی و ماهیچه ها ذخیره می شود.
بدن در صورت لزوم مقدار گلیکوژن مناسب را مصرف می کند. اگر تولید انسولین در مقادیر کافی رخ دهد ، دیابت قند ایجاد می شود. علاوه بر این ، با عملکرد ضعیف لوزالمعده ، بیماری های دیگری ایجاد می شود.
علل بیماری لوزالمعده
اگر معده مان شروع به صدمه کند ، ما طبیعتاً این موضوع را با تغذیه ضعیف ، استراحت ، استرس مداوم مرتبط می کنیم. همچنین شایان ذکر است تعدادی از فاکتورهای دیگر که می توانند به دستگاه گوارش آسیب وارد کرده و باعث بیماری لوزالمعده شوند:
- استفاده بیش از حد از الکل و دخانیات.
- بیماری سنگ کیسه صفرا.
- داروها ، یک دوره طولانی از درمان.
- پانکراس ارثی.
- بیماری های عفونی - هپاتیت اشکال مختلف ، اوریون.
- سرطان لوزالمعده.
اخیراً ذکر شده است که موارد بیماری لوزالمعده به دلیل ویروس ها و باکتری ها شایع تر شده است. نفوذ این عناصر به لوزالمعده بسیار خطرناک است ، زیرا آنها کانونی را در لوزالمعده تشکیل می دهند ، که سپس در سراسر بدن پخش می شود.
حمله حاد درد می تواند به طور ناگهانی اتفاق بیفتد و عملاً فرد را با تعجب درآورد. و می تواند در هر جایی اتفاق بیفتد. علاوه بر این ، هر علتی که باعث ایجاد بیماری شود با درد حاد همراه است و با هر دقیقه غیر قابل تحمل می شود.
در این مرحله ، فراخوانی یک تیم آمبولانس فوری است ، زیرا داروهای خانگی به تسکین درد کمک نمی کنند. اعتیاد به الکل ، سیگار کشیدن می تواند باعث حمله پانکراس شود. تغذیه مناسب ، پیاده روی در هوای تازه ، تمرینات بدنی ، می تواند تأثیر مثبتی در کار لوزالمعده داشته باشد.
تجزیه و تحلیل برای بافت شناسی لوزالمعده: برای چه کسانی تجویز شده است که بررسی می کنند
بافت شناسی ساختار سلول های بدن را بررسی می کند و این مطالعه می تواند وجود سلول ها و تومورهای خطرناک را تعیین کند.
این روش از تحقیقات پانکراس اجازه می دهد تا تغییرات پاتولوژیک با دقت بالایی تعیین شود. خیلی اوقات متخصصان زنان از این روش تحقیق در بدن برای تشخیص سرطان دهانه رحم استفاده می کنند.
برای مطالعه لوزالمعده نیز از آنالیز بافت شناسی استفاده شد. از آنجا که این نتیجه صد در صد است. چه کسی این تحلیل را به شما اختصاص داده است؟ برای بیمارانی که مشکوک به انکولوژی لوزالمعده هستند ، می توان یک جواب داد.
با وجود این واقعیت که این بیماری از تومورهای بدخیم معده کمتر دیده می شود ، اما متأسفانه بیشتر از آنکولوژی ریه ها و کبد شایع است. همه ساله شیوع سرطان لوزالمعده حدود دو درصد افزایش می یابد. علائم زیر ممکن است نتیجه توسعه انکولوژی لوزالمعده باشد:
- پانکراتیت مزمن
- محصولات با کیفیت ضعیف و مواد افزودنی مصنوعی.
- سوء مصرف الکل.
بافت شناسی امکان تشخیص زودرس وجود تومور پاتولوژیک و کمک به موقع به بیمار را می دهد. همه افراد می دانند که از ابتلا به این بیماری آسان تر از درمان در آینده است. مراقب سلامتی خود باشید ، درست بخورید ، از الکل و ورزش استفاده نکنید. یک سبک زندگی سالم به شما امکان می دهد زندگی کامل و جالبی را بدون درد ، بیماری و عوارض مرتبط با آنها بگذرانید.
آناتومی و عملکرد غده
لوزالمعده از بافت همبند تشکیل شده و در یک کپسول متراکم قرار دارد. این مویرگ های زیادی برای تامین خون مناسب لازم است ، بنابراین آسیب آن می تواند منجر به خونریزی خطرناک داخلی شود.
لوزالمعده در حفره رتروپریونئال بدن انسان قرار دارد. در جلوی او شکم قرار دارد ، که با یک کیسه سبزی جدا شده است ، در پشت - ستون فقرات. گره های لنفاوی ، پلکسوس سلیاک و آئورت شکمی در قسمت پشتی غده بومی سازی می شوند. با این ترتیب ارگان ، بار روی آن بهینه توزیع می شود.
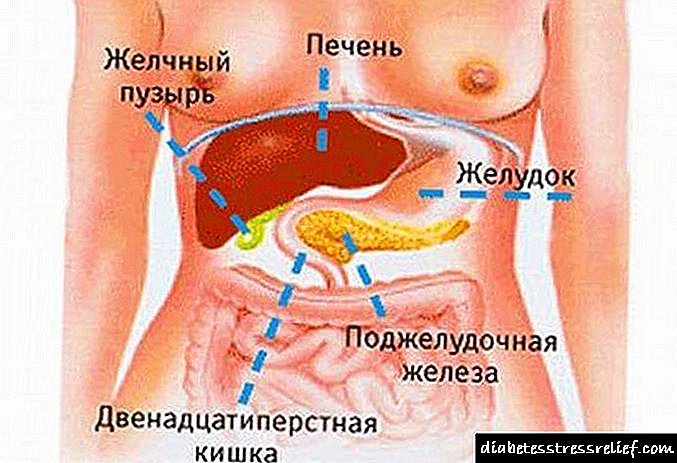
شکل اندام دراز است و از نظر بیرونی شبیه کاما است. به طور مشروط به قسمتهایی تقسیم می شود:
- سر (تا 35 میلی متر طول) - در نزدیکی اثنی عشر قرار دارد و محکم آن را محکم می کند.
- بدن (حداکثر 25 میلی متر) در منطقه اولین مهره کمر بومی سازی می شود.
- دم (حداکثر 30 میلی متر).
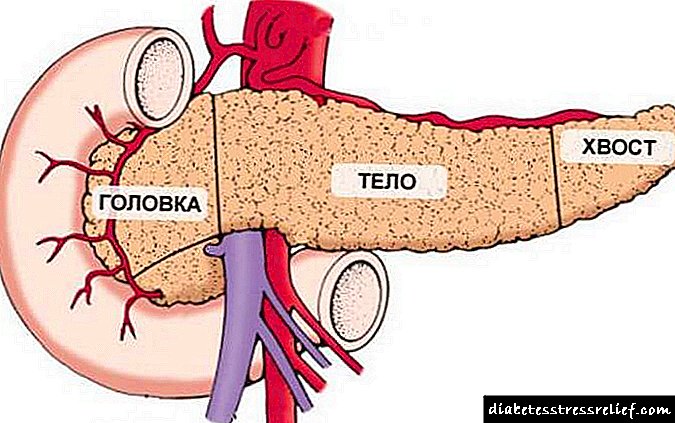
بنابراین ، طول عضو خود یک بزرگسال ، به طور معمول ، بیش از 230 میلی متر نیست.
آناتومی یک اندام پیچیده است. لوزالمعده یکی از اندام های سیستم غدد درون ریز است. بافتهای آن با توجه به نوع ساختار و ساختار به دو نوع اگزوکرین و غدد درون ریز تقسیم می شوند.
قسمت بیرونی غده آنزیم های مورد نیاز برای هضم در اثنی عشر را تشکیل داده و ترشح می کند. آنها به هضم اجزای اصلی مواد غذایی در مواد غذایی کمک می کنند. قسمت غدد درون ریز باعث تولید هورمون ها و متابولیزه شدن می شود.
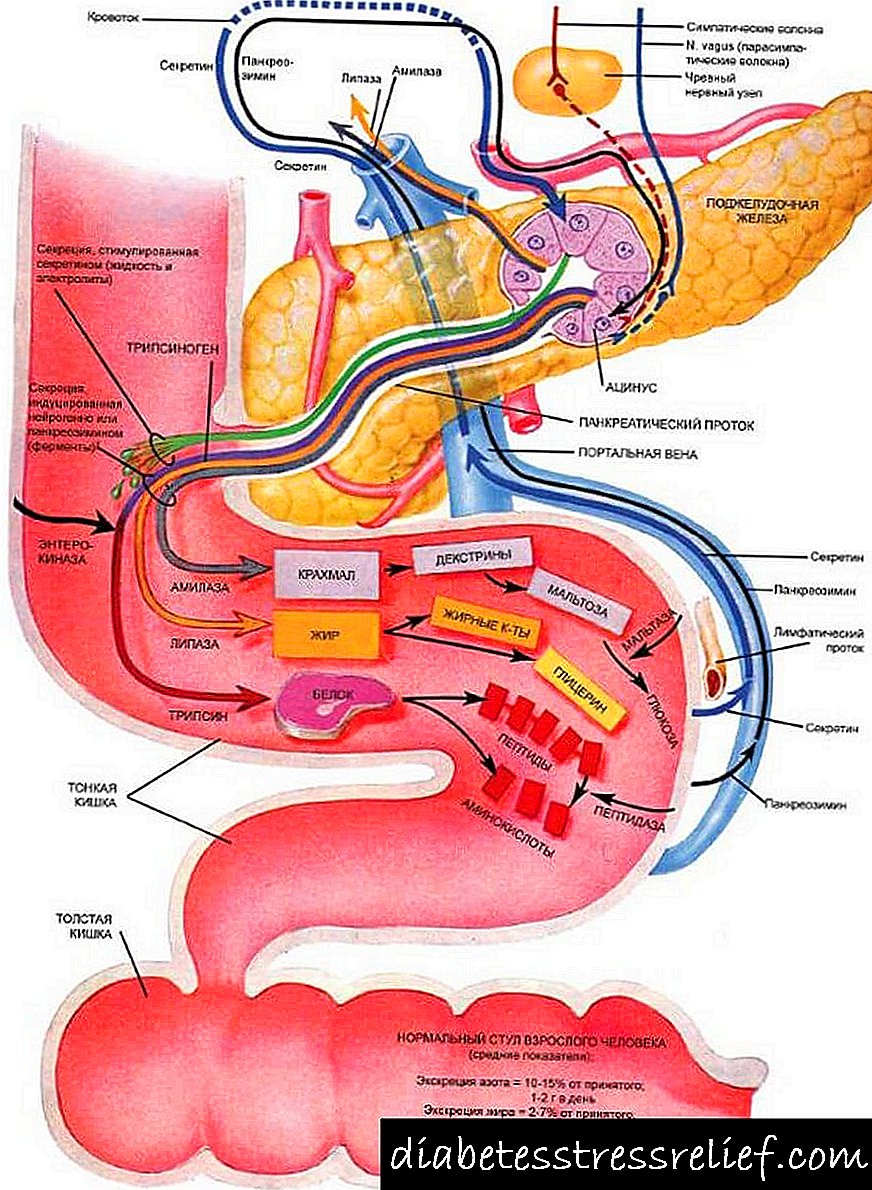
با وجود این واقعیت که لوزالمعده یک اندام کامل است ، آناتومی و بافت شناسی آن به طور قابل توجهی با دیگران متفاوت است.
ساختار بافت شناسی لوزالمعده
بافت شناسی یک بخش علمی از زیست شناسی است که به بررسی ساختار و عملکرد اجزای بدن ، بافت ها و اندام ها می پردازد. لوزالمعده تنها اندام در بدن است که ترشحات داخلی و خارجی را تشکیل می دهد و ترشح می کند. بنابراین ، ساختار بافت شناسی لوزالمعده از ساختار نسبتاً پیچیده ای برخوردار است.
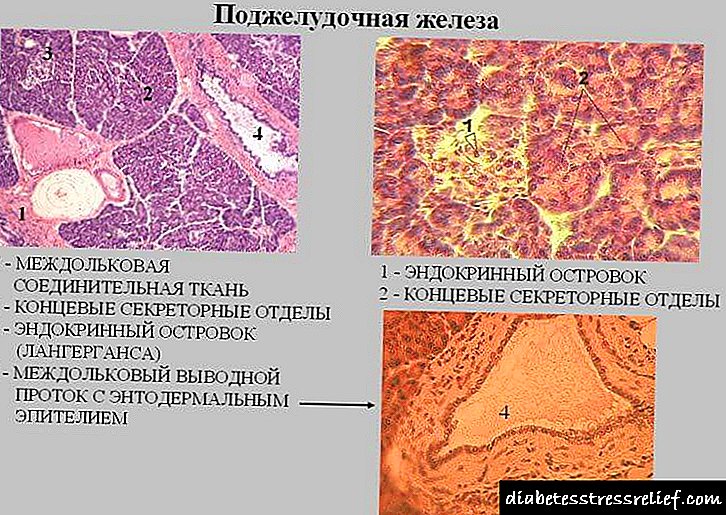
به منظور انجام یک معاینه کامل و کامل از بافت ها با استفاده از آماده سازی بافت شناسی. اینها قطعاتی از بافت هستند که برای آزمایش در زیر میکروسکوپ با ترکیبات خاص رنگ آمیزی شده اند.
بافت اگزوکرین
بافت پانکراس اگزوکرین از acini تشکیل شده است ، که آنزیم های گوارشی و مجاری را تشکیل می دهند و آنها را دفع می کند. Acini متراکم در کنار هم قرار گرفته و با یک لایه نازک از بافت شل حاوی رگ های خونی متصل شده است. سلولهای ناحیه اگزوکرین غده شکل مثلثی دارند. هسته سلول گرد است.
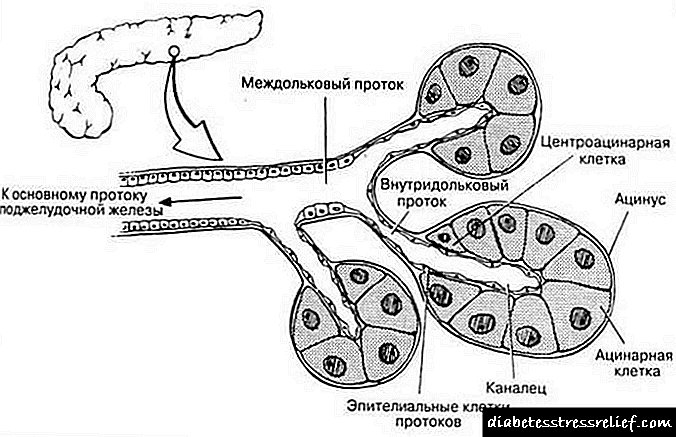
خود Acini به دو بخش پایه و آپیکال تقسیم می شوند. پایه حاوی غشایی از شبکه گرانول است. هنگام استفاده از یک آماده سازی بافت شناسی ، رنگ آمیزی این قسمت کاملاً یکنواخت خواهد بود. آپیکال نیز به نوبه خود رنگهای اسیدی به خود می گیرد. با کمک یک آماده سازی بافت شناسی ، می توان میتوکندری به خوبی توسعه یافته و مجموعه Golgi را نیز در نظر گرفت.
مجاری برای دفع آنزیم ها نیز انواع مختلفی دارند:
- عمومی - از بین لوبولی ، بهم پیوسته تشکیل شده است.
- درج - در ناحیه قسمت درج از اسكینوس بومی سازی شده است. آنها اپیتلیوم مسطح و مکعبی دارند.
- بین لوبولی - پوشیده از پوسته تک لایه.
- داخل چشم (داخل عضلانی).
به کمک پوسته های این مجاری ، بی کربنات ها ترشح می شوند ، که محیط آب قلیایی را در آب لوزالمعده تشکیل می دهد.
بافت غدد درون ریز
این قسمت از لوزالمعده از جزایر به اصطلاح لانگرهان تشکیل شده و از مجموعه سلولهایی تشکیل شده است که شکل گرد و بیضی دارند. این بافت به دلیل وجود شبکه های مویرگی ، به خوبی با خون تأمین می شود. سلول های وی هنگام استفاده از یک آماده سازی بافت شناسی ضعیف می شوند.
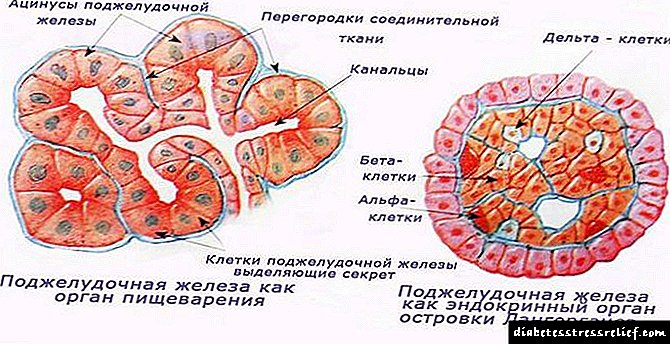
به عنوان یک قاعده ، انواع زیر متمایز می شوند:
- الف - در مناطق محیطی تولید می شود و آنتاگونیست انسولین به حساب می آید. آنها را می توان با الکل حل کرد و در آب حل کرد. گلوکاگون تولید می شود.
- ب - تعداد بسیار زیادی از جمعیت را نشان می دهد و در مرکز جزایر واقع شده است. آنها منبع انسولین هستند که قند خون را پایین می آورند. به خوبی در الکل محلول است. ضعیف با دارو آغشته شده است.
- د - هورمون سوماتوستاتین را که باعث کند شدن سنتز سلولهای A و B می شود تشکیل و ترشح می کند. آنها از نظر تراکم و اندازه متوسط هستند ، در حاشیه قرار دارند.
- D-1 - یک پلی پپتید تولید کرده و کوچکترین گروه سلول را نشان می دهد. مسئول کاهش فشار ، فعال کردن ترشح غده است. چگالی بالایی دارند.
- سلول های PP - یک پلی پپتید را سنتز می کنند و باعث افزایش تولید آب لوزالمعده می شوند. آنها همچنین در حاشیه مناطق واقع شده اند.
هورمون هایی که توسط جزایر لانگرهان تشکیل می شوند بلافاصله به خون منتقل می شوند زیرا مجاری ندارند. علاوه بر این ، بزرگترین قسمت از این سایتها در "دم" لوزالمعده قرار دارد. به طور معمول تعداد آنها با گذشت زمان تغییر می کند. بنابراین در دوره رشد فعال بدن افزایش می یابد و بعد از بیست و پنج سال به تدریج شروع به کاهش می کند.
جزایر لانگرهانس
قسمت غدد درون ریز کوچکتر توسط جزایر لوزالمعده یا جزایر لانگرهانس (insulae pancreaticae ، insula - islet) تشکیل شده است که بین acini قسمت غالب caudal غده واقع شده است.
جزایر با لایه ای از بافت همبند نازک از acini جدا شده و خوشه های سلولی به شکل گرد هستند که توسط یک شبکه متراکم از مویرگ ها با قطر حدود 0.3 میلی متر نفوذ می کنند.
تعداد کل آنها تقریباً 1 میلیون نفر است. غدد درون ریز در رشتهها مویرگهای جزایر ، در تماس نزدیک با عروق را از طریق فرآیندهای سیتوپلاسمی یا مستقیماً در مجاورت آنها احاطه می کنند.
خصوصیات فیزیکوشیمیایی و مورفولوژیکی دانه های غدد درون ریز ترشح ترشح می شود پنج نوع سلول ترشحی:
- سلولهای آلفا (10 تا 30٪) گلوکاگون تولید می کنند ،
- سلولهای بتا (٪ 60-80) انسولین را سنتز می کند ،
- دلتا و د1و فریزر (5-10)) یک پپتید وازو-روده سوماتواستاتین تشکیل می دهند ،
- سلولهای PP (2-5٪) پلی پپتید پانکراس ایجاد می کند.
سلولهای بتا عمدتاً در ناحیه مرکزی جزایر قرار دارند ، در حالی که اندوکرینوسیت های باقیمانده در حاشیه آن قرار دارند.
علاوه بر گونه های اصلی ، نوع خاصی از سلول ها در منطقه جزایر قرار دارد - سلول های آسیلینوس (مختلط یا گذرا) که هم عملکرد غدد درونریز و هم اگزوژن را انجام می دهند. علاوه بر این ، سلولهای تنظیم موضعی غدد درون ریز تولید گاسترین ، تیرولایبرین و سوماتولیبرین در جزایر یافت می شوند.