سیروز رنگدانه ، هموکروماتوز با نام مستعار: علائم و اصول درمان آسیب شناسی
هموکروماتوز (سیروز رنگدانه کبد ، دیابت برنز)
- یک بیماری ارثی که با افزایش جذب آهن در روده و رسوب رنگدانه های حاوی آهن در اندام ها و بافت ها (عمدتاً به صورت هموسیدین) همراه با ایجاد فیبروز مشخص می شود.
(یو. توکاروف ، D.A. Settarova ، 1988 ، با اضافات).
1. هموکروماتوز ارثی (ایدیوپاتیک ، اولیه).
2. هموکروماتوز ثانویه ، فرم:
2.1. پس از تزریق (در صورت کم خونی مزمن ، در معالجه که از انتقال خون برای مدت طولانی استفاده می شود).
2.2. هوشیار (هموکروماتوز بانتو آفریقایی آفریقا به دلیل مصرف بیش از حد آهن با غذا و آب ، سیروز الکلی کبد ، احتمالاً بیماری کاشان بک و غیره).
2.3 متابولیک (اختلال در متابولیسم آهن در بتا تالاسمی واسطه متوسط ، در بیماران مبتلا به سیروز کبد با ایجاد یا استفاده از آناستوموز پورتوکاال ، با انسداد مجرای لوزالمعده ، پورفیری جلدی و غیره).
2.4 منشأ مختلط (تالاسمی بزرگ ، برخی از انواع آنمی dyserythropoietic - نسوز آهن ، siderohrestical ، sideroblastic).
در حال حاضر ، نقش عوامل ژنتیکی در ایجاد هموکروماتوز ایدیوپاتیک اثبات شده است. شیوع ژن هموکروماتوز ارثی (بر روی بازوی کوتاه کروموزوم VI بومی سازی شده است و از نزدیک با منطقه آنتی ژن های سیستم تطابق پذیری HLA مرتبط است) 0.03-0.07٪ با فرکانس هتروزیگوزیته در جمعیت اروپا حدود 10٪ است. این بیماری در 3-5 مورد به ازای هر 1000 حامل ژن هموکروماتوز ارثی ایجاد می شود و توسط یک نوع مغلوب اتوزومی منتقل می شود. رابطه ای بین هموکروماتوز ارثی وجود دارد - یک نقص آنزیمی مادرزادی منجر به تجمع آهن در اندام های داخلی ، و آنتی ژن های سازگاری بافتی سیستم H1A - AZ، B7، B14، Ac
در هموکروماتوز ایدیوپاتیک ، نقص اصلی عملکردی ، اختلال در تنظیم جذب آهن توسط سلولهای مخاط دستگاه گوارش است که منجر به جذب نامحدود آهن و به دنبال آن رسوب بیش از حد هموسایدرین رنگدانه حاوی آهن در کبد ، لوزالمعده ، قلب ، بیضه ها و سایر اندام ها (عدم وجود "حد جذب") می شود. این منجر به مرگ عناصر عملکردی فعال و ایجاد روند اسکلروتیک می شود. علائم بالینی سیروز کبد ، دیابت قندی ، کاردیومیوپاتی متابولیک رخ می دهد.
بدن یک فرد سالم حاوی 3-4 گرم آهن ، همراه با هموکروماتوز - 60- 20 گرم است این به این دلیل است که روزانه حدود 10 میلی گرم آهن در هموکروماتوز جذب می شود ، در حالی که در یک بزرگسال سالم حدود 1.5 میلی گرم (حداکثر 2 میلی گرم) است. ) بنابراین ، طی یک سال ، حدود 3 گرم آهن اضافی در بدن بیمار مبتلا به هموکروماتوز تجمع می یابد. به همین دلیل است که علائم بالینی اصلی هموکروماتوز تقریباً 7-10 سال پس از شروع بیماری ظاهر می شود (L. N. Valenkevich، 1986).
هموکروماتوز ثانویه اغلب با سیروز کبد ، سوء مصرف الکل ، تغذیه پروتئین معیوب ایجاد می شود.
با سیروز کبدی ، سنتز ترانسفرین کاهش می یابد ، که آهن را در خون متصل می کند و آن را به مغز استخوان (برای گلبول های قرمز) ، به بافت (برای فعالیت آنزیم های تنفس بافت) و به انبار آهن منتقل می کند. با کمبود ترانسفرین ، تجمع آهن استفاده نشده برای سوخت و ساز رخ می دهد. علاوه بر این ، با سیروز کبد ، سنتز فریتین ، که نوعی انبار آهن است ، مختل می شود.
سوء مصرف الکل منجر به افزایش جذب آهن در روده می شود که این امر به بروز سریعتر علائم هموکروماتوز ارثی یا آسیب کبدی و ایجاد شکل ثانویه بیماری منجر می شود.
وجود آناستوموزها در سیستم پورتال باعث افزایش رسوب آهن در کبد می شود.
با کم خونی نسوز آهن (سایدروسترسیکال) و تالاسمی بزرگ ، از آهن جذب شده استفاده نمی شود ، زائد است و در کبد ، میوکارد و سایر ارگان ها و بافت ها رسوب می کند.
اکثراً مردان مبتلا هستند (نسبت زنان و مردان 20: 1) ، شکل توسعه یافته بیماری در سن 40-60 سالگی بروز می کند. فرکانس پایین تر این بیماری در زنان به این دلیل است که زنان در طی 25-35 سال آهن را با خون قاعدگی از دست می دهند (O.
علائم بالینی اصلی:
1. رنگدانه پوستی (ملاسما) در 52-94٪ از بیماران مشاهده می شود (S. D. Podymova ، 1984). در اثر رسوب در اپیدرم رنگدانه های بدون آهن (ملانین ، لیپو فسسین) و هموسیدین ایجاد می شود. شدت رنگدانه بستگی به مدت زمان بیماری دارد. پوست دارای رنگ دودی ، برنز ، خاکستری است که بیشتر در مناطق باز بدن (صورت ، دستها) ، در مناطق قبلاً رنگدانه ، در زیر بغل ، در ناحیه دستگاه تناسلی مشاهده می شود.
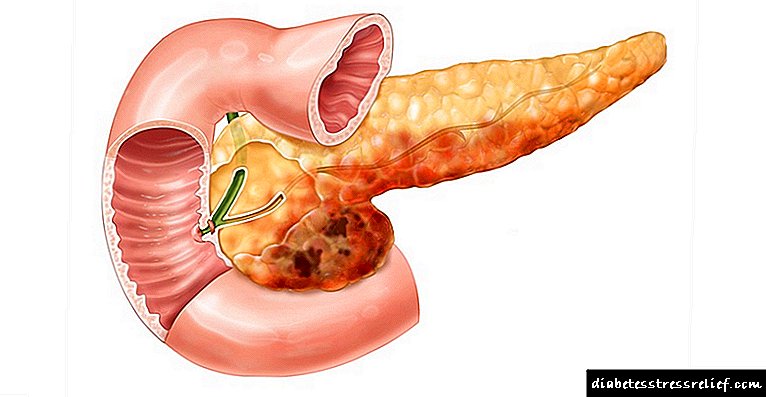
2. افزایش کبد در 97٪ از بیماران در مرحله پیشرفته بیماری مشاهده می شود ، کبد متراکم است ، غالباً دردناک است. در آینده تصویر بالینی سیروز کبدی با آسیت ، فشار خون بالا پورتال ، اسپلنومگالی ایجاد می شود.
3. دیابت قندی در 80٪ بیماران مشاهده می شود ، که ناشی از رسوب آهن در جزایر لانگرهانس است ، که با تشنگی ، پلیوریا ، هایپرگلیسمی ، گلیکوزوری نشان داده می شود. بندرت توسط اسیدوز و کما پیچیده است.
4- سایر اختلالات غدد درون ریز - کمبود فشار خون (کاهش قدرت ، آتروفی بیضه ، از بین رفتن خصوصیات جنسی ثانویه ، زنانه شدن ، در زنان - آمنوره ، ناباروری) ، کمبود فشار خون (ضعف شدید ، کاهش فشار خون ، کاهش شدید وزن).
5- کاردیومیوپاتی با افزایش قلب ، اختلال در ریتم ، رشد تدریجی نارسایی قلبی ، مقاوم در برابر درمان با گلیکوزیدهای قلبی همراه است. 35٪ بیماران هموکروماتوز در اثر نارسایی احتقانی قلب جان خود را از دست می دهند.
6- سندرم سوء جذب متابولیک در اثر اختلال در روده کوچک و لوزالمعده به دلیل رسوب رنگدانه حاوی آهن در این اندام ها ایجاد می شود.
دوره هموکروماتوز اولیه طولانی است (15 سال یا بیشتر) ، با پیشرفت سیروز کبدی ، امید به زندگی وجود ندارد
بیش از 10 سال با وجود هموکروماتوز ثانویه ، امید به زندگی کوتاهتر است.
1. UAC: علائم کم خونی (در همه بیماران) ، افزایش ESR.
2. OAM: پروتئینوری متوسط ، urobilinuria ، گلوکوزوری امکان پذیر است ؛ دفع آهن و ادرار تا 10-20 میلی گرم در روز افزایش می یابد (طبیعی - تا 2 میلی گرم در روز).
3. LHC: سطح آهن سرم بیش از 37 میکرومول در لیتر ، فریتین سرم بیش از 200 میکرومول در لیتر ، درصد اشباع ترانسفرین با آهن بیش از 50٪ ، افزایش ALAT ، tg-globulins ، تست تیمول ، اختلال در تحمل گلوکز یا قند خون
4- کاهش سطح 11-ACS ، 17-ACS ، سدیم ، کلرید ، هیدروکورتیزون ، کاهش میزان دفع روزانه ادرار 17-ACS ، 17-KS ، کاهش سطح هورمونهای جنسی در خون و ادرار.
5- سوراخ داخلی: دیکته دارای محتوای بالای آهن است.
6. در نمونه های بیوپسی پوست - رسوب بیش از حد ملانین ، در نمونه های بیوپسی کبد - رسوب هموسیدرین ، لیپوفوسسین ، تصویری از سیروز میکرونودولار. طبق گفته سارتاپ (1982) میزان آهن موجود در كبد در طی هموکروماتوز اولیه تقریباً 40 برابر نسبت به هنجار افزایش می یابد و در هموکروماتوز ثانویه 5/5 برابر می شود.
7. تست دسفرال - بر اساس توانایی دسفرال در پیوند آهن فریتین و هموسیدرین و خارج کردن آن از بدن. آزمایش مثبت تلقی می شود اگر بعد از تزریق عضلانی 0.5 تا 1 گرم دسفرال در روز ، بیش از 2 میلی گرم آهن در ادرار دفع شود.
1. اسکن سونوگرافی و رادیوایزوتوپ: بزرگ شدن کبد ، لوزالمعده ، تغییرات پراکنده در آنها ، طحال.
2. FEGDS: با ایجاد سیروز کبد ، رگهای واریسی مری و معده تشخیص داده می شود.
3. اکوکاردیوگرافی: افزایش اندازه قلب ، کاهش عملکرد انقباض میوکارد.
4. نوار قلب: تغییرات پراکنده در میوکارد (کاهش موج T ، فاصله 8-T) ، طولانی شدن فاصله (^ -T ، ناهنجاری های قلبی
1. OA خون ، ادرار ، تجزیه و تحلیل ادرار برای گلوکز ، urobilin ، بیلی روبین.
2. LHC: بیلی روبین ، ترانس آمینازها ، کل پروتئین و پروتئین ها ، کسری پروتئین ، گلوکز ، پتاسیم ، سدیم ، کلریدها ، آهن سرم ، فریتین سرم ، درصد اشباع ترانسفرین با آهن. با قند خون طبیعی ، یک آزمایش تحمل گلوکز.
3. اسکن سونوگرافی از کبد ، طحال ، لوزالمعده ، کلیه ها.
6. تعیین محتوای هورمونهای جنسی در خون ، هیدروکورتیزون.
7. تعیین دفع ادرار روزانه 17-OKS ، 17-KS.
سیروز رنگدانه ، هموکروماتوز با نام مستعار: علائم و اصول درمان آسیب شناسی

هموکروماتوز برای اولین بار به عنوان یک بیماری جداگانه در سال 1889 توصیف شد. با این وجود ، با ایجاد ژنتیک پزشکی ، دقیقاً می توان دلایل بیماری را مشخص کرد.
چنین طبقه بندی نسبتاً دیررس با ماهیت بیماری و توزیع نسبتاً محدود آن ترویج شد.
بنابراین ، براساس داده های مدرن ، 0.33 درصد از ساکنان جهان در معرض خطر ابتلا به هموکروماتوز هستند. چه عواملی باعث ایجاد بیماری شده و علائم آن چیست؟
هموکروماتوز - چیست؟

این بیماری ارثی است و با کثرت علائم و خطر بالای عوارض جدی و آسیب شناسی همراه مشخص می شود.
مطالعات نشان داده اند که هموکروماتوز بیشتر در اثر جهش در ژن HFE ایجاد می شود.
در نتیجه خرابی ژن ، مکانیسم جذب آهن در اثنی عشر مختل می شود.. این امر به این واقعیت منجر می شود که بدن در مورد کمبود آهن در بدن یک پیام کاذب دریافت می کند و به طور فعال و در مقادیر اضافی پروتئین ویژه ای را می چسبد که به آهن متصل می شود.
این منجر به رسوب بیش از حد hemosiderin (رنگدانه غده) در اندام های داخلی می شود. در کنار افزایش سنتز پروتئین ، فعال شدن دستگاه گوارش اتفاق می افتد و منجر به جذب بیش از حد آهن از مواد غذایی در روده می شود.
بنابراین حتی با تغذیه طبیعی ، مقدار آهن موجود در بدن چندین برابر بیشتر از حد طبیعی است. این منجر به از بین رفتن بافت های اندام های داخلی ، مشکلات سیستم غدد درون ریز و ایمنی بدن می شود.
طبقه بندی بر اساس انواع ، فرم ها و مراحل



در عمل پزشکی ، انواع اولیه و ثانویه بیماری تقسیم می شود. در این حالت ، اصلی ، که به آن ارثی نیز گفته می شود ، نتیجه یک پیش بینی ژنتیکی است. هموکروماتوز ثانویه نتیجه توسعه انحراف در کار سیستم های آنزیمی درگیر در متابولیسم غده است.
چهار نوع از بیماری ارثی (ژنتیکی) از بیماری شناخته شده است:
- کلاسیک
- نوجوان
- ارثی HFE گونه های جدا نشده ،
- اتوزومال غالب.
نوع اول با جهش کلاسیکی مغلوب ناحیه ششم کروموزوم همراه است. این نوع در اکثر موارد تشخیص داده می شود - بیش از 95 درصد بیماران از هموکروماتوز کلاسیک رنج می برند.
نوع بیماری نوجوانان در نتیجه جهش در ژن دیگری یعنی HAMP رخ می دهد. تحت تأثیر این تغییر ، سنتز هپسیدین ، آنزیمی که مسئول رسوب آهن در اندامها است ، به میزان قابل توجهی افزایش می یابد. معمولاً این بیماری بین سنین ده تا سی سالگی بروز می یابد.
نوع جدا نشده HFE در صورت عدم موفقیت ژن HJV ایجاد می شود. این آسیب شناسی شامل مکانیسم بیش فعالی گیرنده های ترانسفرین-2 است. در نتیجه ، تولید هپسیدین شدت می یابد. تفاوت با نوع بیماری نوجوانان در این است که در حالت اول ، یک ژن از کار می افتد ، که مستقیماً مسئول تولید آنزیم اتصال دهنده آهن است.

در حالی که در حالت دوم ، بدن یک ویژگی خاصیت اضافی آهن در مواد غذایی ایجاد می کند ، که منجر به تولید آنزیم می شود.
نوع چهارم هموکروماتوز ارثی با نقص ژن SLC40A1 همراه است.
این بیماری در پیری ظاهر می شود و با سنتز نادرست پروتئین فروپورتین ، که وظیفه انتقال ترکیبات آهن به سلول ها را بر عهده دارد ، همراه است.
جهش Missense و عوامل خطر

جهش ژنتیکی در یک نوع بیماری ارثی ، نتیجه پیامدهای شخص است.
مطالعات نشان می دهد که اکثر بیماران ساکن سفیدپوست آمریکای شمالی و اروپا هستند و بیشترین تعداد بیماران مبتلا به هموکروماتوز در بین مهاجران از ایرلند مشاهده شده است.
علاوه بر این ، شیوع انواع مختلف جهش ها برای مناطق مختلف جهان مشخص است. مردان چندین برابر بیشتر از خانم ها مستعد ابتلا به این بیماری هستند. در حالت دوم ، علائم معمولاً پس از تغییرات هورمونی در بدن ناشی از یائسگی بروز می کند.
در بین بیماران ثبت شده ، زنان 7-10 برابر کمتر از مردان هستند. دلایل تغییر هنوز مشخص نیست. فقط ماهیت ارثی این بیماری بطور غیرقابل انکار ثابت شده و ارتباط بین وجود هموکروماتوز و فیبروز کبدی نیز ردیابی می شود.

در حالیکه رشد بافت همبند را نمی توان مستقیم با تجمع آهن در بدن توضیح داد ، تا 70٪ بیماران هموکروماتوز فیبروز کبدی داشتند.
علاوه بر این ، یک پیشگیری ژنتیکی لزوماً منجر به پیشرفت بیماری نمی شود.
علاوه بر این ، یک شکل ثانویه هموکروماتوز وجود دارد ، که در افرادی که ژنتیک در ابتدا طبیعی هستند مشاهده می شود. عوامل خطر همچنین برخی از آسیب شناسی ها را شامل می شود. بنابراین ، استئاته هپاتیت منتقل شده (رسوب غیر الکلی بافت چربی) ، ایجاد هپاتیت مزمن علل مختلف و همچنین انسداد لوزالمعده در بروز بیماری نقش دارد.
برخی از نئوپلاسم های بدخیم همچنین می توانند به عنوان یک کاتالیزور برای پیشرفت هموکروماتوز تبدیل شوند.
علائم هموکروماتوز در زنان و مردان

دیابت از این روش درمانی مانند آتش می ترسد!
شما فقط نیاز به اعمال ...

در گذشته ، فقط ایجاد تعدادی از تظاهرات علامت دار جدی باعث می شد تا این بیماری تشخیص داده شود.
بیمار با تجمع بیش از حد آهن احساس خستگی مزمن ، ضعف می کند.
این علائم مشخصه 75٪ بیماران هماتوکروماتوز است. رنگدانه های پوست افزایش یافته است ، و این روند با تولید ملانین همراه نیست. به دلیل تجمع ترکیبات آهن در آنجا ، پوست تیره تر می شود. تیرگی در بیش از 70٪ بیماران مشاهده شده است.
اثر منفی آهن تجمع یافته بر روی سلولهای ایمنی بدن باعث ضعف ایمنی می شود. بنابراین ، با روند بیماری ، استعداد بیمار در برابر عفونت ها افزایش می یابد - از شرایط کاملاً جدی تا پیش پا افتاده و بی ضرر در شرایط عادی.

حدود نیمی از بیماران از آسیب شناسی های مفصلی رنج می برند که در بروز درد بیان می شود.
همچنین در تحرک آنها رو به وخامت گذاشته شده است. این علائم به وجود می آید زیرا مقدار زیادی از ترکیبات آهن باعث رسوب کلسیم موجود در مفاصل می شوند.
آریتمی و ایجاد نارسایی قلبی نیز ممکن است. تأثیر منفی بر لوزالمعده اغلب منجر به دیابت می شود. آهن بیش از حد باعث اختلال در عملکرد غدد عرق می شود. در موارد بسیار نادر ، سردرد مشاهده می شود.
بروز این بیماری منجر به ناتوانی جنسی در مردان می شود. کاهش عملکرد جنسی نشانگر علائم مسمومیت بدن با محصولات مرکب آهن است. در خانمها خونریزی شدید هنگام تنظیم ممکن است.

یک علائم مهم کبد بزرگ شده و همچنین درد شدید شکم است که به نظر می رسد شناسایی سیستمیک امکان پذیر نیست.
وجود چندین علائم نشانگر لزوم تشخیص دقیق آزمایشگاهی بیماری است.
علامت بیماری وجود هموگلوبین زیاد در خون است که مقدار کم آن همزمان در گلبولهای قرمز وجود دارد. سطح ترانسفرین آهن زیر 50 درصد از علائم آزمایشگاهی هموکروماتوز محسوب می شود.
وجود هتروزیگوتهای پیچیده یا جهش های هموزیگوت از نوع خاصی در ژن HFE با شواهد بالینی از تجمع بیش از حد آهن نشان دهنده پیشرفت هموکروماتوز است.
افزایش قابل توجه کبد با تراکم بالای بافت های آن نیز از علائم بیماری است. علاوه بر این ، با هموکروماتوز ، تغییر رنگ بافت کبد مشاهده می شود.
چگونه در کودک بروز می کند؟

هموکروماتوز اولیه دارای چندین ویژگی است - از جهش هایی که باعث شده است تا مناطق کروموزوم مربوطه گرفته تا تصویر و تظاهرات بالینی مشخصه.
اول از همه ، علائم بیماری در سنین پایین چند شکلی است.
کودکان با ایجاد علائم و نشانه های فشار خون بالا در پورتال مشخص می شوند. نقض هضم غذا ، افزایش همزمان طحال و کبد را ایجاد می کند.
با توسعه پاتولوژی ، سنگین و مقاوم در برابر اثرات درمانی آسیت - قطره ای که در ناحیه شکم تشکیل می شود. توسعه رگهای واریسی مری مشخص است.
سیر بیماری شدید است و پیش آگهی درمان تقریباً همیشه نامطلوب است. تقریباً در همه موارد ، این بیماری شکل جدی نارسایی کبد را تحریک می کند.
چه آزمایشات و روشهای تشخیصی به شناسایی آسیب شناسی کمک می کند؟

برای شناسایی این بیماری از چندین روش مختلف آزمایشگاهی تشخیصی استفاده می شود.
در ابتدا نمونه گیری خون برای بررسی سطح هموگلوبین در گلبول های قرمز و پلاسما انجام می شود.
ارزیابی متابولیسم آهن نیز انجام می شود.
آزمایش desferal به تأیید تشخیص کمک می کند. برای این کار ، تزریق داروی غده ای انجام می شود و پس از پنج ساعت نمونه ادرار گرفته می شود. علاوه بر این ، CT و MRI اندامهای داخلی برای تعیین تغییرات آسیب شناختی آنها انجام می شود - افزایش اندازه ، رنگدانه و تغییر در ساختار بافت.
اسکن ژنتیکی مولکولی به شما امکان می دهد وجود یک قسمت آسیب دیده از کروموزوم را مشخص کنید. این مطالعه که در بین اعضای خانواده بیمار انجام شده ، به ما امکان می دهد حتی قبل از شروع تظاهرات بالینی آن که بیمار را مختل می کند ، احتمال بروز این بیماری را نیز ارزیابی کنیم.
اصول درمانی
روشهای اصلی درمان ، عادی سازی قرائت های موجود در آهن و جلوگیری از آسیب رساندن به اندام ها و سیستم های داخلی است. متأسفانه ، طب مدرن نحوه عادی سازی دستگاه ژن را نمی داند.

روش متداول درمان خون ریزی است. با درمان اولیه ، هفته ای 500 میلی گرم خون برداشته می شود. پس از عادی سازی شاخص های میزان آهن ، هنگامی که نمونه گیری خون هر سه ماه یک بار انجام می شود ، به درمان درمانی می روند.
تجویز داخل وریدی داروهای اتصال دهنده آهن نیز انجام می شود. بنابراین ، شلاتات اجازه می دهد تا مواد اضافی را با ادرار یا مدفوع از بین ببرید. با این حال ، یک دوره کوتاه از عمل باعث می شود که تزریق به طور منظم زیر جلدی داروها با کمک پمپ های مخصوص لازم باشد.
نظارت آزمایشگاهی هر سه ماه یک بار انجام می شود. این شامل شمارش مقدار آهن و همچنین تشخیص علائم کم خونی و سایر عواقب بیماری است.
عوارض و پیش آگهی های احتمالی
با تشخیص زودهنگام ، بیماری به طور مؤثر قابل کنترل است.
طول مدت و کیفیت زندگی بیمارانی که مراقبت منظم از آنها انجام می شود ، متفاوت از افراد سالم نیست.
علاوه بر این ، درمان به موقع منجر به عوارض جدی می شود. این موارد شامل ایجاد سیروز و نارسایی کبدی ، دیابت ، آسیب به رگها تا خونریزی است.
احتمال ابتلا به کاردیومیوپاتی و سرطان کبد خطر بالایی دارد ، همچنین عفونت های هم زمان مشاهده می شود.
هموکروماتوز
تعریف هموکروماتوز نوعی بیماری است که با تجمع بیش از حد آهن در سلولهای اندامهای مختلف با آسیب و عملکرد مختص این اندامها همراه است.
ICD10: E83.1 - نقض متابولیسم آهن.
اتیولوژی هموکروماتوز ایدیوپاتیک اولیه و هموکروماتوز علامت دار اکتسابی ثانویه وجود دارد.
هموکروماتوز اولیه یک بیماری مغلوب اتوزومی مادرزادی است که در اثر نقص در ژن واقع در بازوی کوتاه کروموزوم VI ایجاد می شود.
هموکروماتوز ثانویه می تواند هنگامی ایجاد شود که آهن بیش از حد در بدن وجود داشته باشد ، و با عبور مکرر از گلبول های قرمز خون روده ها را دور می زند. غالباً هنگامی رخ می دهد که آهن در سیستم خونریزی نشده در بیماران مبتلا به کم خونی siderochrestic ، تالاسمی جذب نمی شود. علت آن ممکن است سوء استفاده از داروهای حاوی آهن باشد ، ویتامین ث. نوشابه های الکلی باعث افزایش تجمع آهن در بدن می شوند. نیمی از بیماران مبتلا به هموکروماتوز علامت دار الکلی هستند.
پاتوژنز. در افراد سالم آهن اضافی موجود در خون به شکل هموسیدین به صورت نامحلول واریز می شود. در مغز استخوان ماکروفاژها حاوی گرانول هموسیدین (sideroblasts) قرار دارند. با عدم جذب و یا جذب بیش از حد آهن در بدن ، تعداد sideroblasts در مغز استخوان به شدت افزایش می یابد. این حالت هموسیدروز نامیده می شود. برگشت پذیر است ، همراه با آسیب به اندام های داخلی نیست.
با ورود بیشتر بدن به بدن ، آهن در مکان های غیرمعمول - در کبد ، قلب ، لوزالمعده ، دیواره روده و غیره - ذخیره می شود. به این حالت هموکروماتوز گفته می شود. این بیماری با نقض جدی در ساختار و عملکرد اندام هایی که آهن رسوب می کنند همراه است. تجمع پاتولوژیک آهن یک عامل مهم در بیماریهای جدی مانند سیروز ، دیابت قندی ، کاردیومیوپاتی محدود کننده است.
حلقه اصلی در پاتوژنز هموکروماتوز ایدیوپاتیک مادرزادی مادرزادی نقص تعیین شده ژنتیکی در سیستم های آنزیمی است که جذب آهن را در روده تنظیم می کند. در چنین بیمارانی ، با مصرف طبیعی آهن با غذا ، میزان جذب آن از روده افزایش می یابد - تا 10 میلی گرم در روز به جای 1.5 میلی گرم طبیعی. استفاده و دفع آهن از بدن تغییر نمی کند. مقدار کل آهن در بدن بیماران مبتلا به IG به 60- 20 گرم می رسد ، در حالی که در افراد سالم از 3-4 گرم تجاوز نمی کند.
تصویر بالینی مردان بیشتر بیمار می شوند. شروع بیماری بتدریج است. علائم مشخصه 1-3 سال پس از ظهور تغییرات مورفولوژیکی در اندام های داخلی ظاهر می شود. در مراحل اولیه بیماری ، ضعف شدید ، خستگی ، کاهش وزن ، خشکی و تغییرات آتروفی پوست ، ریزش مو و اختلال عملکرد جنسی در آقایان و خانم ها مشاهده می شود.
تظاهرات بالینی این بیماری در بیشتر موارد در سن 40-60 سالگی رخ می دهد. این توسط سه گانه کلاسیک آشکار می شود:
رنگدانه پوست و غشاهای مخاطی.
رنگدانه در بیشتر بیماران مشاهده می شود. شدت آن به مدت زمان بیماری بستگی دارد. پوست رنگی برنز دارد. رنگدانه در قسمتهای آزاد بدن ، در زیر بغل ، در ناحیه تناسلی برجسته تر است.
افزایش کبد تقریباً در کلیه بیماران مبتلا به هموکروماتوز مشاهده می شود. کبد متراکم ، صاف ، با یک لبه جلوی برجسته است ، گاهی اوقات در لمس دردناک است. اسپلنومگالی و "علائم کبدی" نسبتاً نادر است. در مرحله ترمینال ، علائم سیروز جبران نشده کبد غالب است - نارسایی سلول کبدی ، فشار خون بالا در پرتال ، آسیت ، ورم هیپوپروتئینمی.
دفع آهن در لوزالمعده در سلول های جزایر لانگرهانس منجر به دیابت وابسته به انسولین می شود ، که با تجویز پلی اوری ، عطش همراه است. عوارض دیابت به صورت اسیدوز ، اغما نادر است.
بیشتر بیماران آسیب قلبی دارند - کاردیومیوپاتی محدود کننده ثانویه. از نظر عینی ، این بیماری با وجود کاردیومگالی ، انواع اختلالات ریتم و هدایت بروز می یابد و به تدریج در نارسایی قلبی ایجاد می شود. علت مرگ هر بیمار سوم هموکروماتوز جبران نارسایی قلبی است.
سندرم سوء جذب ممکن است ایجاد شود - اسهال با اختلال در جذب پروتئین ها ، کربوهیدرات ها ، چربی های موجود در روده. این امر بر اساس اختلال در عملکرد دیواره روده و لوزالمعده مرتبط با رسوب هموسیدین در سلولهای این اندامها است.
اغلب آرتروپاتی با شکستگی مفاصل کوچک دست ، باسن ، زانوها اتفاق می افتد. در نیمی از موارد ، این یک پیشگویی است - رسوب در غشای سینوویال پیرو فسفات کلسیم.
1/3 از بیماران دارای علائم نارسایی غدد درون ریز چندضلعی است: هیپوفیز ، هیپوفیز ، آدرنال ، غده تیروئید ، آتروفی بیضه در مردان ، آمنوره در زنان.
تشخیصی شمارش کامل خون: ممکن است طبیعی باشد. در موارد جدا شده ، علائم کم خونی ، افزایش ESR مشاهده می شود.
تجزیه و تحلیل بیوشیمیایی خون: افزایش محتوای آهن سرم ، فریتین ، اشباع ترانسفرین با آهن ، قند خون ، افزایش فعالیت ALT ، AST. ممکن است هیپوپروتئینمی رخ دهد (با جبران سیروز).
ادرار: گلوکوزوری ، پروتئینوری متوسط ، افزایش دفع آهن.
تست دسفرال: پس از تجویز عضلانی 0.5-1 گرم دسفرال با ادرار ، بیش از 2 میلی گرم آهن در روز آزاد می شود.
سوراخ شدن داخلی: در مغز استخوان تعداد زیادی از سایدوبلاست ها - ماکروفاژها حاوی اجزاء هموسیدین.
بیوپسی پوست: اپیدرم نازک شده است ، در اپیتلیوم مقدار زیادی ملاتونین رنگدانه ، هموسیدین.
بیوپسی کبد: علائم مورفولوژیکی هپاتیت ، سیروز میکرونودولار. در مراحل اولیه ، با استفاده از واکنش پرلز ، رسوبات آهن به صورت فریتین و hemosiderin در مناطق جانبی ، در سلولهای کوپفر ، در مراحل بعدی - در سلولهای اپیتلیال مجاریهای صفراوی ، در سپرهای فیبری شناسایی می شوند.
نوار قلب: تغییرات پراکنده در میوکارد عمدتا در بطن چپ ، انواع ریتم و اختلالات هدایت.
اکوکاردیوگرافی: گشاد شدن حفره های کلیه محفظه های قلب ، نقض عملکرد دیاستولیک (کاردیومیوپاتی محدود کننده) ، کاهش کسر جهشی ، سکته مغزی و برون ده قلبی.
معاینه سونوگرافی: علائم سیروز ، فشار خون بالا در پرتال ، تغییرات پراکنده در ساختار لوزالمعده ، کلیه ها.
تشخیص افتراقی. اول از همه ، لازم است که هموکروماتوز از هموسیدروز متمایز شود. در یک بررسی بافت شناسی از punctates کبدی ، یک تفاوت مشخص بین hemosiderosis ثانویه و hemochromatosis حفظ ساختار طبیعی لوبولار پارانشیم است. با هموکروماتوز ، تصویر بافتی از هپاتیت مزمن و / یا سیروز رخ می دهد.
سیروز الکلی کبد می تواند علائمی شبیه به هموکروماتوز ایدیوپاتیک داشته باشد: ناتوانی جنسی ، رنگدانه های پوستی ، ریزش مو ، دیابت ، قلب و عروق. اکثر مبتلایان به الکل ، رسوب آهن را در کبد نشان می دهند (هموسیدروز ثانویه). با این حال ، اجسام مالوری ، یک شبکه آندوپلاسمی صاف متراکم ، در نمونه های بیوپسی کبد با سیروز الکلی تشخیص داده می شوند ، که با هموکروماتوز اتفاق نمی افتد. با این وجود ، در بسیاری از مشروبات الکلی ، آسیب کبدی ممکن است به دلیل ایجاد هموکروماتوز ثانویه باشد.
آزمایش خون عمومی.
آزمایش خون بیوشیمیایی: آهن ، فریتین ، اشباع آهن ترانسفرین ، قند ، بیلی روبین ، پروتئین کل ، AST ، ALT.
ادرار با تعیین دفع آهن.
تست دسفرال برای افزایش ترشح آهن در ادرار.