دیابت فسفات در کودکان: علل ، علائم ، اصول درمانی

فسفات دیابت - نقض ژنتیکی متابولیسم معدنی ، که در آن جذب و جذب ترکیبات فسفر در بدن رنج می برد ، که منجر به آسیب شناسی سیستم اسکلتی می شود. طبق آخرین اطلاعات ، این یک گروه کاملاً از بیماریهای ارثی است. این بیماری با افت فشار خون عضلات ، ریشه های اسکلت (تغییر شکل های استخوانی اندام تحتانی ، راکت و دیگران) ، عقب ماندگی رشد بروز می یابد. تشخیص دیابت فسفات براساس نتایج آزمایشات آزمایشگاهی خون و ادرار (سطح قلیایی فسفاتاز ، یون های کلسیم ، فرم فعال ویتامین D) و آنالیزهای ژنتیکی مولکولی انجام می شود. درمان این بیماری با تجویز مقادیر زیاد ویتامین D ، فسفر و ترکیبات کلسیم ، اصلاح ارتوپدی یا جراحی ناهنجاری های اسکلتی انجام می شود.

اطلاعات عمومی
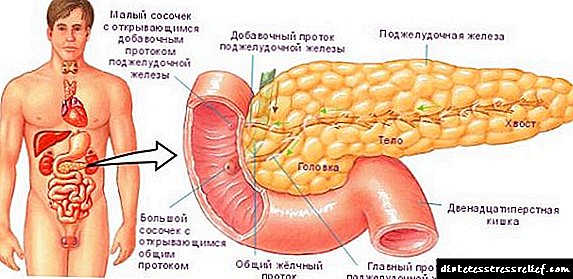
دیابت فسفات (راکت مقاوم در برابر ویتامین D) نام جمعی برای تعدادی از توبوپاتی های تعیین شده ژنتیکی (اختلالات پاتولوژیک حمل و نقل مواد در توبول های کلیه ها) است که در آنها جذب مجدد یون های فسفات با ایجاد نقص آنها در بدن مختل می شود. یکی از شایع ترین اشکال خانوادگی این بیماری ، که توسط مکانیسم غالب مرتبط با کروموزوم X منتقل می شود ، در سال 1937 شرح داده شد. در سال های بعد ، متخصصان ژنتیک چندین نوع دیابت دیگر از فسفات را با علل مختلف ، انتقال ارثی و تصویر بالینی نشان دادند. با این حال ، همه آنها دارای ویژگی های مشترک هستند - آنها در اثر اختلال در جذب فسفر در کلیه ها ایجاد می شوند ، با علائمی شبیه به راکتز مشخص می شوند و تا حدودی نسبت به استفاده از دوزهای معمول ویتامین D. مقاوم هستند تا به امروز ، اشکال خانوادگی دیابت فسفات مشخص شده است که انتقال آن به کروموزوم X مرتبط است ( غالب و مغلوب) ، اتوزومال غالب و اتوزومال مغلوب. شیوع رایج ترین انواع این بیماری 1:20 000 (شکل غالب وابسته به X) است ، انواع دیگر بسیار کمتر دیده می شود.

علل و طبقه بندی دیابت فسفات
علیرغم ناهمگونی ژنتیکی دیابت فسفات ، علل فوری هیپوفسفاتمی در اشکال مختلف بیماری یکسان است - نقض جذب معکوس (جذب مجدد) فسفات ها در لوله های پیچیده کلیه ها. این امر به شما امکان می دهد این شرایط را به توبوپاتی ها یا آسیب شناسی های سیستم ادراری نسبت دهید ، اما در صورت بروز ، کل بدن و به خصوص سیستم اسکلتی عضلانی رنج می برد. علاوه بر این ، برخی از اشکال دیابت فسفات با اختلال در جذب کلسیم در روده و کلیه ، ایجاد urolithiasis ، فعالیت غیر طبیعی غدد پاراتیروئید همراه است. بین انواع ژنتیکی و بالینی بیماری ارتباط مستقیمی وجود دارد ، که به ما امکان می دهد یک طبقه بندی واضح و کلی پذیرفته شده ایجاد کنیم که شامل 5 شکل آسیب شناسی است.
دیابت غالب فسفات مرتبط با X - به دلیل جهش ژن PHEX ، شایع ترین نوع این آسیب شناسی است. کد کننده آنزیمی به نام آندوپپتیداز است که فعالیت کانال های یونی کلیه ها و روده کوچک را کنترل می کند. در نتیجه نقص ژنتیکی ، آنزیم به دست آمده قادر به انجام وظایف خود نیست ، بنابراین ، انتقال فعال یون های فسفات از طریق غشای سلولی در اندام های فوق به شدت کاهش می یابد. این امر منجر به افزایش از دست رفتن یون های فسفات در ادرار و مشکل در جذب آنها در دستگاه گوارش می شود و به همین دلیل هیپوفسفاتمی در خون ایجاد می شود و به دلیل کمبود اجزای معدنی تغییراتی مانند ریشه در بافت استخوان ایجاد می شود.
دیابت فسفات مغلوب مرتبط با X - برخلاف نسخه قبلی ، این فقط مردان را تحت تأثیر قرار می دهد ، در حالی که زنان فقط می توانند به عنوان حامل ژن پاتولوژیک عمل کنند. علت این شکل از بیماری جهش ژن CLCN5 است که یک توالی کانال یونی پروتئین-کلر را کد می کند. در نتیجه نقص ژنتیکی ، حمل و نقل همه یونها (از جمله فسفاتها) از طریق غشای سلولهای اپیتلیال نفرون ناراحت است و به همین دلیل دیابت فسفات ایجاد می شود.
اتوزومال غالب فسفات دیابت - نوعی بیماری ناشی از جهش ژن FGF23 که در کروموزوم 12 قرار دارد. محصول بیان آن پروتئینی است که به اشتباه به عنوان فاکتور رشد فیبروبلاست-23 خوانده می شود ، اگرچه عمدتا توسط استئووبلاست ها ترشح می شود و دفع یون های فسفات در ادرار را تسریع می کند. دیابت فسفات با جهش FGF23 ایجاد می شود ، در نتیجه پروتئین تولید شده در برابر عمل پروتئازهای خون مقاوم می شود و به همین دلیل انباشته می شود و بر همین اساس با پیشرفت هیپوفسفاتمی این اثر تشدید می شود. این نوع بیماری نوعی نسبتاً خفیف دیابت فسفات محسوب می شود.
دیابت فسفات اتوزومال مغلوب نوعی آسیب شناسی بسیار نادر است که ناشی از جهش در ژن DMP1 واقع در کروموزوم 4 است. این ژن یک فسفوپروتئین عاج ماتریکس اسیدی ، که عمدتاً در عاج و بافت استخوانی تشکیل شده است ، رمزگذاری می کند ، جایی که رشد آنها را تنظیم می کند. پاتوژنز دیابت فسفات در این نوع ژنتیکی کاملاً مورد مطالعه قرار نگرفته است.
دیابت فسفات اتوزومال مغلوب با هیپرکلسیوری - همچنین یک نوع نادر از این بیماری ، ناشی از جهش ژن SLC34A3 واقع در کروموزوم 9 است. این توالی کانال وابسته به سدیم یونهای فسفات در کلیه را رمزگذاری می کند و با نقص در ساختار منجر به افزایش دفع کلسیم و فسفر در ادرار با کاهش همزمان پلاسما می شود.
همچنین اشکال دیابت فسفات وجود دارد که همراه با هایپرپاراتیروئیدیسم ، urolithiasis و سایر اختلالات است. برخی از انواع این بیماری با ژن هایی مانند ENPP1 ، SLC34A1 و برخی دیگر همراه هستند. مطالعه همه دلایل احتمالی دیابت فسفات هنوز ادامه دارد.
علائم دیابت فسفات
تظاهرات دیابت فسفات به دلیل ناهمگونی ژنتیکی این بیماری با شدت نسبتاً گسترده ای - از یک دوره تقریباً بدون علامت تا اختلالات شدید آشکار - مشخص می شود. برخی موارد آسیب شناسی (به عنوان مثال ، به دلیل جهش در ژن FGF23) فقط با هیپوفسفاتمی و افزایش سطح فسفر در ادرار قابل مشاهده است ، در حالی که علائم بالینی وجود ندارد. با این حال ، بیشتر اوقات ، دیابت فسفات منجر به تصویری از ریشه های معمولی می شود و عمدتاً در کودکی - 1-2 سال ، به زودی پس از شروع راه رفتن کودک گسترش می یابد.
فشار خون عضلانی در اوایل شیرخوارگی ممکن است یکی از اولین تظاهرات دیابت فسفات باشد ، اما در همه موارد مشاهده نمی شود. بیشتر اوقات ، پیشرفت بیماری با تغییر شکل O از پاها آغاز می شود ، که می تواند به اختلال در راه رفتن منجر شود. با ادامه دوره دیابت فسفات ، سایر علائم بالینی راکتی می توانند رخ دهند - عقب ماندگی رشد و رشد جسمی ، اختلال در تشکیل دندان (به خصوص با فرم مغلوب اتوزومی بیماری) ، آلوپسی. شکستگی های پاتولوژیک ، ظهور راکت ها "تسبیح" ، ضخیم شدن متافیزیک استخوان اندام ها مشخصه است. همچنین ، با دیابت فسفات ، درد در ناحیه پشت (معمولاً از نظر عصبی) و استخوان مشاهده می شود ، در موارد نادری ، به دلیل درد در پاها ، کودک از فرصت پیاده روی محروم می شود. به طور معمول ، اختلالات رشد ذهنی در این بیماری ذکر نمی شود.
تشخیص دیابت فسفات
یکی از اولین روشها برای تشخیص دیابت فسفات ، معاینه کلی کودک بیمار و بررسی واکنش این بیماری به استفاده از دوزهای معمول ویتامین D. به عنوان یک قاعده است ، با این آسیب شناسی ، یک تصویر بالینی از راکت ها با مقاومت در برابر استفاده از داروهای سنتی این ویتامین (روغن ماهی ، محلول روغن) وجود دارد. . برای تعیین دقیق تر دیابت فسفات با استفاده از روش های مطالعات بیوشیمیایی خون و ادرار ، مطالعات اشعه ایکس ، آنالیز ژنتیکی مولکولی. تظاهرات ثابت این بیماری هیپوفسفاتمی یا کاهش سطح یونهای فسفات در پلاسما خون است که به عنوان بخشی از آنالیز بیوشیمیایی تعیین می شود. در عین حال ، سطح کلسیم می تواند طبیعی باشد و یا حتی افزایش یابد ، با این حال ، برخی از اشکال دیابت فسفات (به دلیل جهش در ژن SLC34A3) همچنین با هیپوکلسمی مشخص می شوند. همچنین ، با دیابت فسفات ، افزایش سطح قلیایی فسفاتاز و گاهی افزایش سطح هورمونهای پاراتیروئید ممکن است رخ دهد. آزمایش ادرار بیوشیمیایی میزان دفع زیاد فسفر (هایپروفوسفاتوری) و در برخی موارد چربی خون را نشان می دهد.
مطالعات رادیولوژیکی دیابت فسفات علائم کلاسیک راکتی را تعیین می کند - تغییر شکل استخوان های پاها ، زانوها و باسن ، وجود پوکی استخوان (در بعضی موارد ممکن است پوکی استخوان موضعی رخ دهد) و پوکی استخوان. ساختار استخوان ها تغییر یافته است - لایه قشر ضخیم می شود ، الگوی ترابکولار درشت تر می شود ، دیافیزس گسترش می یابد. غالباً سن پرتونگاری استخوان با دیابت فسفات به میزان قابل توجهی عقب مانده است ، که نشانگر تأخیر در پیشرفت اسکلت است. ژنتیک مدرن به شما امکان می دهد تقریباً انواع مختلفی از این بیماری را تشخیص دهید ، به عنوان یک قاعده ، از روش توالی یابی مستقیم ژن های مرتبط با آسیب شناسی استفاده می شود. در برخی موارد ، سابقه ژنتیکی در بیمار ممکن است ماهیت ژنتیکی دیابت فسفات را نشان دهد.
درمان دیابت فسفات
دیابت فسفات با ترکیبی از ویتامین درمانی ، ارتوپدی و گاهی تکنیک های جراحی درمان می شود. با وجود نام دیگر این آسیب شناسی (راکت مقاوم به ویتامین D) ، این ویتامین به طور فعال در درمان این بیماری استفاده می شود ، اما باید دوزها به میزان قابل توجهی افزایش یابد. علاوه بر این ، در بیماران دیابتی فسفات ، داروهای آماده سازی کلسیم و فسفر ، ویتامین های A ، E و گروه B تجویز می شود ، لازم است که درمان با ویتامین های محلول در چربی (خصوصاً D و A) به طور انحصاری تحت نظارت پزشک و با رعایت دقیق دوزها انجام شود تا از بروز عوارض جانبی ناخواسته جلوگیری شود و عوارض برای نظارت بر اثربخشی درمان و صحت دوز تجویز شده دارو ، اندازه گیری منظم سطح فسفات و کلسیم در ادرار انجام می شود. در خصوص اشکال شدید دیابت فسفات ، استفاده از ویتامین D ممکن است برای زندگی مشخص شود.
در تشخیص اولیه این بیماری ، درمان آن لزوماً شامل پیشگیری از اختلالات اسکلتی با تکنیک های ارتوپدی به طور کلی پذیرفته شده - پوشیدن بانداژ برای ستون فقرات است. با تشخیص بعدی دیابت فسفات با ناهنجاری های شدید اسکلتی ، ممکن است اصلاح جراحی نشان داده شود. اشکال بدون علامت این بیماری ، که فقط با هیپوفسفاتمی و هیپرفسفاتوریا بروز می کند ، به گفته اکثر متخصصان ، نیازی به درمان فشرده ندارند. با این وجود ، نظارت دقیق بر وضعیت اسکلت ، سیستم عضلانی و کلیه ها (پیشگیری از ورولیتیتازیس) لازم است که از طریق معاینات پزشکی منظم توسط متخصص غدد انجام می شود.
پیش بینی و پیشگیری از دیابت فسفات
پیش آگهی دیابت فسفات می تواند متفاوت باشد و به عوامل زیادی بستگی دارد - نوع بیماری ، شدت علائم ، سن تعیین پاتولوژی و شروع درمان مناسب. بیشتر اوقات ، پیش آگهی مطلوب است ، اما نیاز مادام العمر برای استفاده از ویتامین D ، کلسیم و فسفر آماده است. ناهنجاری های اسکلتی مشخص شده ناشی از تشخیص دیرهنگام یا درمان نادرست دیابت فسفات می تواند کیفیت زندگی بیمار را مختل کند. پیشگیری از این بیماری ارثی فقط به صورت مشاوره پزشکی و ژنتیکی والدین قبل از بچهدار شدن امکان پذیر است ، برای برخی اشکال روشهای تشخیص پیش از تولد تدوین شده است.
علل و انواع دیابت فسفات
اولین توصیف های این بیماری در قرن بیستم ظاهر شد. بيمار با شايع ترين نوع رايكس هيپوفسفاتميك ثبت شد و نقش وراثت در بروز آن ثابت شد. بعداً ، انواع دیگری از دیابت فسفات نیز مشخص شد که هم خصوصیات مشترک دارند و هم علل آنها ، نوع وراثت و ویژگیهای دوره. در زیر ما به موارد اصلی می پردازیم.
- راکتهای هیپوفسفاتماتیک مرتبط با X. این یکی از شایع ترین بیماری های شبیه به راکت است ، فرکانس آن 1: 20،000 نفر از جمعیت کودک است. علت این آسیب شناسی در نظر گرفته شده جهش در ژن PHEX است که فعالیت آنزیم اندوپپتیداز درگیر در فعال سازی و تخریب هورمونهای مختلف پپتید را رمزگذاری می کند. در این حالت ، کمبود پروتئین ها رخ می دهد ، تركیبات فسفر را در لوله های نفرون (یك واحد ساختاری كلیه) و روده ها حمل می كنند كه منجر به از بین رفتن یون های فسفر در ادرار و اختلال در جذب در دستگاه گوارش می شود. بنابراین ، متابولیسم فسفر و کلسیم در بدن مختل می شود و علائم مختلف پاتولوژیک مرتبط با این اتفاق می افتد. روند بیماری با نقض متابولیسم ویتامین D در سلولهای کبدی (سلولهای کبدی) و ترشح بیش از حد غدد پاراتیروئید توسط هورمون پاراتیروئید تشدید می شود.
- راکت های هیپوفسفاتماتی غالب اتوزومی این شکل از بیماری نسبت به نوع قبلی کمتر دیده می شود و روند شدیدتری نیز دارد. این بیماری با جهش ژن FGF-23 همراه است ، کاریوتایپ شده بر روی کروموزوم 12. این ژن یک عامل در گردش است که به منظور مهار جذب مجدد کلیوی (جذب مجدد از ادرار) فسفاتها توسط استئوسیت ها (سلول های استخوانی) ساخته می شود. با افزایش فعالیت آن در خون ، هیپوفسفاتمی مشاهده می شود.
- راکت های هیپوفسفاتماتو مغلوب اتوزومی این نوع دیابت فسفات ناشی از جهش در ژن DMP1 است ، که وظیفه سنتز یک پروتئین خاص استخوانی را دارد که در تنظیم تکثیر استئوبلاستهای تمایز نیافته (سلولهای استخوانی نابالغ) نقش دارد. همچنین باعث از بین رفتن فسفر در ادرار در غلظت طبیعی هورمون پاراتیروئید و کلسیتریول می شود.
- راکت هیپوفسفاتماتی ارثی با هیپرکلسیوریا. این یک آسیب شناسی نسبتاً نادر است که به دلیل جهش ژن SLC34A3 وجود دارد ، که فعالیت شرکتهای انتقال دهنده فسفات سدیم را رمزگذاری می کند ، و این امر انتقال حمل و نقل مواد در لوله های کلیوی و هموستاز فسفات را فراهم می کند. این بیماری با از بین رفتن فسفر و کلسیم در ادرار ، افزایش فعالیت کلسیتریول و ایجاد راکت مشخص می شود.
دوره بالینی دیابت فسفات چند شکل است. این بیماری معمولاً در اوایل کودکی آغاز می شود ، اما می تواند دیرتر بروز کند - در 7-9 سالگی. علاوه بر این ، شدت علائم پاتولوژیک نیز ممکن است متفاوت باشد. در بعضی موارد ، این بیماری دارای یک دوره بدون علامت است و با تغییرات خفیف در متابولیسم فسفر-کلسیم بروز می کند. با این حال ، بیشتر اوقات ریکت های هیپوفسفاتمیک یک تصویر بالینی برجسته دارد:
- عقب ماندگی رشد جسمی و نرخ رشد ،
- ناهنجاری های اسکلتی (تغییر شکل وارس از اندام تحتانی ، "راکت" روی دنده ها ، ضخیم شدن استخوان های لوله دیستال ساعد ، تغییر شکل جمجمه) ،
- تغییر در راه رفتن کودک (شبیه اردک)
- نقض تشکیل دندان ها ،
- شکستگی های پاتولوژیک ،
- درد استخوان و غیره
فشارخون عضلانی ، مشخصه ریشه های واقعی ، معمولاً در دیابت فسفات وجود ندارد.
رشد فکری در این بیماری رنج نمی برد.
تشخیصی
تشخیص دیابت فسفات در کودکان براساس تصویر بالینی معمولی ، داده های مربوط به معاینه و معاینه فیزیکی است. این تشخیص توسط نتایج مطالعات آزمایشگاهی و ابزاری تأیید می شود:
- تغییرات آزمایش خون (هیپوفسفاتمی ، افزایش فسفاتاز قلیایی ، سطح طبیعی یا زیاد هورمون پاراتیروئید و کلسیتونین) و ادرار (هایپروفسفاتوریا ، کاهش جذب مجدد فسفات در لولههای کلیوی ، افزایش دفع کلسیم تنها با راشهای هیپوفسفاتمیک با کلسیم) ،
- داده های اشعه ایکس (علائم پوکی استخوان سیستمیک ، ناهنجاری استخوان ، تغییر در ساختار استخوان ، پوکی استخوان).
بعضی اوقات در شروع بیماری ، چنین بیمارانی با راشیت تشخیص داده می شوند و دارو با ویتامین D تجویز می شود ، چنین درمانی نتیجه ای حاصل نمی کند و دلیلی برای ظن دیابت فسفات در کودک ایجاد می کند. در صورت لزوم ، در چنین مواردی می توان یک مطالعه ژنتیکی مولکولی برای شناسایی نقایص ژنتیکی اختصاص داد.
ترکیبی از هیپوفسفاتمی و راکتی اندام نیز در برخی شرایط پاتولوژیک دیگر مشاهده می شود که تشخیص افتراقی باید انجام شود:
- بیماری کلیه (اسیدوز توبولار کلیوی ، بیماری مزمن کلیه) و کبد (سیروز) ،
- آسیب شناسی غدد درون ریز (عملکرد بیش از حد غدد پاراتیروئید) ،
- سوء جذب در کولیت اولسراتیو ، آنتروپاتی سلیاک ،
- کمبود غذایی ویتامین D و فسفر ،
- مصرف داروهای خاص.
درمان جامع ریشه های هیپوفسفاتمیک باید در مراحل اولیه بیماری آغاز شود. اول از همه ، این امر با هدف اصلاح اختلالات متابولیک و جلوگیری از ناهنجاری های استخوانی انجام می شود. هنگام تجویز ، فعالیت فرآیند و تحمل فردی داروها در نظر گرفته می شود.
اساس اثر درمانی درمانی طولانی مدت با دوز بالای ویتامین D است. تجویز می شود:
- با راکت فعال در بافت استخوان ،
- از بین رفتن ترکیبات فسفر در ادرار ،
- افزایش سطح قلیایی فسفاتاز در خون ،
- در مرحله آماده سازی برای جراحی برای اصلاح ناهنجاری های اسکلتی.
دوزهای اولیه ویتامین D روزانه 10،000-20000 IU است. افزایش بیشتر آنها تحت کنترل شاخصهای متابولیسم فسفر-کلسیم در خون انجام می شود. حداکثر دوز روزانه می تواند بسیار زیاد باشد و بعضی اوقات به 250،000-300،000 IU برسد.
در صورت عدم تحمل فردی به ویتامین D و همچنین هیپرکلسیوریای شدید ، تعیین چنین درمانی نامناسب تلقی می شود.
علاوه بر ویتامین D ، به این بیماران توصیه می شود:
- فسفر و کلسیم آماده سازی ،
- مخلوط سیترات (در مدت 6 ماه برای بهبود جذب این عناصر کمیاب) ،
- هورمون رشد
در طی یک دوره فعالیت زیاد فرآیند ، به بیماران توصیه می شود بعد از دستیابی به بهبودی - استراحت در رختخواب را انجام دهند - ماساژ درمانی ، فعالیت بدنی با دوز و درمان آبگرم.
معیارهای اثربخشی درمان محافظه کارانه عبارتند از:
- رفاه عمومی ،
- شتاب رشد ،
- عادی سازی متابولیسم فسفر در بدن ،
- پویایی رادیولوژیکی مثبت (ترمیم ساختار طبیعی استخوان).
در صورت وجود ناهنجاریهای استخوانی برجسته در پس زمینه ترمیم مداوم بالینی و آزمایشگاهی ، اصلاح جراحی آنها انجام می شود. برای این کار می توان از روشهای زیر استفاده کرد:
- استئوتومی (برش) استخوانهای لولهای بلند با تصحیح محور اندامها ،
- بیحرکتی اندام توسط دستگاه پرت و فشار فشرده سازی الیزاروف.
چنین عملیاتی فقط باید بعد از درمان طولانی مدت محافظه کارانه و معاینه کامل انجام شود.
با کدام پزشک تماس بگیرید
در صورت مشکوک بودن به دیابت فسفات ، لازم است با پزشک متخصص کودک مشورت کنید که پس از معاینه اولیه ، کودک را برای مشاوره با متخصص غدد ، ارتوپدی و نفرولوژیک کودک ارجاع دهد. این درمان شامل یک ماساژور ، فیزیوتراپیست ، متخصص ورزش درمانی و تغذیه درمانی است. در صورت لزوم ، درمان توسط یک جراح ارتوپدی انجام می شود.