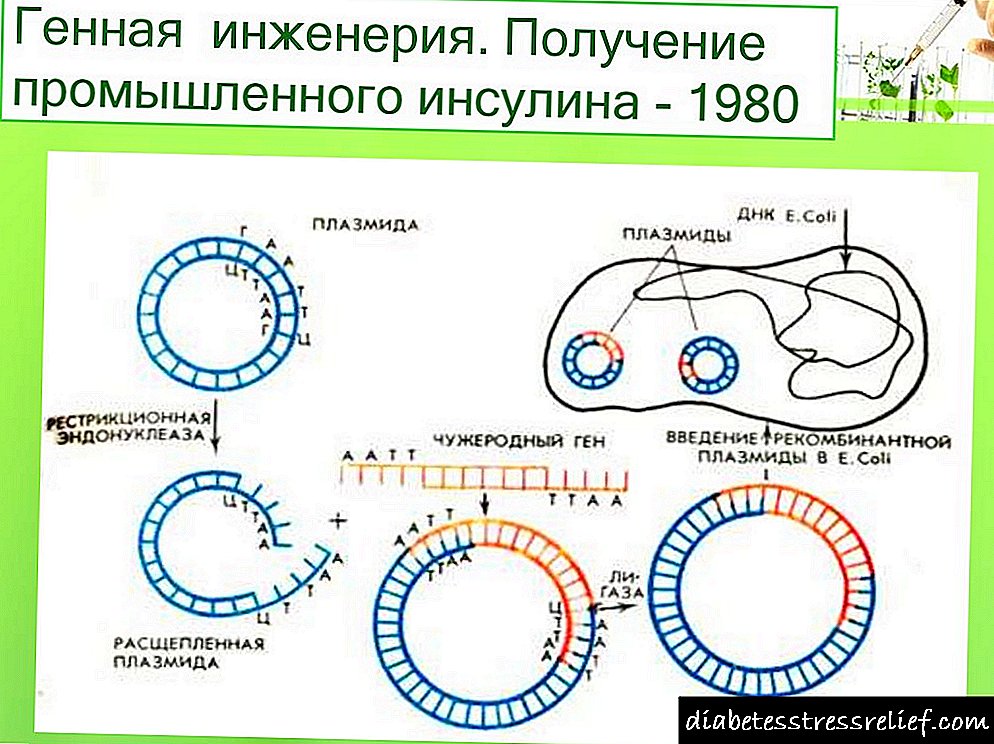
تولید انسولین مهندسی ژنتیک
انسولین - هورمون لوزالمعده که تنظیم کننده | متابولیسم کربوهیدرات و حفظ سطح طبیعی گاوبدوندر خون فقدان این هورمون در بدن منجر می شود.) به یکی از جدی ترین بیماری ها - دیابت ، که به عنوان علت مرگ ، بعد از بیماری های قلبی عروقی و سرطان در جایگاه سوم قرار دارد. انسولین یک گلوبول کوچک است | پروتئین حاوی 51 اسید آمینه باقی مانده و متشکل از دو زنجیره پلی پپتیدی است که توسط دو پل دی سولفید به یکدیگر وصل شده اند. این ماده به صورت پیش ماده جنین تک زنجیره ای ، پروپروئینسولین ، حاوی سنتز می شود کوی یک پپتید سیگنال مرکزی (23 باقیمانده اسید آمینه) و یک پپتید متصل به 35 پیوند (C-پپتید). وقتی پپتید سیگنال برداشته شود ، پروینسولین از 86 باقیمانده اسید آمینه در سلول تشکیل می شود ، که در آن زنجیره های A و B انسولین به هم وصل می شوندC-Neiیک توییت که جهت آنها را با قیمت 3 دلار در بورس دی سولفید فراهم می کند. پس از جدا شدن پروتئولیتیک پپتید C ، انسولین تشکیل می شود.
چندین شکل از دیابت شناخته شده است. شدیدترین شکل ، برای درمان که بیمار به انسولین نیاز دارد (یک نوع وابسته به انسولین بیماری) ، ناشی از مرگ انتخابی سلولهای سنتز کننده این هورمون (سلولهای جزایر لانگرهانس در پانکراس) است. نوعی دیابت قندی ، که برای آن نیاز به درمان با انسولین نیست ، رایج تر است ، می توان با کمک رژیمهای غذایی مناسب مدیریت کرد و دوباره: به طور معمول ، لوزالمعده گاو و گاو در صنایع گوشت و کنسرو استفاده نمی شود و برای شرکت های دارویی که استخراج هورمون در آنها انجام می شود ، در واگن های یخچال قرار می گیرد. برای به دست آوردن 100 گرم Cr! انسولین تالیک به 800-1000 کیلوگرم مواد اولیه نیاز دارد
سنتز هر دو زنجیره و اتصال پیوندهای disidfid آنها برای به دست آوردن انسولین در سال 1963 و 1965 انجام شد. سه تیم تحقیقاتی در ایالات متحده ، چین و آلمان. در سال 1980 ، شرکت دانمارکی Novo Industri با جایگزینی 30 ماده باقی مانده آلانین در زنجیره B با مانده ترئونین روشی را برای تبدیل انسولین خوک به انسولین انسانی ایجاد کرد. هر دو انسولین از نظر فعالیت و مدت زمان عملکرد متفاوت نبودند.
کار روی مهندسی ژنتیک انسولین از حدود 20 سال پیش آغاز شد. در سال 1978 ، پیامی در مورد تولید نوعی از اشرشیا کولی تولید پروینسولین موش (ایالات متحده) منتشر شد. در همان سال ، زنجیره های انسولین انسانی فردی با بیان ژن های مصنوعی آنها در سلول ها سنتز شدند.ایکولی(شکل 5.11). هر یک از ژنهای مصنوعی به دست آمده به انتهای 3 ژن ژن آنزیم (3-گالاکتوزیداز) تنظیم و وارد پلاسمید بردار شدند.(pBR322).سلولایکولیبا چنین پلاسمیدهای نوترکیب تبدیل شده ، پروتئین های ترکیبی (کیمریک) متشکل از قطعه ای از p-galactosidase و پپتید انسولین A یا B متصل به آن از طریق یک مانده متیونین تولید شد. هنگام پردازش پروتئین کیمریک با برمید سیانوژن ، پپتید آزاد می شود. با این حال ، بسته شدن پل های دی سولفید بین زنجیره های انسولین تشکیل شده دشوار بود.
در سال 1981 ، یک آنالوگ طرفدار انسولین ، مینی C-pro-انسولین ، ساخته شد که در آن 35 واحد C- پپتید با یک بخش از شش اسید آمینه جایگزین شد: arg-arg-gly-ser-lys-arg و بیان آن درایکولی
در سال 1980 ، دبلیو گیلبرت و همكارانش mRNA انسولین را از تومور لوزالمعده لوزالمعده موش جدا كردند و با استفاده از رونویسی معكوس ، cDNA را از آن بدست آوردند. cDNA حاصل در پلاسمید وارد شدpBR322ایکولیدر قسمت میانی ژن پنی سیلیناز. پلاسمید نوترکیب حاوی اطلاعاتی در مورد ساختار پروینسولین بود.در نتیجه ترجمه mRNA ، پروتئین هیبریدی در سلولهای حاوی توالی پنی سیلیناز و پروینسولین ساخته شد که با استفاده از تریپسین از چنین پروتئینی هضم شد.
در سال 1978 ، کارمندان مؤسسه شیمی بیو ارگانیک تحت نظارت Acad فعالیت می کنند. یو. A. اوچچنیکوف ، دو ژن ساختاری که سنتز نوروپپتیدها را رمزگذاری می کنند ، ساخته شدند:لوسین- انکفالین و برادی کینین.ژن آنسفالین لوسین سنتز دو انتهای "چسبنده" داشت:
ژن مصنوعی حاصل با یک قطعه DNA طبیعی حاوی پروموتر و پروگزیمال ژن پروتئین E. coli P-galactosidase وارد شد.ایکولیبه پلاسمید
به دست آوردن انسولین ، روشهای مهندسی ژنتیک ، بیوتکنولوژی - کار درسی

1. ساختار و عملکرد انسولین 5
1.1. ساختار مولکول انسولین 5
1.2 اهمیت بیولوژیکی انسولین 7
1.3 بیوسنتز انسولین 8
2. سنتز انسولین مهندسی ژنتیک 10
2.1. استفاده از روشهای مهندسی ژنتیک برای سنتز داروها 10
2.2. روشهای مهندسی ژنتیک 11
2.3 تولید انسولین مهندسی ژنتیک 14
گزیده ای از متن
علاوه بر این ، هر دو این مؤلفه ها ممکن است همزمان در ترکیب پروتئین ترکیبی موجود باشند. علاوه بر این ، هنگام ایجاد پروتئین های ترکیبی ، می توان از اصل چند بعدی بودن استفاده کرد - وجود چندین نسخه از پلی پپتید هدف در پروتئین ترکیبی ، که می تواند عملکرد محصول مورد نظر را به میزان قابل توجهی افزایش دهد.
در انگلستان ، هر دو رشته انسولین انسانی با استفاده از E. coli ، به مولکول هورمون بیولوژیکی فعال متصل شدند. برای اینکه یک ارگانیسم تک سلولی بتواند مولکولهای انسولین را بر روی ریبوزومهای خود سنتز کند ، لازم است برنامه لازم را تهیه کنید ، یعنی ژن هورمون را به آن معرفی کنید.
انسولین نوترکیب در انستیتوی آکادمی علوم روسیه با استفاده از سویه های ژنتیکی باکتری E. coli بدست آمد. پروتئین پیشرو ترکیبی از زیست توده رشد یافته ، بیان شده در مقادیر بیان شده است
40. از کل پروتئین سلولی حاوی پروپروئینسولین.
تبدیل آن به انسولین در شرایط آزمایشگاهی به همان ترتیب در داخل بدن انجام می شود - پلی پپتید پیشرو قطع می شود ، پیش پروینولین از طریق مراحل سولفیتولیز اکسیداتیو به انسولین تبدیل می شود و به دنبال آن بسته شدن کاهنده سه پیوند دی سولفید و جداسازی آنزیمی از C-پپتید اتصال دهنده انجام می شود. پس از یک سری تبادل یونی ، ژل و خالص سازی کروماتوگرافی HPLC ، انسولین انسانی با خلوص بالا و فعالیت طبیعی به دست می آید.
برای به دست آوردن انسولین ، یک کرنش با یک دنباله نوکلئوتیدی درج شده در پلاسمید که بیانگر یک پروتئین ترکیبی متشکل از یک پروینسولین خطی و قطعه ای از پروتئین استافیلوکوکوس اورئوس A است که از طریق باقیمانده متیونین 8 ، 9 ، 10 به انتهای N آن متصل می شود ، استفاده می شود.
کشت زیست توده اشباع شده سلولهای سویه نوترکیب ، آغاز تولید پروتئین ترکیبی را فراهم می کند ، جداسازی و تبدیل پی در پی آن در لوله منجر به انسولین می شود.
راه دیگر نیز ممکن است: به دست آوردن در سیستم باکتریایی بیان پروتئین نوترکیب متشکل از پروینسولین انسانی و دم پلی هیدیدین متصل به آن از طریق باقیمانده متیونین. با استفاده از کروماتوگرافی کلات روی ستونهایی که دارای نیکل آگارز و برم هستند جدا شده است.
پروتئین جدا شده S-sulfonated است. نقشه برداری و تجزیه و تحلیل طیف سنجی جرمی از پروینسولین به دست آمده خالص شده توسط کروماتوگرافی تبادل یونی بر روی رزین تبادل آنیون و RP (فاز معکوس) کروماتوگرافی مایع با کارایی بالا ، وجود پل های دی سولفید را نشان می دهد که مطابق با پل های دی سولفید پروتئینولین بومی انسان است.
اخیراً توجه ساده ای به ساده سازی روش تولید انسولین نوترکیب توسط مهندسی ژنتیک شده است.به عنوان مثال ، می توانید پروتئین متشکل از پروینسولین متصل به N- پایانه از طریق مانده لیزین رهبر اینترلوکین دریافت کنید
2- پروتئین به طور موثری در بدنهای ورود به بدن بیان و محلی سازی می شود. پس از جداسازی ، پروتئین برای تولید انسولین و پپتید C با تریپسین 5 ، 8 ، 10 پاک می شود.
انسولین حاصل و پپتید C با RP-HPLC خالص می شود. نسبت جرم پروتئین حامل و پلی پپتید هدف بسیار مهم است.
پپتیدهای C به کمک فاصله بین اسیدهای آمینه حامل محل محدودیت Sfi I و دو ماده باقیمانده آرژنین در ابتدا و انتهای فضا برای هضم پروتئین بعدی تریپسین طبق اصل سر سر به هم متصل می شوند.
HPLC محصولات شکاف نشان می دهد که شکاف C- پپتید به صورت کمی پیش می رود ، و این به استفاده از ژن های مصنوعی مولتی متر برای تولید پلی پپتیدهای هدف در مقیاس صنعتی اجازه می دهد.
نتیجه گیری
رادیکال ، و در بیشتر موارد ، تنها راه برای حفظ زندگی و ظرفیت کار بیماران مبتلا به دیابت تا به امروز ، انسولین است.
قبل از دریافت و معرفی انسولین در عمل بالینی ، از زمان شروع بیماری بیماران دیابتی نوع یک ، علی رغم استفاده از ناتوان کننده ترین رژیم های غذایی ، نتیجه مرگبار به مدت یک یا دو سال پیش بینی می شد.
بیماران دیابتی نوع I به درمان جایگزین مادام العمر با داروهای انسولین نیاز دارند. قطع تجویز منظم انسولین به یک دلیل یا دلیل دیگر منجر به رشد سریع عوارض و مرگ سریع بیمار می شود.
در حال حاضر ، شیوع دیابت پس از بیماری های سیستم قلبی عروقی و تومورهای بدخیم در جایگاه سوم قرار دارد. به گفته سازمان بهداشت جهانی شیوع دیابت در بزرگسالان ، در بیشتر مناطق جهان 2-5٪ است و تمایل به افزایش دارد
1. سال تعداد بیماران تقریبا دو برابر شده است. تعداد بیماران وابسته به انسولین علی رغم پیشرفت های آشکار در زمینه مراقبت های بهداشتی ، هر ساله در حال افزایش است و در حال حاضر تنها در روسیه حدود 2 میلیون نفر است.
امیدوار کننده ترین روشها برای تولید انسولین روشهای مهندسی ژنتیک است. انسولین مهندسی شده ژنتیکی با تولید جداگانه زنجیره های A و B با استفاده از سویه های مختلف تولید کننده و تاشو متعاقب آن مولکول و به دنبال آن جداسازی ایزوفرم ها و سنتز پروینسولین در سلول های E. coli با شکاف آن با تریپسین و کربوکسی پپتیداز و تولید انسولین بومی حاصل می شود.
ایجاد داروهای انسولین انسانی ژنتیکی داخلی ، برای نجات جان میلیون ها نفر از مبتلایان به دیابت ، امکانات جدیدی را برای حل بسیاری از مشکلات دیابت شناسی روسی ایجاد می کند.
ادبیات
Balabolkin M.I.، Klebanova E.M.، Kreminskaya V.M. دیابت قندی: جنبه های مدرن تشخیص و درمان / دکتر ، ویرایش. G.L. Vyshkovsky.-2005.- M: RLS-2005، 2004.- 960 ص.
گاوریکوف ، A.V. بهینه سازی تولید بیوتکنولوژیک مواد اینترفرونهای نوترکیب انسانی: دیس. ... نبات بیول علوم - م ، 2003
انسولین انسانی مهندسی ژنتیکی. افزایش بهره وری از جدایی کروماتوگرافی با استفاده از اصل عملکردی. / Romanchikov A.B.، Yakimov S.A.، Klyushnichenko V.E.، Arutunyan A.M.، Wulfson A.N. // شیمی بیوایی ، 1997 - 23 ، شماره 2
Glick B.، Pasternak J. کنترل استفاده از روشهای بیوتکنولوژیک // B. Glick، J. Parsnip / Biotechnology Molecular = بیوتکنولوژی مولکولی. - م: میر ، 2002 .-- س 517-532. - 589 ص.
Glick B. ، Pesticak J. بیوتکنولوژی مولکولی. اصول و کاربرد. م: میر ، 2002.
دیویس R. ، Botstein D ، Roth J. روشهای مهندسی ژنتیک. ژنتیک باکتری ها // R. Davis، D. Botstein، J. Roth / Per. از انگلیسی.-م: میر. - 1984.- 176 ص.
ارمیشین A.P.ارگانیسم های اصلاح شده ژنتیکی: اسطوره ها و واقعیت ها / A.P. Ermishin // Mn.: Tekhnalogaliya.- 2004. - 118 ص.
اصول بیوتکنولوژی دارویی: کتاب درسی / TP پریشپ ، V.S. چوچالین ، K.L. زایکوف ، L.K. میخالوا - روستوف روی دون: ققنوس ، تامسک: انتشارات NTL ، 2006.
Patrushev L.I. سیستم های ژنتیکی مصنوعی. // L.I. Patrushev / M.: Nauka.- 2004.
رومانچیکوف ، A.B. انسولین انسانی مهندسی ژنتیکی. افزایش بهره وری از جدایی کروماتوگرافی با استفاده از اصل عملکردی. / A.B. رومانچیکوف و دیگران.
// شیمی بیو ارگانیک. 1997. شماره 2. ص. 23
Rybchin V.N. اصول مهندسی ژنتیک // V.N. Rybchin / ed. 2 ، ویرایش شده. و کتاب اضافه کنید: کتاب درسی دانشگاه ها. SPb .: انتشارات SPbSTU. - 2002 .-- 522 s.
Schelkunov S. N. مهندسی ژنتیک // Schelkunov S. N. / Novosibirsk: Sib. دانشگاه انتشارات خانه .2008.
Schelkunov ، S.N. مهندسی ژنتیک: کتاب درسی. کمک هزینه - 2 ، ویرایش ، احیاء. و اضافه کنید - نووسیبیرسک: سیب. دانشگاه انتشارات خانه ، 2004 .-- 496 ص.
1. محل پیوندهای دی سولفید در مولکول انسولین.
2. ترتیب مانده اسیدهای آمینه در مولکول انسولین
تأثیر انسولین بر آنزیمهای متابولیک کلیدی
عضله کبد فعال سازی بافت چربی 1. فسفودی استراز 1. فسفودی استراز 1. LP-lipase
4- کمپلکس پیروات دهیدروژناز
4- کمپلکس پیروات دهیدروژناز
5- فسفاتاز گلیکوژن سنتاز و گلیکوژن فسفوریلاز
5- گلیکوژن سنتاز فسفاتاز b. القای استیل کوآ-کربوکسیلاز 1. گلوکوکیناز 1. گلیسیرالدئید فسفات دهیدروژناز
6. گلوکز-6-فسفات دهیدروژناز سرکوب فسفوئنولپیروات کربوکسیکیناز
شکل 3 طرح بیوسنتز انسولین در سلولهای β از جزایر لانگرهانس. ER - شبکه آندوپلاسمی. 1 - تشکیل یک پپتید سیگنال ، 2 - سنتز پروپروسولین ، 3 - برش پپتید سیگنال ، 4 - انتقال پروینسولین به دستگاه گلگی ، 5 - تبدیل پروینسولین به انسولین و پپتید C و گنجاندن انسولین و پپتید به گرانولهای ترشحی ، 6 - ترشح انسولین و پپتید C.
4- طرح کلی سنتز انسولین از پیشینیان
شکل 5 سنتز انسولین با تشکیل دو زنجیره جداگانه
روش بدست آوردن انسولین انسانی ژنتیکی مهندسی شده

این اختراع مربوط به زمینه بیوتکنولوژی ، به ویژه تولید انسولین انسانی ژنتیکی برای ساخت داروهای مورد استفاده در معالجه دیابت است.
این روش با کشت یک پروتئین تولیدکننده پروتئین ترکیبی حاوی پروینسولین انسانی ، Escherichia coli BL21 / pPINS07 (BL07) یا Escherichia coli JM109 / pPINS07 انجام می شود ، سلول ها را با تجزیه از هم جدا می کند ، بدن جدا کننده های حاوی پروتئین ترکیبی را جدا می کند.
در مرحله بعد ، شستشوی مقدماتی اجسام گنجاندن ، انحلال همزمان پروتئین و ترمیم پیوندهای دی سولفید در بافر با 5-10 میلی متر دیتیوتریتول و 1 میلی متر EDTA ، تجدید ساختار و تصفیه پروتئین فیوژن مجدد توسط کروماتوگرافی تبادل یونی انجام می شود.
شکاف پروتئین ترکیبی با هیدرولیز مشترک تریپسین و کربوکسی پپتیداز B با نسبت وزن پروتئین ترکیبی ، تریپسین و کربوکسی پپتیداز B 4000: 0.6: 0.9 انجام می شود.
تصفیه انسولین توسط کروماتوگرافی آبگریز یا کروماتوگرافی مایع با فاز معکوس و به دنبال آن فیلتراسیون ژل و جداسازی انسولین با تبلور در حضور نمک روی انجام می شود. این اختراع می تواند روند دستیابی به انسولین انسانی ژنتیکی انسانی را کاهش داده و بازده آن را افزایش دهد.
این اختراع مربوط به زمینه بیوتکنولوژی و به ویژه تولید انسولین انسانی ژنتیکی برای تولید داروهای مورد استفاده در معالجه دیابت است.
با توجه به دستاوردهای اصلی دیابولوژیولوژی مدرن و توصیه های سازمان بهداشت جهانی ، کشورهای اروپایی تا سال 2001 انتقال به استفاده از انسولین انسانی را کامل کردند. در این راستا ، توسعه روشهای تولید انسولین با استفاده از روشهای فناوری نوترکیب DNA یک کار فوری است.
یک روش شناخته شده برای تولید انسولین انسانی ژنتیکی ، که شامل کشت یک سویه تولید کننده E. coli است که پروینسولین تولید می کند ، حاوی یک توالی از دو حوزه اتصال IgG مصنوعی پروتئین استافیلوکوکی A است.
این روش شامل از بین بردن سلولهای باکتریایی ، بدست آوردن گنجاندن برج ثوروس حاوی پروینسولین ، انحلال گنجاندن برج ثوروس ، سولفیتولیز اکسیداتیو پروینسولین ، تجدید ساختار آن ، خالص سازی پروتئین مجدد با استفاده از کروماتوگرافی میل ترکیبی ، برش پروینسولین با آنزیم های پروتئولیتیک (تریپسین و کربوکسیپپتیداز B) و تصفیه نهایی نهایی کروماتوگرافی (Nilson J. ، Jonasson P.، Samuelsson E.، Stahl S.، Uhlen M. "تولید یکپارچه انسولین انسانی و پپتید C آن" ، مجله بیوتکنولوژی ، 1996 ، نسخه 48 ، صص 241-250) .
مضرات این روش هزینه بالای محصول و استفاده در تولید مواد شوینده انسولین است که ممکن است در محصول مورد نظر وجود داشته باشد.
یک روش شناخته شده برای تولید انسولین انسانی با ژنتیک ، که شامل کشت سلول های فشار دهنده تولید کننده E. است.
Coli DN5 a / pVK100 ، سلولهای باکتریایی را با تجزیه اولتراسونیک از بین می برد ، اجسام جداکننده جداگانه حاوی پروتئین ترکیبی از ناخالصی های محلول در آب توسط سانتریفیوژ ، اجساد ورود را درون یک بافر حاوی 8 M اوره ، 1 میلی متر دیثیتروتیتول ، 0.1 M Tris-HCl حل می کنند. pH 8.0 ، به مدت 12-16 ساعت.
ناخالصی های نامحلول توسط سانتریفیوژ برداشته می شوند ، پس از آن غلظت دییتیوتریتول به 10 میلی متر افزایش می یابد و پیوندهای دی سولفید در دمای 37 درجه سانتیگراد به مدت 1 ساعت احیا می شود. محلول 5 بار با آب سرد رقیق شد ، در pH 4.5 تنظیم شد و به مدت 2 ساعت در 4 درجه سانتیگراد انکوبه شد تا رسوب تشکیل شود.
رسوب حاوی پروتئین ترکیبی با سانتریفیوژ جدا شد و دوباره تجدید مجدد ، به سرعت در آب سرد با pH 10-12 حل شد ، پس از آن با 10 میلی متر بافر گلیسین ، pH 10.8 رقیق شد و در شب 4 درجه سانتیگراد نگهداری شد. پس از اولترافیلتراسیون ، محلول به یک ژل فیلتراسیون در یک ستون G-50 Sephadex قرار گرفت و با 10 میلی متر بافر گلیسین شسته شد.
کسرهای حاوی پروتئین فیوژن جمع آوری ، تصفیه نشده و یخ زده می شوند. پروتئین فیوژن حاصل در 0.08 M بافر Tris-HCl با pH 7.5 به غلظت 10 میلی گرم در میلی لیتر حل می شود و همزمان با تریپسین و کربوکسی پپتیداز B (نسبت کربوکسی پپتیداز B: تریپسین: پروتئین فیوژن 0.3: 1: 10) در 37 حل می شود. 30 درجه سانتیگراد.
سپس ایزوپروپانول را به 40٪ اضافه کنید. این مخلوط بر روی ستون DEAE-Sephadex A-25 کروماتوگرافی شده و با 0.05 M بافر Tris-HCl ، pH 7.5 با 40٪ ایزوپروپانول با گرادیان خطی از کلرید سدیم از 0 تا 1/0 متر استخراج می شود و پس از حذف ایزوپروپانول ، غلظت کلرید سدیم تا 25٪ افزایش یابد ، pH را به 2.0 تغییر دهید و رسوب انسولین را جمع کنید.
(Chen J.-Q.، Zhang H.-T.، Hu M.-N.، Tang J.-G.) ، "تولید انسولین انسانی در یک سیستم E. coli با prinsulin met-lys-انسانی به عنوان بیان پیشرو "بیوشیمی کاربردی و بیوتکنولوژی کاربردی ، 1995 ، صفحه 55 ، ص 5-15).
مضرات این روش شامل استفاده از فیلتراسیون ژل در مراحل اولیه است که به مقادیر قابل توجهی از سوربنت و تعداد زیادی آنزیم مورد استفاده در شکاف پروتئین ترکیبی احتیاج دارد.
یک روش شناخته شده برای تولید انسولین انسانی ژنتیکی از جمله کشت یک سویه سازنده Escherichia coli JM109 / pPINS07 ، از بین بردن سلولهای باکتریایی با تجزیه ، جدا کردن اجسام ورود به محتوی پروتئین ترکیبی ، حل آنها در بافر حاوی اوره و دیتیوتریتول ، اصلاح و تصفیه پروتئین ترمیم شده بارش ترکیبات ناخالصی در 40٪ ایزوپروپانول و به دنبال آن کروماتوگرافی روی KM-seararose ، شکاف پی در پی آن با تریپسین و کربوکسی پپتیداز B ، در حالی که محصولات تریپسینولیز بر روی SP-Sepharose کروماتوگرافی شده است ، با بافر استات آمونیوم 0.03-0.1 میلی گرم pH حاوی pH 5.0-6.0 حاوی 6 M اوره ، با شستشوی پروتئین با یک شیب خطی کلرید سدیم از 0 تا 0.5 M در ابتدا تعادل می یابد. بافر ، و کسر انسولین به دست آمده پس از جدا شدن با کربوکسی پپتیداز B با استفاده از کروماتوگرافی مایع با کارایی بالا در فاز معکوس (RP HPLC) و پس از آن با فیلتراسیون ژل خالص شد (پات. RF شماره 2141531 ، MKI C12P 21/02 ، انتشار). 1999)
از مضرات این روش استفاده از مقادیر قابل توجهی اوره و حلالهای آلی در مرحله تصفیه پروتئین ترکیبی است.
متخصص دیابت

قبل از استفاده از انسولین ، امید به زندگی بیمار مبتلا به دیابت بیشتر از 10 سال نبود. اختراع این دارو میلیون ها بیمار را نجات داده است. انسولین مهندسی ژنتیک بشر آخرین پیشرفت در علم است.
نتیجه سالها کار سخت
قبل از اختراع مهندسی ژنتیک (نوترکیب) آماده سازی ، انسولین از لوزالمعده گاو و خوک ها جدا می شد.
تفاوت بین انسولین خوک و انسان تنها یک اسید آمینه است
مضرات این روش در تهیه دارو:
- پیچیدگی ذخیره و حمل مواد اولیه بیولوژیکی ،
- کمبود دام
- مشکلات مربوط به تخصیص و پاکسازی هورمون پانکراس ،
- خطر بالای واکنشهای آلرژیک
با سنتز انسولین طبیعی انسان در بیوراکتور در سال 1982 ، دوره جدید بیوتکنولوژی آغاز شد. اگر در سحر انسولین درمانی ، هدف دانشمندان فقط بقای بیمار بود ، در زمان ما تولید داروهای جدید با هدف دستیابی به جبران پایدار بیماری است. هدف اصلی تحقیقات علمی ارتقاء کیفیت زندگی بیمار مبتلا به دیابت است.
فناوری مدرن
بسته به روش تهیه انواع دارو:
| نوترکیب مهندسی ژنتیک | برای تولید ، از یک E. coli اصلاح شده ژنتیکی استفاده می شود.
| مورد علاقه متخصصان ژنتیک E. coli است |
| اصلاح شده ژنتیکی | ماده شروع آن انسولین خوک است. با روش مهندسی ژنتیک اصلاح می شود. | ساختار هورمون |
| مصنوعی | یک داروی سنتز شده مصنوعی ، در ترکیب آن با انسولین انسانی کاملاً یکسان است. | تولید دارو |
بعد از تجویز دارو چه اتفاقی در بدن می افتد؟
انسولین با گیرنده غشای سلولی متصل می شود و مجموعه ای را تشکیل می دهد که مراحل زیر را انجام می دهد:
- حمل و نقل داخل سلولی گلوکز را بهبود می بخشد و جذب آن را تسهیل می کند.
- ترشح آنزیم هایی که در پردازش گلوکز نقش دارند را ارتقا می بخشد.
- میزان تشکیل گلیکوژن در کبد را کاهش می دهد.
- متابولیسم چربی و پروتئین را تحریک می کند.
در مورد تجویز زیر جلدی ، انسولین از 20-25 دقیقه شروع به فعالیت می کند. مدت زمان مصرف دارو از 5 تا 8 ساعت است. بیشتر توسط آنزیم انسولیناز بریده می شود و در ادرار دفع می شود. این دارو از جفت عبور نمی کند و به شیر مادر منتقل نمی شود.
چه زمانی انسولین مهندسی ژنتیک تجویز می شود؟
در صورت نیاز به کمک فوری
انسولین مهندسی ژنتیکی انسانی در موارد زیر استفاده می شود:
- دیابت نوع 1 یا نوع 2. این دارو به عنوان یک درمان مستقل یا همراه با سایر داروها استفاده می شود.
- با مقاومت در برابر عوامل هیپوگلیسمی خوراکی.
- با دیابت در زنان باردار.
- در صورت بروز عوارض ناشی از کلیه و کبد.
- هنگام تغییر به انسولین طولانی مدت.
- در دوره قبل از عمل
- در مورد شرایط تهدید کننده زندگی (کما هایپراسمولار یا کتواسیدوتیک).
- در مواقع اضطراری (قبل از زایمان ، با جراحات).
- در صورت وجود ضایعات پوستی دیستروفیک (زخم ، فورونکولوز) وجود دارد.
- درمان دیابت در پس زمینه عفونت.
انسولین مهندسی ژنتیک انسان به خوبی تحمل می شود و باعث ایجاد واکنش های آلرژیک نمی شود ، زیرا با هورمون طبیعی کاملاً یکسان است.
نظارت مداوم مهم است!
تجویز دارو در موارد زیر ممنوع است:
- کاهش قند خون
- حساسیت به دارو
در روزهای اول پس از تعیین وقت دارویی ، نظارت دقیق بر بیمار ضروری است.
عوارض جانبی
Urticaria Danger! ورم کوینکی!
در موارد نادر ، هنگام استفاده از انسولین ، عوارض زیر وجود دارد:
- واکنشهای آلرژیک (کهیر ، ادم کوینکی ، خارش پوست) ،
- کاهش شدید قند خون (به دلیل رد دارو توسط بدن یا در صورت درگیری ایمونولوژیکی) ایجاد می شود ،
- اختلال آگاهی
- در موارد شدید ، ایجاد کما هیپوگلیسمی ممکن است ،
- تشنگی ، خشکی دهان ، بی حالی ، بی اشتهایی ،
- هایپرگلیسمی (هنگام استفاده از دارو در برابر پس زمینه عفونت یا تب) ،
- قرمزی صورت
- واکنشهای موضعی در منطقه تجویز (سوزش ، خارش ، آتروفی یا تکثیر چربی زیر جلدی).
بعضی اوقات سازگاری با دارو با اختلالاتی مانند تورم و نقص بینایی همراه است. این تظاهرات معمولاً بعد از چند هفته از بین می روند.
چگونه انسولین مهندسی ژنتیک را در داروخانه پیدا کنیم؟
این دارو به صورت یک راه حل برای تجویز تزریقی در دسترس است:
| "بیوسولین" | میانگین مدت زمان عمل |
| بازیگر | انسولین کوتاه مدت |
| جنسولین | آماده سازی دوتایی (ترکیبی از انسولین های کوتاه و متوسط) |
| رینسولین | اثر سریع |
| هومالوگ | از قلم سرنگ برای تجویز دارو استفاده می شود. |
انتخاب یک داروی انسولین با در نظر گرفتن خصوصیات فردی بیمار دشوار نیست.
شرایط استفاده
بیشتر اوقات ، از تزریق زیر جلدی انسولین استفاده می شود.
در موارد فوری ، دارو به صورت داخل وریدی تجویز می شود.
در شرایط شدید بیمار
حتی یک فرد دیابتی با تجربه می تواند هنگام استفاده از دارو اشتباه کند.
برای جلوگیری از عوارض ، لازم است:
- قبل از استفاده ، تاریخ انقضاء دارو را بررسی کنید.
- توصیه های مربوط به ذخیره سازی را رعایت کنید: ویال های یدکی باید در یخچال نگهداری شوند. ویال توسعه یافته می تواند در دمای اتاق در مکانی تاریک نگهداری شود.
- حتما دوز صحیح را به خاطر بسپارید: تجویز پزشک را دوباره بخوانید.
- قبل از تزریق ، حتما هوا را از سرنگ خون بگیرید.
- پوست باید تمیز باشد ، اما استفاده از الکل برای پردازش نامطلوب است ، زیرا اثر بخشی دارو را کاهش می دهد.
- بهترین مکان را برای تزریق انتخاب کنید. هنگامی که زیر پوست شکم معرفی شود ، دارو سریعتر عمل می کند. کندتر انسولین هنگام وارد شدن به چین یا شانه گلوتئال.
- از کل سطح (پیشگیری از عوارض موضعی) استفاده کنید. فاصله بین تزریق ها باید حداقل 2 سانتی متر باشد.
- پوست را در چین و چروک بزنید تا خطر ابتلا به عضله کاهش یابد.
- سرنگ را زیر پوست با زاویه تزریق کنید تا دارو نشت نکند.
- در صورت تزریق به معده ، انسولین کوتاه مدت 20 دقیقه قبل از غذا تجویز می شود. در صورت انتخاب شانه یا باسن - سی دقیقه قبل از غذا.
ترکیب با داروهای دیگر
غالباً با دیابت ، بیمار داروهای مختلفی مصرف می کند. این ترکیب با سایر داروها می تواند بر اثر درمانی انسولین مهندسی ژنتیک تأثیر بگذارد.
برای جلوگیری از عوارض ، باید بدانید:
| با کاهش قند خون اثر انسولین مهندسی ژنتیک را افزایش دهید |
| یک داروی محبوب که در درمان عفونتهای ادراری داکسی سایکلین استفاده می شود |
| عمل انسولین را کاهش دهید |
| توجه کنید دیورتیک |
مصرف بیش از حد
در برخی موارد ، تجویز انسولین منجر به کاهش ناگهانی قند خون می شود. این مشکل اغلب به دلیل انتخاب نادرست دوز ایجاد می شود.
علائم اولیه هیپوگلیسمی:
- ضعف
- رنگ پریدگی پوست
- حالت اضطراب
- سرگیجه
- بی نظمی
- بی حسی بازوها ، پاها ، زبان و لب ها ،
- لرزش اندام
- عرق سرد
- احساس گرسنگی شدید
- سردرد
لرزیدن ؛ وخیم شدن ناگهانی در بهزیستی
اگر متوجه این علائم شدید ، باید به سرعت چیزی را حاوی کربوهیدرات هایی که به راحتی قابل هضم هستند بخورید. این می تواند کوکی ها ، آب نبات ها ، یک تکه شکر یا نان سفید باشد. چای شیرین در چنین شرایطی کمک می کند.
اگر شرایط بدتر شود ، باید با آمبولانس تماس بگیرید. هیپوگلیسمی ممکن است منجر به اغما یا مرگ بیمار شود.
آیا انسولین نوترکیب خطرناک است؟
سلام انسولین نوترکیب هیچ تفاوتی با طبیعی ندارد. برای به دست آوردن آن از باکتریهای اصلاح شده ژنتیکی استفاده می شود.
با استفاده از فن آوری های مهندسی ژنتیک ، یک DNA نوترکیب حاوی ژن انسولین در سلول E. coli کاشته می شود. ارگانیسم های اصلاح شده ژنتیکی ضرب شده و هورمون تولید می کنند. این دارو بسیار مؤثر است و درجه خلوص بالایی دارد.
انسولین قسمت دوم تولید انسولین میکروبیولوژیکی

جزء میل - به طور قابل توجهی جداسازی پروتئین ترکیبی را تسهیل می کند.
علاوه بر این ، هر دو این مؤلفه می توانند همزمان در ترکیب پروتئین ترکیبی حضور داشته باشند.
علاوه بر این ، هنگام ایجاد پروتئین های ترکیبی ، می توان از اصل چند بعدی استفاده کرد (یعنی چندین نسخه از پلی پپتید هدف در پروتئین ترکیبی موجود است) ، که می تواند عملکرد محصول مورد نظر را به میزان قابل توجهی افزایش دهد.
2 بیان پروینسولین در سلولهای E. coli ..
در این کار ، نویسندگان از کرنش JM 109 N1864 با یک توالی نوکلئوتیدی درج شده در پلاسمید به بیان پروتئین ترکیبی استفاده کردند که از پروینسولین خطی و قطعه ای از پروتئین استافیلوکوکوس اورئوس A متصل به انتهای N آن از طریق مانده متیونین تشکیل شده است.
کشت زیست توده اشباع شده سلولهای سویه نوترکیب ، آغاز تولید پروتئین ترکیبی را فراهم می کند ، جداسازی و تبدیل پی در پی آن در لوله منجر به انسولین می شود.
گروه دیگری از محققان ، یک پروتئین نوترکیب در سیستم بیان باکتریایی یک همجوشی متشکل از پروینسولین انسانی و یک دم پلی اتیستین متصل به آن از طریق یک مانده متیونین دریافت کردند. با استفاده از کروماتوگرافی کلات روی ستونهای Ni-agarose از بدن درج جدا شد و با برمید سیانوژن هضم شد.
نقشه برداری و تجزیه و تحلیل طیف سنجی جرمی از پروینسولین به دست آمده خالص شده توسط کروماتوگرافی تبادل یونی بر روی رزین تبادل آنیون و RP (فاز معکوس) HPLC (کروماتوگرافی مایع با کارایی بالا) وجود پل های دی سولفید مربوط به پل های دی سولفید پروتئینولین بومی انسان را نشان داد. در این مقاله به تهیه یک روش جدید و بهبود یافته برای تولید انسولین انسانی توسط مهندسی ژنتیک در سلولهای پروکاریوتی پرداخته شده است. نویسندگان دریافتند که انسولین حاصل در ساختار و فعالیت بیولوژیکی آن با هورمون جدا شده از پانکراس یکسان است.
اخیراً توجه ساده ای به ساده سازی روش تولید انسولین نوترکیب توسط مهندسی ژنتیک شده است. بنابراین ، نویسندگان پروتئین فیوژن متشکل از پپتید رهبر از اینترلوکین 2 متصل به N- پایانه پروینسولین را از طریق مانده لیزین دریافت کردند.
پروتئین به طور مؤثر بیان شده و در بدن ورود به سیستم بومی سازی شد. پس از جداسازی ، پروتئین با تریپسین هضم شد تا انسولین و پپتید C تولید کند. گروه دیگری از محققان به همین روش عمل کردند.
پروتئین فیوژن متشکل از پروینسولین و دو حوزه مصنوعی استافیلوکوک A پروتئین اتصال IgG در بدن ورود به مطالعه بومی سازی شد ، اما سطح بیان بالاتری دارد. پروتئین توسط کروماتوگرافی میل ترکیبی با استفاده از IgG جدا شد و با تریپسین و کربوکسیپپتیداز B پردازش شد.
انسولین حاصل و پپتید C با RP HPLC خالص شد. هنگام ایجاد ساختارهای ذوب شده ، نسبت جرم پروتئین حامل و پلی پپتید هدف بسیار قابل توجه است.
بنابراین ، این کار ساخت و ساز سازه های همجوشی را توصیف می کند ، که در آن از پروتئین متصل کننده آلبومین سرم انسانی به عنوان یک پلی پپتید حامل استفاده شده است. یک ، سه و هفت پپتید C به آن وصل شد.
C- پپتیدها بر اساس دم سر با استفاده از فاصله دهنده های اسید آمینه حامل محل محدودیت Sfi I و دو باقیمانده آرژینین در ابتدا و انتهای فضا برای تقسیم پروتئین بعدی با تریپسین متصل شدند. HPLC محصولات شکاف نشان داد که شکاف C- پپتید کمی است ، و این به استفاده از ژنهای مصنوعی مولتی متر برای دستیابی به پلی پپتیدهای هدف در مقیاس صنعتی اجازه می دهد.
در این مقاله آماده سازی جهش پروینسولین ، که شامل جایگزینی Arg32Tyr است ، توصیف می شود. هنگامی که این پروتئین با تریپسین و کربوکسی پپتیداز B به هم ریخته شد ، انسولین بومی و یک پپتید C حاوی مانده تیروزین تشکیل شد. دوم ، پس از برچسب زدن به 125I ، به طور فعال در رادیو ایمونواسی استفاده می شود. 3 تصفیه انسولین.
انسولین در نظر گرفته شده برای ساخت داروها باید از خلوص بالایی برخوردار باشد. بنابراین ، یک کنترل بسیار مؤثر بر خلوص محصولات به دست آمده در هر مرحله از تولید ضروری است. پیش از این ، از RP و IO (تبادل یونی) HPLC برای توصیف پروینسولین-S-سولفونات ، پروینسولین ، A- و B- زنجیره های فردی و S-sulfonates آنها استفاده می شد.
توجه ویژه ای نیز به مشتقات انسولین فلورسنت شده است. در این کار ، نویسندگان کاربردی بودن و اطلاع رسانی روشهای کروماتوگرافی در تجزیه و تحلیل محصولات در کلیه مراحل تولید انسولین انسانی را مورد بررسی قرار داده و برنامه ای از عملیات کروماتوگرافی تهیه کرده اند تا بطور مؤثر و جداگانه و توصیف کننده محصولات حاصل از آن مشخص شوند.
علاوه بر این ، رویکردهایی برای خودکارسازی و تسریع فرآیندهای تعیین خلوص و کمیت انسولین ایجاد شده است.
در این مقاله مطالعات مربوط به امکان استفاده از کروماتوگرافی مایع RP با تشخیص الکتروشیمیایی برای تعیین انسولین ارائه شده است ، و یک روش برای تعیین انسولین جدا شده از جزایر لانگرهان با کروماتوگرافی ایمونوافینتی با تشخیص طیف سنجی تهیه شده است.
در این کار ، امکان استفاده از میکروسیدان سریع انسولین با استفاده از الکتروفورز مویرگی با تشخیص فلورسانس لیزری مورد بررسی قرار گرفت. این تجزیه و تحلیل با اضافه کردن مقدار مشخصی از انسولین با فنیلیزوتیوسیانات (FITC) و یک قطعه Fab از آنتی بادی های انسولین مونوکلونال به نمونه به مقدار نمونه انجام می شود. انسولین های برچسب خورده و منظم با رقابت فاب واکنش نشان می دهند. انسولین با FITZ و مجموعه آن با Fab در 30 ثانیه از هم جدا می شوند.
اخیراً تعداد زیادی اثر به بهبود روش های تولید انسولین و همچنین ایجاد فرم های دوز بر اساس آن اختصاص یافته است.
به عنوان مثال ، در آمریكا ، آنالوگهای انسولین مخصوص سلولهای کبدی به دلیل معرفی مواد باقیمانده اسیدآمینه در موقعیتهای 13-15 و 19 زنجیره A و در موقعیت 16 زنجیره B ثبت شده و از نظر ساختاری با هورمون طبیعی متفاوت است.
آنالوگ های به دست آمده در انواع مختلف تزریقی (داخل وریدی ، عضلانی ، زیر جلدی) ، دوز داخل رحمی یا کاشت به شکل کپسول های خاص در درمان دیابت استفاده می شود. از اهمیت ویژه ای ایجاد فرم های دوز تجویز شده بدون تزریق است.
در این مقاله از ایجاد یک سیستم ماکرومولکولی برای تجویز خوراکی ، که انسولین در حجم هیدروژل پلیمری اصلاح شده با مهارکننده های آنزیم پروتئولیتیک است ، گزارش شده است. اثربخشی چنین دارویی 70-80٪ از اثر بخشی انسولین بومی به صورت زیر جلدی معرفی شده است.
در یک کار دیگر ، یک داروی با جوجه کشی یک مرحله ای انسولین با گلبول های قرمز ، که با نسبت 1-4: 100 و در حضور ماده اتصال دهنده گرفته می شود ، بدست می آید.نویسندگان دریافت دارویی را با فعالیت 1000 واحد در گرم ، حفظ كامل فعالیت پس از تجویز خوراكی و ذخیره چندین سال به صورت لیوفیلیزه گزارش می كنند.
علاوه بر ایجاد داروهای جدید و فرم های دوز مبتنی بر انسولین ، رویکردهای جدیدی برای حل مشکل دیابت ایجاد شده است.
بنابراین ، نویسندگان پروتئین حمل و نقل گلوکز GLUT2 cDNA که قبلاً با cDNA انسولین به اندازه کامل سلولهای انسولین HEP G2 به طور پایدار منتقل شده بودند ، را ترشح کردند.
در کلون های HEP G2 Insgl به دست آمده ، گلوکز نزدیک به ترشح انسولین طبیعی را تحریک می کند و واکنش ترشحی سایر محرکهای ترشح را تقویت می کند.
تحت میکروسکوپ ایمونوالکترون ، گرانولهای حاوی انسولین در سلولهایی یافت شد که از نظر مورفولوژیکی شبیه به گرانولها در سلولهای B جزایر لانگرهان هستند. احتمال استفاده از "سلول B- مصنوعی" به دست آمده با روشهای مهندسی ژنتیک برای درمان دیابت نوع 1 در حال حاضر مورد بحث جدی است.
در کنار حل مشکلات عملی ، مکانیسم های عملکرد انسولین و همچنین روابط ساختاری و عملکردی در این مولکول مورد بررسی قرار می گیرد. یكی از روشهای تحقیق ایجاد مشتقات مختلف انسولین و بررسی خصوصیات فیزیكوشیمیایی و ایمونولوژیك آنها 23 ، 24 است.
همانطور که در بالا گفته شد ، تعدادی از روش های تولید انسولین بر اساس تولید این هورمون به شکل پیش ساز (پروینسولین) انجام می شود و پس از آن شکاف آنزیمی به انسولین و پپتید C انجام می شود. در حال حاضر وجود فعالیت بیولوژیکی برای پپتید C نشان داده شده است که باعث می شود در کنار انسولین استفاده از آن برای اهداف درمانی انجام شود.
در مقاله های بعدی این مجموعه ، خصوصیات فیزیکی و بیولوژیکی پپتید C و همچنین روش های تهیه آن مورد بررسی قرار خواهد گرفت.
بیوتکنولوژی در ساخت داروها
تحولات برای به دست آوردن نسخه 20K از STGh مورد توجه است. یک کار امیدوارکننده ، بدست آوردن و مطالعه نه تنها اشکال مختلف STH ، بلکه بی تحرک STH به منظور به دست آوردن عملکرد طولانی مدت هورمون است. یک روش اصلی برای بدست آوردن STHch بی حرکت با یک عمل طولانی مدت ایجاد شده است.
به موازات تولید STH ، یک فناوری یکپارچه اصلی برای تولید هورمونهای آدنوهیپوفیز ، از جمله کلیه گونه های خاص ، و برخی از اصلاحات آنها از GST ایجاد شد. اجرای یک برنامه هدفمند برای ایجاد یک داروی درمانی STH (سوماتوژن) که توسط مهندسی ژنتیک بدست آمده از اهمیت ویژه ای برخوردار است.
تجربه بالینی نشان داده است كه بهینه سازی درمان لكنت ، بهتر است در زرادخانه چندین داروی مشابه دارویی مشابه به دست آمده توسط فن آوری های مختلف یا حتی روش ها (MF ، Ausomatin ، Somatogen) وجود داشته باشد.
درمان طولانی مدت (سالها) با یک آماده سازی STHh باعث کاهش حساسیت در بدن می شود.
تا حدودی ، این ممکن است نتیجه تشکیل آنتی بادی ها باشد ، اما دلیل اصلی را باید در سطح گیرنده ها و پردازش هورمون جستجو کرد.
کار با GST و همچنین مطالعات جامع در مورد هورمونهای ترشح شده و اشکال مختلف آنها باعث می شود سیستمهای ایجاد شده توسط طبیعت مورد مطالعه قرار گرفته و آنها را بهتر بشناسیم. وجود اشکال مختلف بومی STH در بدن نشانگر امکان سنجی و استفاده احتمالی آنها ، به عنوان مثال در یک کلینیک است.
هنگام ایجاد آماده سازی جدید STHch ، قبل از هر چیز لازم است که روی اشکال طبیعی بومی هورمون تمرکز شود و در صورت لزوم ، آنها را با مهندسی ژنتیک مقیاس گذاری کنید ، همانطور که با مونومر STHch انجام می شود.
در تولید فرآورده های STHch از GST ، یک فناوری جامع صنعتی برای تولید هورمون های دیگر آدنوهیپوفیز (LGH ، FSHch ، TTGch و دیگران) با موفقیت اجرا می شود. لازم است با معرفی روشهای پیشرفته جدید (کروماتوگرافی میل و غیره) تولید بهینه شود.
) ، با استفاده از فناوری یکپارچه ، هورمونهای بسیار خالص دریافت کنید.
لازم است تولید و استفاده از مجموعه هایی از ایمنی بدن ، تجزیه و تحلیل هورمونهای آدنوهیپوفیز جهت تشخیص و بیوتکنولوژی ، گسترش تولید تنظیم شده آنتی بادی های استاندارد از مقیاس های مختلف ، ایجاد ترکیبات جدید STHch از جمله بی تحرکی ضروری باشد.
این واقعیت که STH بر متابولیسم پروتئین ، چربی و مواد معدنی تأثیر می گذارد ، در سطح سلول بدون اندام هدف عمل می کند و آنابولیک است ، چشم انداز بسیار خوبی برای استفاده از آن برای تحریک فرآیندهای ترمیم و درمان بیماری های مختلف ایجاد می کند. مطالعه گسترده تر در مورد این موضوعات و همچنین امکان استفاده از اشکال و انواع مختلف اصلاح شده STGch ، یک کار فوری و امیدوار کننده است.
به دست آوردن انسولین در بیوتکنولوژی
انسولین ، هورمون پپتید جزایر لانگرهانس لوزالمعده ، درمان اصلی برای دیابت است. این بیماری در اثر کمبود انسولین ایجاد می شود و با افزایش قند خون ظاهر می شود. تا همین اواخر انسولین از لوزالمعده یک گاو و خوک به دست می آمد.
این دارو از نظر انسولین انسانی با 1-3 اسید آمینه جایگزین می شود ، به طوری که تهدیدی از واکنش های آلرژیک به ویژه در کودکان وجود دارد. استفاده گسترده از انسولین درمانی به دلیل هزینه بالا و منابع محدود آن محدود شده است.
با اصلاح شیمیایی ، انسولین از حیوانات از انسان قابل تشخیص نیست ، اما این به معنای افزایش اضافی قیمت محصول است.
از سال 1982 ، الی لیلی تولید انسولین مهندسی ژنتیک را بر اساس سنتز جداگانه زنجیره های E. coli A و B تولید می کند. هزینه محصول بسیار کاهش یافته است ، انسولین حاصل با انسان یکسان است. از سال 1980 ، در مطبوعات گزارشی در مورد کلونینگ ژن پروینسولین وجود دارد ، یک پیش ساز هورمون که با پروتئولیز محدود به یک فرم بالغ تبدیل می شود.
از فناوری کپسولی برای درمان دیابت نیز استفاده می شود: سلول های لوزالمعده در یک کپسول ، که یک بار وارد بدن بیمار می شوند ، در طول سال انسولین تولید می کنند.
ژنتیک یکپارچه هورمون های تحریک کننده فولیکول و لوتئین کننده را راه اندازی کرده است. این پپتیدها از دو زیر واحد تشکیل شده اند. در دستور کار سنتز صنعتی هورمون های الیگوپپتید سیستم عصبی - آنکفالین ها ، ساخته شده از 5 اسید آمینه باقی مانده ، و اندورفین ها ، آنالوگ های مورفین است.
این پپتیدها وقتی به صورت عقلانی مورد استفاده قرار می گیرند ، درد را تسکین می دهند ، خلق و خوی خوبی ایجاد می کنند ، ظرفیت کاری را افزایش می دهند ، توجه را به خود معطوف می کنند ، باعث بهبود حافظه می شوند و خواب و بیداری را مرتب می کنند.
نمونه ای از کاربرد موفق روشهای مهندسی ژنتیک سنتز p-endorphin با استفاده از فناوری پروتئین ترکیبی است که در بالا برای هورمون پپتید دیگری ، سوماتوستاتین توضیح داده شده است.
روشهای تولید انسولین انسانی:
از نظر تاریخی ، اولین راه برای به دست آوردن انسولین برای اهداف درمانی ، جداسازی آنالوگ های این هورمون از منابع طبیعی (جزایر پانکراس گاو و خوک) است.
در دهه 20 قرن گذشته مشخص شد که انسولین های گاو و گوشت خوک (که به ساختار و دنباله اسیدهای آمینه به انسولین انسانی نزدیک هستند) فعالیتی در بدن انسان دارند که با انسولین انسانی قابل مقایسه است. پس از آن از انسولین گاو یا خوک برای معالجه بیماران دیابت نوع I استفاده شد.
با این حال ، پس از مدتی نشان داده شد كه در بعضی موارد آنتی بادی های انسولین گاو و بز گوشت خوك در بدن انسان تجمع می یابند ، در نتیجه اثر آنها را نفی می كنند.
از طرف دیگر ، یکی از مزایای این روش به دست آوردن انسولین ، در دسترس بودن مواد اولیه است (انسولین گاو و خوک را به راحتی در مقادیر زیادی می توان به دست آورد) ، که نقش تعیین کننده ای در ساخت اولین روش برای تولید انسولین انسانی داشت.این روش نیمه مصنوعی نامیده می شود.
در این روش تولید انسولین انسانی از انسولین خوک به عنوان ماده اولیه خوراک استفاده شده است. اکتاپپتید C- ترمینال زنجیره B از انسولین خوک خالص جدا شد ، و پس از آن اکتاپپتید C- ترمینال انسولین انسانی سنتز شد.
سپس به صورت شیمیایی متصل شد ، گروههای محافظ برداشته شد و انسولین حاصل خالص شد. هنگام آزمایش این روش به دست آوردن انسولین ، هویت کامل هورمون بدست آمده به انسولین انسانی نشان داده شد.
ضرر اصلی این روش ، هزینه بالای انسولین حاصل از آن است (حتی در حال حاضر ، سنتز شیمیایی اکتاپپتید یک لذت گران به خصوص در مقیاس صنعتی است).
در حال حاضر ، انسولین انسانی عمدتاً از دو طریق بدست می آید: با اصلاح انسولین خوک به روش سنتزی - آنزیمی و به روش مهندسی ژنتیک.
در حالت اول ، این روش مبتنی بر این واقعیت است که انسولین خوک با انسولین انسانی در یک تعویض در C- پایانه زنجیره Ala30Thr B متفاوت است.
جایگزینی آلانین با ترئونین با استفاده از آنزیم کاتالیز شده آلانین و اضافه کردن مانده ترئونین به جای آن توسط گروه کربوکسی محافظت می شود ، که در مقدار زیادی در مخلوط واکنش موجود است. پس از جدا شدن از گروه محافظ O-tert-butyl ، انسولین انسانی بدست می آید.
انسولین اولین پروتئین است که با استفاده از فناوری DNA نوترکیب به اهداف تجاری بدست آمد. دو روش اصلی برای تولید انسولین انسانی ژنتیکی وجود دارد.
در حالت اول ، جداگانه (سویه های تولید کننده مختلف) برای هر دو زنجیره به دست می آید که به دنبال آن تاشو مولکول (تشکیل پل های دی سولفید) و جداسازی ایزوفرم ها است.
در مرحله دوم ، تولید به صورت پیش ساز (پروینسولین) و به دنبال آن هضم آنزیمی با تریپسین و کربوکسی پپتیداز B به شکل فعال هورمون.
در حال حاضر بیشترین مطلوب برای بدست آوردن انسولین به صورت پیش ساز است که باعث بسته شدن صحیح پل های دی سولفید می شود (در صورت تهیه جداگانه زنجیرها ، چرخه های متوالی دناتوراسیون ، جداسازی ایزوفرم و تجدید حیات انجام می شود).
با هر دو روش ، هر دو به طور جداگانه می توانند اجزای شروع (A- و B- زنجیره ها یا پروینسولین) و همچنین به عنوان بخشی از پروتئین های ترکیبی را بدست آورند. علاوه بر زنجیره های A و B یا پروینسولین ، پروتئین های ترکیبی ممکن است شامل موارد زیر باشد:
1) پروتئین حامل - تأمین انتقال پروتئین ترکیبی به فضای محیطی سلول یا محیط کشت ،
2) مؤلفه میل - به طور قابل توجهی جداسازی پروتئین ترکیبی را تسهیل می کند.
علاوه بر این ، هر دو این مؤلفه می توانند همزمان در ترکیب پروتئین ترکیبی حضور داشته باشند. علاوه بر این ، هنگام ایجاد پروتئین های ترکیبی ، می توان از اصل چند بعدی استفاده کرد (یعنی چندین نسخه از پلی پپتید هدف در پروتئین ترکیبی موجود است) ، که می تواند عملکرد محصول مورد نظر را به میزان قابل توجهی افزایش دهد.
بیان پروینسولین در سلولهای E. coli ..
Strain JM 109 N1864 با یک توالی نوکلئوتیدی به بیان پروتئین فیوژن ، که از یک پروینسولین خطی و یک قطعه پروتئین A از استافیلوکوکوس اورئوس متصل به انتهای آن از طریق باقیمانده متیونین تشکیل شده است.
کشت زیست توده اشباع شده سلولهای سویه نوترکیب ، آغاز تولید پروتئین ترکیبی را فراهم می کند ، جداسازی و تبدیل پی در پی آن در لوله منجر به انسولین می شود.
گروه دیگری از محققان ، یک پروتئین نوترکیب در سیستم بیان باکتریایی یک همجوشی متشکل از پروینسولین انسانی و یک دم پلی اتیستین متصل به آن از طریق یک مانده متیونین دریافت کردند. با استفاده از کروماتوگرافی کلات روی ستونهای Ni-agarose از بدن درج جدا شد و با برمید سیانوژن هضم شد.
نقشه برداری و تجزیه و تحلیل طیف سنجی جرمی از پروینسولین به دست آمده خالص شده توسط کروماتوگرافی تبادل یونی بر روی رزین تبادل آنیون و RP (فاز معکوس) HPLC (کروماتوگرافی مایع با کارایی بالا) وجود پل های دی سولفید مربوط به پل های دی سولفید پروتئینولین بومی انسان را نشان داد. همچنین ، از ایجاد یک روش جدید و بهبود یافته برای تولید انسولین انسانی توسط مهندسی ژنتیک در سلولهای پروکاریوتی گزارش شده است. نویسندگان دریافتند که انسولین حاصل در ساختار و فعالیت بیولوژیکی آن با هورمون جدا شده از پانکراس یکسان است.
اخیراً توجه ساده ای به ساده سازی روش تولید انسولین نوترکیب توسط مهندسی ژنتیک شده است. بنابراین ، یک پروتئین فیوژن متشکل از پپتید رهبر از اینترلوکین متصل به N- پایانه پروینسولین از طریق مانده لیزین به دست آمد. پروتئین به طور مؤثر بیان شده و در بدن ورود به سیستم بومی سازی شد.
پس از جداسازی ، پروتئین با تریپسین هضم شد تا انسولین و پپتید C تولید کند. گروه دیگری از محققان به همین روش عمل کردند. پروتئین فیوژن متشکل از پروینسولین و دو حوزه مصنوعی استافیلوکوک A پروتئین اتصال IgG در بدن ورود به مطالعه بومی سازی شد ، اما سطح بیان بالاتری دارد.
پروتئین توسط کروماتوگرافی میل ترکیبی IgG جدا شد و با تریپسین و کربوکسیپپتیداز B. هضم شد. انسولین و سی پپتید حاصل از طریق RP HPLC خالص شدند. هنگام ایجاد ساختارهای ذوب شده ، نسبت جرم پروتئین حامل و پلی پپتید هدف بسیار قابل توجه است.
ساخت سازه های فیوژن در جایی توصیف شده است که یک پروتئین اتصال دهنده آلبومین سرم انسانی به عنوان یک پلی پپتید حامل استفاده می شود. یک ، سه و هفت پپتید C به آن وصل شد.
C- پپتیدها بر اساس دم سر با استفاده از فاصله دهنده های اسید آمینه حامل محل محدودیت Sfi I و دو باقیمانده آرژینین در ابتدا و انتهای فضا برای تقسیم پروتئین بعدی با تریپسین متصل شدند. HPLC محصولات شکاف نشان داد که شکاف C- پپتید کمی است ، و این به استفاده از ژنهای مصنوعی مولتی متر برای دستیابی به پلی پپتیدهای هدف در مقیاس صنعتی اجازه می دهد.
به دست آوردن پروینسولین جهش یافته ، که شامل جایگزینی Arg32Tyr بود. هنگامی که این پروتئین با تریپسین و کربوکسی پپتیداز B به هم ریخته شد ، انسولین بومی و یک پپتید C حاوی مانده تیروزین تشکیل شد. دوم ، پس از برچسب زدن به 125I ، به طور فعال در رادیو ایمونواسی استفاده می شود.
انسولین در نظر گرفته شده برای ساخت داروها باید از خلوص بالایی برخوردار باشد. بنابراین ، یک کنترل بسیار مؤثر بر خلوص محصولات به دست آمده در هر مرحله از تولید ضروری است. پیش از این ، از RP و IO (تبادل یونی) HPLC برای توصیف پروینسولین-S-سولفونات ، پروینسولین ، A- و B- زنجیره های فردی و S-sulfonates آنها استفاده می شد.
توجه ویژه ای نیز به مشتقات انسولین فلورسنت شده است. در این کار ، نویسندگان کاربردی بودن و اطلاع رسانی روشهای کروماتوگرافی در تجزیه و تحلیل محصولات در کلیه مراحل تولید انسولین انسانی را مورد بررسی قرار داده و برنامه ای از عملیات کروماتوگرافی تهیه کرده اند تا بطور مؤثر و جداگانه و توصیف کننده محصولات حاصل از آن مشخص شوند.
علاوه بر این ، رویکردهایی برای خودکارسازی و تسریع فرآیندهای تعیین خلوص و کمیت انسولین ایجاد شده است.
مطالعات در مورد امکان استفاده از کروماتوگرافی مایع RP با تشخیص الکتروشیمیایی برای تعیین انسولین گزارش شده است ، و روشی برای تعیین انسولین جدا شده از جزایر لانگرهانس توسط کروماتوگرافی ایمنی اونا با تشخیص طیف سنجی تهیه شده است.
در این کار ، امکان استفاده از میکروسیدان سریع انسولین با استفاده از الکتروفورز مویرگی با تشخیص فلورسانس لیزری مورد بررسی قرار گرفت.این تجزیه و تحلیل با اضافه کردن مقدار مشخصی از انسولین با فنیلیزوتیوسیانات (FITC) و یک قطعه Fab از آنتی بادی های انسولین مونوکلونال به نمونه به مقدار نمونه انجام می شود. انسولین های برچسب خورده و منظم با رقابت فاب واکنش نشان می دهند. انسولین با FITZ و مجموعه آن با Fab در 30 ثانیه از هم جدا می شوند.
انسولین مهندسی ژنتیک

این سؤال که انسولین از چه چیزی ساخته شده است نه تنها برای پزشکان و داروسازان بلکه برای بیماران مبتلا به دیابت و همچنین بستگان و دوستانشان مورد توجه است.
امروزه ، این هورمون منحصر به فرد و بسیار مهم برای سلامتی انسان می تواند از مواد اولیه مختلف با استفاده از فناوری های ویژه توسعه یافته و با دقت آزمایش شده بدست آید. بسته به روش تهیه ، انواع انسولین زیر مشخص می شود:
- گوشت خوک یا گاو ، به عنوان محصول حیوانی نیز خوانده می شود
- خوک بیوسنتز اصلاح شده اصلاح شده است
- مهندسی ژنتیکی یا نوترکیب
- اصلاح شده ژنتیکی
- مصنوعی
انسولین خوک از طولانی ترین زمان برای دیابت استفاده شده است. کاربرد آن در دهه 20 قرن گذشته آغاز شد.
لازم به ذکر است که گوشت خوک یا حیوانات تنها دارویی تا دهه 80 قرن گذشته بود. برای به دست آوردن آن ، از بافت پانکراس حیوانات استفاده می شود.
با این وجود ، به سختی می توان این روش را بهینه یا ساده نامید: کار با مواد اولیه بیولوژیکی همیشه راحت نیست و خود ماده اولیه نیز کافی نیست.
علاوه بر این ، ترکیب انسولین خوک به طور کامل با ترکیب هورمون تولید شده توسط یک فرد سالم مطابقت ندارد: باقیمانده اسیدهای آمینه مختلف در ساختار آنها وجود دارد. لازم به ذکر است که هورمونهای تولید شده از لوزالمعده گاو اختلافات حتی بیشتری دارند که از این رو نمی توان پدیده ای مثبت نامید.
در چنین آماده سازی ، علاوه بر ماده خالص مولکولی خالص ، به اصطلاح پروینسولین همواره حاوی ماده است که با استفاده از روشهای نوین تصفیه جدا نمی شود. این شخص است که اغلب اوقات منبعی از واکنش های آلرژیک می شود ، به ویژه برای کودکان و افراد مسن خطرناک است.
داروخانه ها یک بار دیگر می خواهند از افراد دیابتی پول بگیرند. یک داروی مدرن معقول اروپایی وجود دارد ، اما آنها در مورد آن ساکت هستند. این است
به همین دلیل دانشمندان در سراسر جهان مدتهاست که علاقه دارند ترکیب هورمون تولید شده توسط حیوانات را به طور کامل با هورمونهای لوزالمعده یک فرد سالم سازگار کنند. یک پیشرفت واقعی در فارماکولوژی و درمان دیابت تولید یک داروی نیمه مصنوعی است که با جایگزین کردن اسید آمینه آلانین در آماده سازی حیوانات با ترئونین بدست آمده است.
در عین حال ، یک روش نیمه سنتز برای تولید هورمون مبتنی بر استفاده از داروهای آماده سازی حیوانات است. به عبارت دیگر ، آنها به سادگی تحت اصلاحات قرار می گیرند و با هورمون های تولید شده توسط انسان یکسان می شوند. از جمله مزایای آنها سازگاری با بدن انسان و عدم وجود واکنش های آلرژیک است.
از مضرات این روش می توان به کمبود مواد اولیه و مشکل در کار با مواد بیولوژیکی و همچنین هزینه بالای خود فناوری و داروی حاصل از آن اشاره کرد.
از این نظر بهترین داروی برای درمان دیابت انسولین نوترکیب است که توسط مهندسی ژنتیک به دست می آید.
اتفاقاً غالباً آن را انسولین مهندسی ژنتیک می نامند ، بنابراین روش دریافت آن را نشان می دهد و محصول حاصل آن انسولین انسانی نامیده می شود و از این طریق بر هویت مطلق آن بر هورمون های تولید شده از لوزالمعده یک فرد سالم تأکید می شود.
از جمله مزایای انسولین مهندسی ژنتیک باید به درجه خلوص بالای آن و عدم وجود پروینسولین نیز اشاره کرد ، همچنین این واقعیت را دارد که هیچگونه واکنش آلرژیک ایجاد نمی کند و هیچگونه منع مصرف ندارد.
سؤال متداول قابل درک است: از انسولین نوترکیب دقیقاً چه چیزی ساخته شده است؟ به نظر می رسد که این هورمون توسط سویه های مخمر و همچنین اشرشیاکلی تولید می شود که در یک ماده غذایی خاص قرار می گیرد. علاوه بر این ، مقدار ماده به دست آمده به قدری زیاد است که می توان از مصرف داروهای بدست آمده از اندام حیوانات کاملاً کنار گذاشت.
البته این در مورد E. coli ساده نیست ، بلکه در مورد ژن اصلاح شده و قادر به تولید انسولین مهندسی ژنتیکی محلول در انسان است ، ترکیب و خواص آن دقیقاً مشابه هورمون تولید شده توسط سلولهای پانکراس یک فرد سالم است.
از مزایای انسولین مهندسی ژنتیک نه تنها شباهت مطلق آن با هورمون انسانی ، بلکه سهولت تهیه ، مقدار کافی مواد اولیه و هزینه مقرون به صرفه است.
دانشمندان در سراسر جهان تولید انسولین نوترکیب را یک پیشرفت واقعی در درمان دیابت می دانند. اهمیت این اکتشاف به قدری بزرگ و مهم است که دست کم گرفتن آن دشوار است.
ذکر این نکته به اندازه کافی ساده است که امروزه تقریباً 95٪ از نیاز این هورمون با کمک انسولین ژنتیکی برآورده می شود.
در همین زمان ، هزاران نفر که قبلاً حساسیت به مواد مخدر داشتند ، فرصتی برای یک زندگی عادی دریافت کردند.
31 سال دیابت داشتم. او اکنون سالم است. اما ، این کپسولها برای افراد عادی غیرقابل دسترسی هستند ، آنها مایل به فروش داروخانه نیستند ، برای آنها سودآور نیست.
انسولین مهندسی انسانی چگونه کار می کند
در درمان دیابت نوع 1 از انسولین مهندسی ژنتیک انسانی دو فاز استفاده می شود. در داروخانه ها ، به صورت محلول فروخته می شود و علامت "دوست داشتنی" دارد. اگر داروهای تجویز شده برای دیابتی مناسب نباشد ، نوع دوم بیماری نیز با چنین دارویی قابل درمان است.
از انسولین مهندسی ژنتیکی نیز در صورت داشتن کما دیابتی استفاده می شود. پزشکان غالباً در هنگام تزریق قرص های کاهش قند و رژیم درمانی ، به زنان باردار مبتلا به دیابت قند تزریق می کنند.
به طور کلی ، انسولین های ژنتیکی یا GMO در هنگام زایمان ، هنگامی که تحت عمل جراحی قرار می گیرند ، یا اگر دیابتی به شدت آسیب دیده باشد ، استفاده می شود. این دارو به شما امکان می دهد با خیال راحت به استفاده از هورمون هایی که به سرعت عمل می کنند تغییر دهید.
- قبل از استفاده از مهندسی ژنتیک انسولین بیفازی انسولین ، لازم است که یک آزمایش انجام شود و بدانید که آیا این دارو برای بیمار مناسب است یا خیر. اگر یک فرد دیابتی هیپوگلیسمی را نشان دهد ، استفاده از دارو توصیه نمی شود.
- طرح عمل راه حل این است که انسولین مهندسی ژنتیک با سلول ها در تعامل است و این منجر به تشکیل مجتمع ها می شود. وقتی سلول ها وارد این مجتمع ها می شوند ، تحریک می شوند و فعالانه تر شروع به کار می کنند. در نتیجه آنزیم های بیشتری تولید می شوند.
- در این فرآیند ، گلوکز سریعتر جذب می شود ، کربوهیدرات هایی که وارد بدن می شوند به طور فعال پردازش می شوند. بنابراین ، کبد طولانی تر گلوکز تولید می کند و پروتئین ها خیلی سریعتر جذب می شوند.
اصل عملکرد دارو به میزان دوز ، نوع انسولین ، انتخاب محل تزریق بستگی دارد. هر روش باید فقط پس از توافق با پزشک معالج انجام شود. اولین تزریق ها با نظارت پزشکی انجام می شود.
توصیه هایی برای استفاده از دارو
مهندسی ژنتیک انسانی یا انسولین دوفازی مانند نامهای تجاری مختلفی دارد. همچنین هورمون ها می توانند از نظر مدت زمان عمل ، روش تهیه محلول متفاوت باشند. محصولات بر اساس نوع انسولین نامگذاری شده اند.
انسولین های ساخته شده از نظر ژنتیکی بخشی از داروهایی مانند Humudar ، Vozulim ، Actrapid هستند. اینسوران ، جنسولین. این یک لیست کامل از چنین داروهایی نیست ، تعداد آنها بسیار زیاد است.
تمام داروهای فوق از نظر قرار گرفتن در معرض بدن متفاوت است.GMOs می تواند چندین ساعت طول بکشد یا برای کل روزها فعال باشد.
داروهای ترکیبی دو فاز شامل داروهایی است که شامل اجزای خاصی است که دوره قرار گرفتن در معرض دارو را تغییر می دهد.
- چنین داروهایی به شکل مخلوط فروخته می شوند ، از جمله هورمون هایی که به صورت ژنتیکی بدست می آیند.
- این وجوه شامل Mikstard ، Insuman ، Gansulin ، Gensulin می شود.
- داروها دو بار در روز ، نیم ساعت قبل از غذا استفاده می شوند. چنین سیستمی باید کاملاً رعایت شود ، زیرا این هورمون ارتباط مستقیمی با دوره مصرف مواد غذایی دارد.
با تولید ژن انسولین انسانی ، آماده سازی به دست می آید که دارای مدت زمان قرار گرفتن در معرض متوسط است.
- محلول ظرف 60 دقیقه اثر می گذارد ، اما لحظه ی بیشترین فعالیت شش تا هفت ساعت پس از تزریق مشاهده می شود.
- این دارو پس از 12 ساعت کاملاً از بدن خارج می شود.
- چنین داروهایی شامل Insuran ، Insuman ، Protafan ، Rinsulin ، Biosulin است.
همچنین GMO هایی وجود دارند که مدت کوتاهی در معرض بدن دارند. این داروها شامل انسولین Actrapid ، Gansulin ، Humulin ، Insuran ، Rinsulin ، Bioinsulin است. چنین انسولین ها بعد از دو تا سه ساعت یک مرحله فعال دارند و اولین علائم عملکرد دارو در طی نیم ساعت پس از تزریق قابل مشاهده است.
قبل از تجویز انسولین ، GMOs باید برای شفافیت و عدم وجود مواد خارجی در مایع مورد بررسی قرار گیرند. اگر مواد خارجی ، کدورت یا بارش در دارو ظاهر می شود ، باید ویال را دور ریخت - دارو برای استفاده مناسب نیست.
انسولین مورد استفاده باید در دمای اتاق باشد. اگر دیابتی دارای بیماری عفونی ، اختلال عملکرد تیروئید ، بیماری آدیسون ، هیپوپیتویتاریسم و بیماری مزمن کلیه باشد ، مقدار هورمون باید تنظیم شود.
در صورت انتقال به نوع جدید انسولین ، به دلیل پرش از خوردن وعده های غذایی یا محدودیت بدنی ، حمله به هیپوگلیسمی با مصرف بیش از حد دارو ممکن است. همچنین گسل می تواند بیماریهایی باشد که نیاز به هورمون را کاهش می دهد - درجه شدید بیماری کلیوی ، بیماری کبد ، کاهش غده تیروئید ، قشر آدرنال و غده هیپوفیز.
- کاهش شدید قند خون با تغییر در ناحیه تزریق امکان پذیر است. بنابراین ، لازم است از یک نوع انسولین به طور معقول و تنها پس از توافق با پزشک معالج جابجایی شود.
- اگر یک فرد دیابتی از انسولین با عملکرد کوتاه استفاده کند ، گاهی اوقات حجم بافت چربی در محل تزریق کاهش می یابد یا برعکس ، افزایش می یابد. برای جلوگیری از این امر ، تزریق باید در مکان های مختلف انجام شود.
زنان باردار باید بدانند كه نیازهای انسولین در سه ماهه مختلف بارداری متفاوت است. برای انجام این کار ، شما باید یک آزمایش قند خون روزانه با یک گلوکومتر انجام دهید.
عملکرد انسولین بر روی بدن انسان در این مقاله به تفصیل شرح داده شده است.
1. ساختار و عملکرد انسولین 5
1.1. ساختار مولکول انسولین 5
1.2 اهمیت بیولوژیکی انسولین 7
1.3 بیوسنتز انسولین 8
2. سنتز انسولین مهندسی ژنتیک 10
2.1. استفاده از روشهای مهندسی ژنتیک برای سنتز داروها 10
2.2. روشهای مهندسی ژنتیک 11
2.3 تولید انسولین مهندسی ژنتیک 14

نتیجه گیری 18
علائم مصرف بیش از حد
هنگام استفاده از انسولین ، پیروی از توصیه های پزشک و رعایت دوز دقیق داروی تجویز شده حائز اهمیت است.
در صورت عدم رعایت قوانین و مصرف بیش از حد ، دیابتی شروع به سردردهای شدید ، گرفتگی ، گرسنگی ، عرق کردن ، ضربان قلب می کند ، فرد بیش از حد کار می کند ، تحریک می شود. لرز در کل بدن و لرزیدن نیز می تواند مشاهده شود.
چنین علائمی بسیار شبیه به علائم کاهش قند خون است.با یک مرحله خفیف از علائم ، دیابتی می تواند به طور مستقل مشکل را برطرف کرده و شرایط را بهبود بخشد. برای این کار آب نبات یا هر محصول شیرین دیگری که حاوی شکر باشد ، میل کنید.
- اگر یک کما دیابتی رخ دهد ، از محلول دکستروز استفاده می کنند ، دارو تا زمان آگاهی فرد از طریق وریدی تجویز می شود. در اولین علائم مشکوک ، لازم است که یک آمبولانس فراخوانی شود ، که با روشهای اورژانس قادر به زنده ماندن بیمار خواهد بود.
- به عنوان عوارض جانبی بعد از استفاده از GMO ، فرد دچار بثوراتی روی پوست به صورت کهیر می شود ، قسمت هایی از بدن متورم می شود ، فشار خون به شدت افت می شود ، خارش و تنگی نفس ممکن است رخ دهد. این یک واکنش آلرژیک به یک دارو است ، که پس از مدتی می تواند به خودی خود و بدون مداخله پزشکی از بین برود. در صورت ادامه شرایط ، باید با پزشک خود مشورت کنید.
- در روزهای اول مصرف داروی انسولین ، افراد دیابتی اغلب بدن را آب بدن می کنند ، فرد کمبود مایعات را تجربه می کند ، اشتها بدتر می شود ، تورم در بازوها و پاها ظاهر می شود و خواب آلودگی مداوم احساس می شود. چنین علائمی معمولاً سریع از بین می روند و عود نمی شود.
نظرات و نظرات
من دیابت نوع 2 دارم - وابسته به انسولین نیست. یکی از دوستان توصیه کرد قند خون را با DiabeNot کم کنید. من از طریق اینترنت سفارش دادم پذیرش را شروع کرد.
من یک رژیم غیر دقیق را دنبال می کنم ، هر روز صبح شروع کردم به راه رفتن 2-3 کیلومتر با پای پیاده. طی دو هفته گذشته ، صبح قبل از صرف صبحانه از ساعت 9.3 به 7.1 و حتی دیروز به 6 ، کاهش صاف قند در متر را مشاهده می کنم.
1! دوره پیشگیری را ادامه می دهم. در مورد موفقیتها مشترک می شوم.
مارگاریتا پاولووا ، من هم اکنون در دیابنوت نشسته ام. SD 2. من واقعاً وقت ندارم برای رژیم و پیاده روی ، اما از شیرینی و کربوهیدرات سوء استفاده نمی کنم ، فکر می کنم XE است ، اما به دلیل افزایش سن ، قند هنوز زیاد است.
نتایج به اندازه مال شما خوب نیستند ، اما برای 7.0 قند به مدت یک هفته ظاهر نمی شود. قند را با چه اندازه گیری می کنید؟ آیا او به شما پلاسمایی یا خون کامل نشان می دهد؟ می خواهم نتایج حاصل از مصرف دارو را با هم مقایسه کنم.
از این پست آموزنده بسیار متشکرم
تولید انسولین مهندسی ژنتیک

برای اینکه فرد احساس سلامتی کند ، باید بر میزان انسولین در بدن نظارت داشته باشید. این هورمون باید به اندازه کافی باشد تا گلوکز در خون جمع نشود. در غیر این صورت ، در صورت بروز اختلالات متابولیک ، پزشک تشخیص دیابت را می دهد.
درمان در مرحله پیشرفته دیابت ، تکمیل غلظت گمشده انسولین است که به طور طبیعی بدن نمی تواند تولید شود. برای این کار از انسولین محلول استفاده شده است که شبیه به مهندسی ژنتیک انسانی است. لوزالمعده مسئول تولید چنین هورمونی است.
برای تولید انسولین ، نه تنها از فناوری تولید هورمون طبیعی استفاده می شود ، تولید کنندگان نیز از انسولین اصلاح شده مصنوعی به دست آمده استفاده می کنند. داروی مشخص شده "solubilis" به عنوان محلول در نظر گرفته شده است.
انواع داروها
مهندسی ژنتیک انسانی یا انسولین دوفازی مانند نامهای تجاری مختلفی دارد. همچنین هورمون ها می توانند از نظر مدت زمان عمل ، روش تهیه محلول متفاوت باشند. محصولات بر اساس نوع انسولین نامگذاری شده اند.
انسولین های ساخته شده از نظر ژنتیکی بخشی از داروهایی مانند Humudar ، Vozulim ، Actrapid هستند. اینسوران ، جنسولین. این یک لیست کامل از چنین داروهایی نیست ، تعداد آنها بسیار زیاد است.
تمام داروهای فوق از نظر قرار گرفتن در معرض بدن متفاوت است. GMOs می تواند چندین ساعت طول بکشد یا برای کل روزها فعال باشد.
داروهای ترکیبی دو فاز شامل داروهایی است که شامل اجزای خاصی است که دوره قرار گرفتن در معرض دارو را تغییر می دهد.
- چنین داروهایی به شکل مخلوط فروخته می شوند ، از جمله هورمون هایی که به صورت ژنتیکی بدست می آیند.
- این وجوه شامل Mikstard ، Insuman ، Gansulin ، Gensulin می شود.
- داروها دو بار در روز ، نیم ساعت قبل از غذا استفاده می شوند. چنین سیستمی باید کاملاً رعایت شود ، زیرا این هورمون ارتباط مستقیمی با دوره مصرف مواد غذایی دارد.
با تولید ژن انسولین انسانی ، آماده سازی به دست می آید که دارای مدت زمان قرار گرفتن در معرض متوسط است.
- محلول ظرف 60 دقیقه اثر می گذارد ، اما لحظه ی بیشترین فعالیت شش تا هفت ساعت پس از تزریق مشاهده می شود.
- این دارو پس از 12 ساعت کاملاً از بدن خارج می شود.
- چنین داروهایی شامل Insuran ، Insuman ، Protafan ، Rinsulin ، Biosulin است.
همچنین GMO هایی وجود دارند که مدت کوتاهی در معرض بدن دارند. این داروها شامل انسولین Actrapid ، Gansulin ، Humulin ، Insuran ، Rinsulin ، Bioinsulin است. چنین انسولین ها بعد از دو تا سه ساعت یک مرحله فعال دارند و اولین علائم عملکرد دارو در طی نیم ساعت پس از تزریق قابل مشاهده است.
چنین داروهایی پس از شش ساعت کاملاً دفع می شوند.
استفاده از انسولین انسانی محلول در انسولین برای ایجاد دیابت

انسولین مهندسی ژنتیکی انسان یک جایگزین هورمون معمول برای انسولین است که لوزالمعده را تولید می کند. نه تنها هورمون انسانی اصلاح شده از نظر ژنتیکی برای سنتز استفاده می شود بلکه از ماده ایجاد شده مصنوعی نیز استفاده می شود. یکی دیگر از گزینه های شناخته شده برای ایجاد دارو ، استفاده از انسولین خوک اصلاح شده است ، زیرا در ترکیب و کارکردهای آن به انسان نزدیک است. برنامه تولید انسولین مهندسی ژنتیک. انسولین مهندسی ژنتیکی می تواند هم برای دیابت نوع 1 و هم برای دیابت نوع 2 مورد استفاده قرار گیرد ، هنگامی که یک واکنش پایدار به داروهای خوراکی با ماهیت هیپوگلیسمی مشاهده می شود. در بیمار در انواع خاصی از اغما قابل استفاده است. اگر یک زن باردار به تازگی شروع به ابتلا به دیابت کند ، استفاده از انسولین مهندسی مجاز است ، اما فقط در صورت کمک به رژیم غذایی روی سطح گلوکز تأثیر نمی گذارد. استفاده از آن در موارد عفونت با عفونت هایی که در آنها می توان فشار خون بالا مشاهده کرد توصیه می شود. آماده سازی ژن در استفاده از آنها در هنگام زایمان ، جراحی ، صدمات ، اختلالات متابولیک و در صورت انتقال تدریجی به انسولین با یک عمل طولانی در موفقیت آنها مؤثر است. استفاده از داروهای ژنی که جایگزین این هورمون با حساسیت به عناصر خاصی از دارو و هیپوگلیسمی هستند ، ممنوع است. مواد مخدر از این نوع با گیرنده های خاصی از غشای سلولی واکنش نشان می دهند ، و مجتمع هایی را با آنها تشکیل می دهند. هنگامی که وارد سلول ها می شود ، کمپلکس دارو روی کار تأثیر می گذارد و باعث می شود که آن را فعال تر کرده و آنزیم های بیشتری تولید کند. سطح گلوکز به دلیل این واقعیت است که با سرعت بیشتری توسط سلولها پردازش می شود. پس از آن روند لیپوژنز ، تولید پروتئین تسریع شده و سرعت کبد در تشکیل گلوکز کاهش می یابد. مدت زمان مصرف دارو بستگی به محل تزریق ، نوع دارو ، دوز و پاسخ فردی بدن انسان دارد. فقط پزشک در این گروه می تواند دوز تعیین کند و داروهای خاصی را تجویز کند. در دوره اولیه مصرف دارو ، بیمار از نزدیک توسط پزشکان مورد بررسی قرار می گیرد تا متوجه شود که آیا این دارو رد شده است یا خیر. انسولین مهندسی ژنتیکی انسان در داروهای مشهور مانند Insuran ، Insuman ، Vozulim ، Penfill ، Biosulin ، Gensulin ، Actrapid ، Rinsulin ، Humulin ، Humudar ، Rosinsulin و برخی دیگر موجود است. انواع مختلف انسولین وجود دارد.یکی از طبقه بندی ها مربوط به مدت زمان مصرف دارو است. به گفته وی ، انسولین محلول می تواند یک عمل کوتاه و طولانی داشته باشد. داروهای ترکیبی (انسولین دو فاز) وجود دارد که حاوی ماده ای سریع و طولانی است. به این نوع دارو مخلوط گفته می شود. در میان آنها ، مواردی وجود دارد که با تغییر در هورمون انسانی ایجاد می شود. انسولین دو فاز عبارت است از Mikstard ، Gansulin ، Insuman ، Humulin و Gensulin. آنها باید دو بار در روز ، نیم ساعت قبل از غذا استفاده شوند. این در شرایطی است که انسولین دو فاز دارای ماده ای کوتاه مدت است که میزان مصرف آن به رژیم بستگی دارد. یک آنالوگ مهندسی هورمون انسانی از جمله داروهایی است که دارای مدت متوسط است. این انسولین محلول بعد از یک ساعت شروع به فعالیت می کند و اوج فعالیت آن پس از 7 ساعت اتفاق می افتد. پس از 12 ساعت ، نمایش داده می شود. داروی مهندسی ژنتیکی انسانی این گروه Insuman، Protafan، Humulin، Rinsulin، Biosulin، Gensulin، Gansulin، Insuran است. یک داروی مهندسی ژنتیک انسانی در بین گروه با یک عمل کوتاه وجود دارد. به عنوان مثال ، اینها شامل Gansulin ، Insuran ، Humulin ، Rinsulin ، Gensulin ، Bioinsulin و Actrapid است. چنین انسولین محلول از نیم ساعت شروع به فعالیت می کند و فعالیت آن طی چند ساعت به حداکثر می رسد. چنین داروهایی به مدت 6 ساعت دفع می شوند. در صورت مصرف بیش از حد داروها با انسولین مهندسی ژنتیک ، ضعف ، خواب آلودگی ، خستگی ، تحریک پذیری ، لرز ، افزایش دفع عرق سرد ، لرزش ، رنگ پریدگی ، تپش قلب ، سردرد ، گرفتگی و گرسنگی رخ می دهد. همه اینها علائم کمبود قند خون است. اگر این بیماری به تازگی شروع به توسعه کرده است و در مراحل ابتدایی و آسان تر خود است ، پس می توانید خود علائم را از بین ببرید. برای انجام این کار ، شما باید غذاهایی را با قند و کربوهیدرات های زیاد میل کنید که به راحتی هضم می شوند. گلوکاگون و محلول دکستروز را می توان در بدن وارد کرد. اگر فردی به حالت اغما افتاده است ، باید تا زمان بهبود وضعیت ، یک محلول دکستروز اصلاح شده تزریق کنید. برخی از افراد ممکن است نسبت به استفاده از داروهای اصلاح شده ژنتیکی با انسولین واکنش آلرژی ایجاد کنند. علائم ممکن است شامل کهیر ، تورم ، از بین رفتن قدرت ، فشار خون پایین ، تنگی نفس ، بثورات ، تب و خارش باشد. در بعضی موارد ، هیپوگلیسمی و کما رخ می دهد. مشکلاتی که در آگاهی انسان وجود دارد و حتی ممکن است اغما باشد. اگر بیمار دارویی را از دست ندهد ، ممکن است دچار قند خون شود. به دلیل دوزهای پایین اولیه ، با ایجاد پدیده های عفونی در بدن و همچنین در صورت عدم رعایت قوانین رژیم ، به نظر می رسد. در بعضی موارد ، بیمار ممکن است در مکانهایی که دارو مصرف می کند ، لیپودیستروفی ایجاد کند. در ابتدای استفاده از دارو ، پف کرده ، کمبود آب ، خواب آلودگی و اشتها ممکن است رو به زوال باشد. اما این پدیده ها موقتی هستند. استفاده از یک جایگزین برای انسولین طبیعی ، مانند یک ماده سازنده ژنتیکی ، یک افزودنی عالی برای درمان دیابت است. به دلیل اینکه گلوکز بیشتر جذب سلول می شود ، باعث کاهش سطح قند می شود و فرایندهای انتقال آن تغییر می کند. اما این داروها طبق تجویز پزشک باید کاملاً مورد استفاده قرار گیرند ، زیرا آنها می توانند اثرات بهداشتی ناخواسته ای را برای بیمار ایجاد کنند. انسولین داروی اصلی برای درمان دیابت نوع 1 است. بعضی اوقات از آن برای تثبیت بیمار و بهبود رفاه وی در نوع دوم بیماری نیز استفاده می شود. این ماده به دلیل ماهیت خود هورمونی است که قادر است در دوزهای اندک در متابولیسم کربوهیدرات تأثیر بگذارد. به طور معمول ، لوزالمعده انسولین کافی تولید می کند ، که به حفظ سطح فیزیولوژیکی قند خون کمک می کند. اما با اختلالات جدی غدد درون ریز ، تنها فرصتی برای کمک به بیمار اغلب تزریق انسولین است. متأسفانه ، مصرف آن به صورت خوراکی (به شکل قرص) غیرممکن است ، زیرا در دستگاه گوارش کاملاً از بین می رود و ارزش بیولوژیکی خود را از دست می دهد. به دست آوردن این هورمون از لوزالمعده خوک ها و گاوها یک فناوری قدیمی است که امروزه بندرت مورد استفاده قرار می گیرد. این به دلیل کیفیت پایین داروهای دریافتی ، تمایل آن به ایجاد واکنشهای آلرژیک و عدم کفایت تصفیه آن است. واقعیت این است که از آنجا که هورمون یک ماده پروتئینی است ، از مجموعه خاصی از اسیدهای آمینه تشکیل شده است. انسولین تولید شده در بدن خوک در ترکیب اسید آمینه از انسولین انسانی با 1 اسید آمینه و انسولین گاوی با 3 متفاوت است. در آغاز و اواسط قرن بیستم ، هنگامی که داروهای مشابه وجود نداشتند ، حتی چنین انسولین یک پیشرفت در پزشکی بود و اجازه داد تا درمان دیابتی ها به سطح جدیدی انجام شود. هورمون های به دست آمده از این روش قند خون را کاهش می دهند ، با این حال ، آنها اغلب باعث عوارض جانبی و آلرژی می شوند. تفاوت در ترکیب اسیدهای آمینه و ناخالصی های موجود در دارو وضعیت بیماران را تحت تأثیر قرار داده است ، خصوصاً در دسته های آسیب پذیرتر بیماران (کودکان و افراد مسن). یکی دیگر از دلایل عدم تحمل چنین انسولین ، وجود پیشرونده غیرفعال آن در دارو (پروینسولین) است که خلاص شدن از شر این تغییر دارو غیرممکن بود. در حال حاضر ، انسولین های گوشتی پیشرفته وجود دارد که عاری از این کاستی ها است. آنها از لوزالمعده یک خوک به دست می آیند ، اما پس از آن تحت پردازش و تصفیه اضافی قرار می گیرند. آنها چند جزئی هستند و حاوی مواد تحریک کننده هستند. انسولین گوشت خوک اصلاح شده عملا هیچ تفاوتی با هورمون انسانی ندارد ، بنابراین هنوز هم در عمل استفاده می شود چنین داروهایی توسط بیماران بسیار بهتر تحمل می شوند و عملا باعث ایجاد عوارض جانبی نمی شوند ، سیستم ایمنی بدن را مهار نمی کنند و به طور موثر قند خون را کاهش می دهند. انسولین گاو امروزه در پزشکی مورد استفاده قرار نمی گیرد ، زیرا به دلیل ساختار خارجی آن تأثیر منفی بر سیستم ایمنی و سایر سیستم های بدن انسان دارد. انسولین انسانی ، که برای بیماران دیابتیک استفاده می شود ، در مقیاس صنعتی از دو طریق بدست می آید: شرایط ذخیره انسولیننشانه ها و موارد منع مصرف
عمل دارویی داروها
نمونه هایی از داروهای انسولین مهندسی ژنتیکی انسانی
انسولین از چه چیزی ساخته شده است؟

آماده سازی های بدست آمده از مواد اولیه با منشاء حیوانی
انسولین مهندسی ژنتیک
با یک تغییر فیزیکی و شیمیایی ، مولکولهای انسولین خوک تحت عمل آنزیمهای ویژه با انسولین انسانی یکسان می شوند. ترکیب اسید آمینه از آماده سازی حاصل شده هیچ تفاوتی با ترکیب هورمون طبیعی تولید شده در بدن انسان ندارد.
در فرایند تولید ، دارو تحت تصفیه بسیار بالایی قرار می گیرد ، بنابراین باعث ایجاد واکنش های آلرژیک یا سایر تظاهرات نامطلوب نمی شود.
اما بیشتر اوقات ، انسولین با استفاده از میکروارگانیسم های اصلاح شده (اصلاح شده ژنتیکی) به دست می آید. با استفاده از روش های بیوتکنولوژیک ، باکتری ها یا مخمر به گونه ای اصلاح می شوند که خود آنها بتوانند انسولین تولید کنند.
علاوه بر تولید انسولین ، تصفیه آن نقش مهمی دارد. به طوری که این دارو هیچگونه واکنش آلرژیک و التهابی ایجاد نکند ، در هر مرحله لازم است بر پاکی خلوص میکروارگانیسم ها و کلیه محلول ها و همچنین مواد تشکیل دهنده مورد استفاده نظارت شود.
برای تولید انسولین 2 روش وجود دارد. اولین آنها بر اساس استفاده از دو سویه (گونه) متفاوت از یک میکروارگانیسم واحد است.
هر یک از آنها تنها یک زنجیره از مولکول DNA هورمون را سنتز می کنند (فقط دو مورد از آنها وجود دارد ، و آنها به صورت مارپیچ به هم پیچیده می شوند).
سپس این زنجیره ها به هم متصل می شوند و در محلول حاصل می توان از قبل اشکال فعال انسولین را از آن دسته جدا کرد که هیچ اهمیت بیولوژیکی ندارند.
راه دوم برای تهیه دارو با استفاده از اشرشیا کولی یا مخمر ، مبتنی بر این واقعیت است که میکروب ابتدا انسولین غیرفعال تولید می کند (یعنی پیشرو آن پروینسولین است). سپس با استفاده از درمان آنزیمی ، این فرم فعال شده و در پزشکی استفاده می شود.
پرسنلی که به برخی از امکانات تولید خاص دسترسی دارند ، همیشه باید با لباس محافظ استریل پوشیده شوند ، که باعث از بین رفتن تماس دارو با مایعات بیولوژیکی انسان می شود.
همه این فرآیندها معمولاً به صورت خودکار انجام می شوند ، هوا و تمام سطوح در تماس با آمپول ها و ویال ها استریل هستند و خطوط با تجهیزات بصورت هرمتیکی مهر و موم شده اند.
روش های بیوتکنولوژی دانشمندان را قادر می سازد در مورد راه حل های جایگزین برای دیابت فکر کنند.
به عنوان مثال ، تا به امروز ، مطالعات بالینی در مورد تولید سلولهای بتا پانکراس مصنوعی در حال انجام است که می توان با استفاده از روشهای مهندسی ژنتیک به دست آورد.
شاید در آینده از آنها برای بهبود عملکرد این اندام در فرد بیمار استفاده شود.
تولید داروهای مدرن انسولین یک فرآیند پیچیده فن آوری است که شامل اتوماسیون و مداخلات حداقل انسان است
اجزای اضافی
تولید انسولین بدون مواد تحریک کننده در دنیای مدرن تقریبا غیرممکن است ، زیرا آنها می توانند خواص شیمیایی آن را بهبود بخشند ، زمان عمل را تمدید کرده و به درجه خلوص بالایی برسند.
با توجه به خصوصیات آنها ، تمام مواد اضافی را می توان به کلاسهای زیر تقسیم کرد:
- طولانی کننده ها (موادی که برای تأمین مدت زمان طولانی تر عمل دارو) استفاده می شوند ،
- اجزای ضد عفونی کننده
- تثبیت کننده ، که به دلیل آن اسیدیته بهینه در محلول دارو حفظ می شود.
طولانی کردن مواد افزودنی
انسولین هایی با عملکرد طولانی وجود دارد که فعالیت بیولوژیکی آنها 8 تا 42 ساعت طول می کشد (بسته به گروه دارویی). این اثر به دلیل افزودن مواد ویژه - طولانی کننده به محلول تزریق حاصل می شود. در بیشتر موارد ، یکی از ترکیبات زیر برای این منظور استفاده می شود:
پروتئین هایی که اثر دارو را طولانی می کنند ، تحت تصفیه دقیق قرار می گیرند و کم حساسیت دارند (به عنوان مثال پروتامین). نمک روی نیز بر فعالیت انسولین یا بهزیستی انسان تأثیر منفی نمی گذارد.
ضد عفونی کننده های موجود در ترکیب انسولین لازم است به طوری که فلور میکروبی در طول ذخیره و استفاده در آن تکثیر نمی شود. این مواد نگهدارنده هستند و از حفظ فعالیتهای بیولوژیکی دارو اطمینان می کنند.
علاوه بر این ، اگر بیمار هورمون را از یک ویال فقط به خود تجویز کند ، ممکن است دارو برای چند روز دوام داشته باشد.
با توجه به اجزای ضد باکتریایی با کیفیت بالا ، وی به دلیل امکان نظری تولید مثل در محلول میکروب ها نیازی به دور ریختن داروی بلااستفاده نخواهد داشت.
از مواد زیر به عنوان ضد عفونی کننده در تولید انسولین استفاده می شود:
اگر محلول حاوی یون های روی باشد ، به دلیل خاصیت ضد میکروبی آنها به عنوان ماده نگهدارنده دیگری عمل می کنند
برای تولید هر نوع انسولین ، برخی از مواد ضد عفونی کننده مناسب هستند. تعامل آنها با هورمون باید در مرحله آزمایشات بالینی مورد بررسی قرار گیرد ، زیرا ماده نگهدارنده نباید باعث اختلال در فعالیت بیولوژیکی انسولین شود یا در غیر این صورت بر روی خواص آن تأثیر منفی بگذارد.
استفاده از مواد نگهدارنده در بیشتر موارد ، این هورمون را در زیر پوست و بدون درمان قبلی با الکل یا سایر ضد عفونی کننده ها تجویز می کند (سازنده معمولاً به این امر در دستورالعمل ها اشاره می کند).
این کار دارو را ساده می کند و باعث کاهش تعداد دستکاری های مقدماتی قبل از تزریق می شود.
اما این توصیه فقط درصورتی انجام می شود که محلول با استفاده از یک سرنگ انسولین فردی با یک سوزن نازک تجویز شود.
تثبیت کننده ها
تثبیت کننده ها لازم هستند به طوری که pH محلول در یک سطح معین حفظ شود. حفظ دارو ، فعالیت آن و پایداری خواص شیمیایی بستگی به میزان اسیدیته دارد. در ساخت هورمون تزریق برای بیماران مبتلا به دیابت معمولاً از این فسفاتها استفاده می شود.
برای انسولین همراه با روی ، ثابت کننده کننده محلول همیشه مورد نیاز نیست ، زیرا یون های فلزی به حفظ تعادل لازم کمک می کنند.
اگر با این وجود از آنها استفاده شود ، از ترکیبات شیمیایی دیگر به جای فسفاتها استفاده می شود ، زیرا ترکیبی از این مواد باعث رسوب و نامناسب بودن دارو می شود.
خاصیت مهمی که برای همه تثبیت کننده ها نشان داده شده ایمنی و عدم توانایی در ایجاد هرگونه واکنش با انسولین است.
یک متخصص غدد داخلی باید با انتخاب داروهای تزریقی برای دیابت برای هر بیمار خاص مقابله کند.
وظیفه انسولین تنها حفظ سطح طبیعی قند در خون نیست بلکه آسیب رساندن به سایر ارگان ها و سیستم ها نیست. این دارو باید از نظر شیمیایی خنثی ، حساسیت کم باشد و ترجیحاً مقرون به صرفه باشد.
همچنین انسولین انتخابی با توجه به مدت زمان عمل می تواند با سایر نسخه های آن مخلوط شود بسیار مناسب است.
به دست آوردن انسولین ، روشهای مهندسی ژنتیک ، بیوتکنولوژی - کار درسی

1. ساختار و عملکرد انسولین 5
1.1. ساختار مولکول انسولین 5
1.2 اهمیت بیولوژیکی انسولین 7
1.3 بیوسنتز انسولین 8
2. سنتز انسولین مهندسی ژنتیک 10
2.1. استفاده از روشهای مهندسی ژنتیک برای سنتز داروها 10
2.2. روشهای مهندسی ژنتیک 11
2.3 تولید انسولین مهندسی ژنتیک 14