اصول تشخیص دیابت وابسته به انسولین و غیر وابسته به انسولین
دیابت قندی (دیابت قندی) نوعی بیماری است که به دلیل کمبود انسولین مطلق یا نسبی ایجاد می شود و با نقض انواع متابولیسم و در درجه اول متابولیسم کربوهیدرات مشخص می شود. کلمه دیابت از زبان یونانی است. دیابت - "من در حال گذراندن چیزی هستم" ، "من در حال جریان هستم" ، کلمه "mellitus" از کلمه لاتین "عسل" است که نشانگر طعم شیرین ادرار در دیابت است. دیابت قندی در 4٪ از افراد (در روسیه 1-2٪) و در بین بومیان تعدادی از کشورها تا 20٪ و بالاتر مشاهده می شود. در حال حاضر ، حدود 200 میلیون نفر مبتلا به دیابت در جهان وجود دارند که امید به زندگی آنها 7٪ کاهش یافته است. طبق آمار ، هر پنجمین فرد سالخورده از دیابت رنج می برد که سومین عامل شایع مرگ و کوری محسوب می شود. نیمی از بیماران در اثر نارسایی مزمن کلیه ، 75٪ - از عوارض آترواسکلروز می میرند. آنها 2 برابر بیشتر در معرض بیماری های قلبی و 17 بار نفروپاتی هستند.
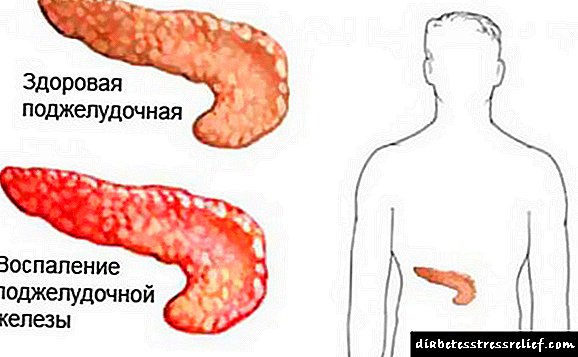
اولین ذکر یک بیماری که یادآور دیابت است مربوط به هزاره چهارم قبل از میلاد (3200 سال) است. اصطلاح دیابت توسط آرتیوس کاپادوکیا (حدود 2000 سال از دوران ما) وارد ادبیات شده است. در قرن XI ، ابن سینا به طور مفصل علائم "بیماری قند" را توصیف کرد و در سال 1679 ، توماس ویلیسون آن را "دیابت" نامید. در سال 1869 ، P. Langerhans ابتدا بستر مورفولوژیکی عملکرد غدد درون ریز لوزالمعده را توصیف کرد ، که توسط خوشههای سلولهای α- (A-) ، β- (B-) ، δ- و PP- نشان داده شده است. مجموعه تمام عناصر سلولی فوق ، از جمله سیستم های عروقی و عصبی ، متعاقباً جزایر لانگرهان نامگذاری شد. در لوزالمعده انسان ، حدود 1 میلیون جزیره وجود دارد که دارای کل جرم 1-1.5 گرم (6 / 0-6٪ از توده غده) و اندازه 100-200 میکرون هستند. هر جزیره تقریباً 2000 سلول ترشحی دارد. جزایر عمدتاً در بدن و دم غده قرار دارند.
در سال 1909 مینر ماده فعال موجود در عصاره لوزالمعده انسولین را نام برد. در سال 1926 ، هابیل و همكاران آن را به شكل شیمیایی خالص جدا كردند. F. Sanger (1956) ساختار شیمیایی خود را نشان داد و در سال 1963 به همراه کوتوسیاننیس و Tsang که به وسیله مصنوعی ساخته شده اند. در حال حاضر ، انسولین در مقادیر صنعتی توسط مهندسی ژنتیک بدست می آید. بخش عمده ای از جزایر لانگرهانس - 68٪ سلول های B- یا β هستند که انسولین تولید می کنند. علاوه بر آنها ، در دستگاه جزایر سلولهای A- یا α (20٪) که گلوکاگون را ترشح می کنند ، و همچنین سلولهای δ (10٪ ، ترشح سوماتوستاتین) و سلولهای PP (2٪ ، پلی پپتید پانکراس ترشح) وجود دارد. سلولهای انتروكرومافین D كه باعث تولید پلی پپتید وازواكتیو روده (VIP) و سروتونین می شوند نیز در اینجا یافت می شوند.
انسولین پروتئین متشکل از دو زنجیره پلی پپتیدی از جمله 51 اسید آمینه است (زنجیره A متشکل از 21 ، زنجیره B از 30 باقیمانده اسید آمینه) ، با وزن مولکولی نزدیک به 6000 D. سنتز آن به شکل پروینسولین در ریبوزوم ها اتفاق می افتد. در شرایط فیزیولوژیکی ، لوزالمعده حدود 25 میلی گرم دارد و نیاز روزانه به آن 5/5 میلی گرم انسولین است. در پلاسما ، آن را به قطعه بافت همبند پروتئین - C-پپتید متصل می کند ، و مقدار پلاسما آن 400-800 نانوگرم در لیتر (ng / l) و C-پپتید - 0.9-3.5 ng / l تخمین زده می شود. . انسولین توسط انسولیناز یا سایر آنزیم های پروتئولیتیک لیزوزوم در کبد (60-40٪) و کلیه ها (20-20٪) از بین می رود.
انسولین در بدن بر انواع اصلی متابولیسم - کربوهیدرات ، پروتئین ، چربی و الکترولیت آب تأثیر می گذارد.
I. با توجه به متابولیسم کربوهیدرات ، اثرات زیر انسولین مشاهده می شود:
آنزیم هگزوکیناز (گلوکوکیناز) را فعال می کند و واکنش بیوشیمیایی اصلی تجزیه هوازی و بی هوازی کربوهیدرات ها را ایجاد می کند - فسفوریلاسیون گلوکز ،
فسفوفروكوكیناز را فعال می كند و فسفوریلاسیون فروكتوز -6-فسفات را فراهم می كند. این واکنش شناخته شده است که نقش مهمی در فرآیندهای گلیکولیز و گلوکونوژنز بازی می کند.
این گلیکوژن سنتاز را فعال می کند و باعث تحریک سنتز گلیکوژن از گلوکز در واکنش های گلیکوژنز می شود.
این فعالیت کربوکسیکیناز فسفینولپیروات را مهار می کند و واکنش گلوکونوژنز کلیدی را مهار می کند ، یعنی تبدیل پیروات به فسفوئنولپیروات - سایپرز ، باشگاه دانش
سنتز اسید استیک از سیتریک را در چرخه کربس فعال می کند.
انتقال گلوکز (و سایر مواد) از طریق غشاهای سیتوپلاسمی ، به ویژه در بافتهای وابسته به انسولین - چربی ، ماهیچه و کبد را تسهیل می کند.
دوم نقش انسولین در تنظیم متابولیسم چربی.
فسفودی استراز را فعال می کند و تجزیه cAMP را افزایش می دهد و این باعث مهار لیپولیز در بافت چربی می شود.
سنتز acyl-coenzyme-A را از اسیدهای چرب تحریک می کند و باعث افزایش استفاده از بدن های کتون توسط سلول ها می شود.
III. نقش انسولین در تنظیم متابولیسم پروتئین:
جذب اسیدهای آمینه را تقویت می کند.
سنتز پروتئین توسط سلول ها را تحریک می کند.
این شکست پروتئین را مهار می کند.
اکسیداسیون اسیدهای آمینه را سرکوب می کند.
چهارم نقش انسولین در تنظیم متابولیسم الکترولیت آب:
باعث تقویت عضلات و کبد پتاسیم می شود.
دفع سدیم ادرار را کاهش می دهد.
احتباس آب را در بدن ترویج می کند.
عمل انسولین بر روی سلولهای هدف بافتهای وابسته به انسولین با اتصال آن به یک گیرنده خاص گلیکوپروتئین آغاز می شود. روی غشای سیتوپلاسمی سلولهای این بافتها ، 50000-250000 گیرنده وجود دارد ، اگرچه فقط حدود 10٪ در واقع عملکرد دارند. رویدادهای زیر به دلیل تعامل انسولین و گیرنده ایجاد می شوند:
تغییرات ساختاری در گیرنده اتفاق می افتد
چندین گیرنده به هم وصل می شوند و یک میکرواگرافات تشکیل می دهند ،
میکرواگرافات توسط سلول جذب می شود (درونی گیرنده) ،
یک یا چند سیگنال درون سلولی شکل می گیرد.
در شرایط خاص ، به عنوان مثال ، با افزایش انسولین در خون ، تعداد گیرنده های سطح سلول های هدف برای انسولین کاهش می یابد و سلول ها نسبت به انسولین حساس تر می شوند. چنین کاهش در تعداد گیرنده ها و کاهش حساسیت آنها به انسولین ، این پدیده را توضیح می دهد مقاومت به انسولین (به عنوان مثال برای چاقی و NIDDM ، به تصویر زیر مراجعه کنید).
ترشح انسولین توسط بسیاری از متابولیتها و مواد فعال بیولوژیکی تحریک می شود: گلوکز ، مانوزای ، اسیدهای آمینه ، به ویژه لوسین و آرژینین ، بمبسین ، گاسترین ، پانکراسین ، سکرتین ، گلوکوکورتیکوئیدها ، گلوکاگون ، STH ، β- آدرنرمی کننده ها. هیپوگلیسمی ، سوماتواستاتین ، اسید نیکوتین ، α-آدرنوستیمولانتها مانع از تولید انسولین می شوند. در اینجا ، ما توجه می کنیم که فعالیت انسولین تحت تأثیر آنتاگونیست های انسولین در پلاسمای خون مرتبط با آلبومین (سینالبومین) ، β-لیپوپروتئین ها و گلوبولین ها (γ-گلوبولین) تغییر می کند.
هورمون پانکراس دوم ، گلوکاگون ، یک پلی پپتید تک رشته ای است که از 29 باقیمانده اسید آمینه با وزن مولکولی حدود 3500 D. تشکیل شده است. به شکل خالص آن ، گلوکاگون در سال 1951 توسط گید جدا شد. سطح خون ناشتا آن در افراد سالم تقریباً 75-150 نانوگرم در لیتر است (تنها 40٪ هورمون فعال است). در طول روز ، بطور مداوم توسط سلولهای α سلولهای جزایر لانگرهان ساخته می شود. ترشح گلوکاگون توسط گلوکز و سوماتوستاتین مهار می شود. همانطور که بیان شد ، گلوکاگون لیپولیز ، کتوژنز ، گلیکوژنولیز ، گلوکونوژنز را تحریک می کند ، که منجر به افزایش قند خون می شود. از اهمیت قابل توجهی در تنظیم گلیسمی تأثیر تحریک کننده آن بر ترشح انسولین - تحریک غیرمستقیم از طریق قند خون و تحریک سریع هتروسلولی مستقیم مستقیم در جزایر است. هورمون در کلیه تجزیه می شود.
مکانیسم عملکرد گلوکاگون از طریق گیرنده های خاص غشای سیتوپلاسمی آدنیلات سیکلاز ، به طور عمده از کبد و افزایش بعدی در محتوای cAMP در سلول ها به فعال سازی کاهش می یابد. این منجر به گلیکوژنولیز ، گلوکونوژنز و بر همین اساس به هایپرگلیسمی ، لیپولیز ، کتوژنز و برخی اثرات دیگر می شود.
علائم اصلی دیابت موارد زیر است:
قند خون (سطح قند خون بالاتر از 6.66 میلی مول در لیتر) ،
گلوکزوزوری (گلوکز در ادرار می تواند به 555-666 میلی مول در لیتر برسد ، در روز حداکثر 150 گرم گلوکز در ادرار اولیه افراد سالم فیلتر می شود ، حدود 300-600 گرم از بیماران دیابتی ، و از بین رفتن احتمالی گلوکز در ادرار به 300 گرم در روز می رسد) ،
پلی اوریا (دیورز روزانه بالای 2 لیتر ، اما می تواند به 12 لیتر برسد) ،
polydipsia - (مصرف بیش از 2 لیتر در روز) ، عطش ،
هایپرلاکتاسیدمی (میزان لاکتات خون بیش از 0.8 میلی مول در لیتر ، اغلب 1.1-1.4 میلی مول در لیتر) ،
هایپرکتونمی - افزایش محتوای بدن کتون در خون (معمولاً بالاتر از 520 میکرومول در لیتر) ، کتونوری ،
لیپمی (لیپید خون بالا ، اغلب بالاتر از 8 گرم در لیتر) ،
مشخصه کاهش سریع وزن بیماران مبتلا به IDDM.
کاهش تحمل گلوکز بدن ، که با آزمایش بارگیری گلوکز با 75 گرم گلوکز و یک لیوان آب تعیین می شود ، در این صورت در طول دقیقه 60 ، 90 و 120 دقیقه میزان اضافی مضاعف گلوکز (حداکثر 11.1 میلی مول در لیتر) وجود دارد.
مظاهرات ناشی از اختلال در متابولیسم چربی عبارتند از:
هایپرلیپمی (لیپیدهای پلاسما بالای 8 گرم در لیتر ، 4-8 نرمال) ،
هایپرکتونمی (محتوای بدن کتون در پلاسما بالاتر از 30 میلی گرم در لیتر یا 520 میکرومول در لیتر) ،
هایپر کلسترول خون (بیش از 6 میلی مول در لیتر ، هنجار 4.2-5.2) ،
هایپرفسفولیپیدمی (بیش از 3.5 میلی مول در لیتر ، هنجار 2.0-3.5) ،
افزایش محتوای NEFA (بیش از 0.8 میلی مول در لیتر) ،
افزایش تری گلیسیرید - تری گلیسیریدمی (بیش از 1.6 میلی مول در لیتر ، هنجار 1 / 1-1 / 6 است) ،
افزایش محتوای لیپوپروتئین ها (بیشتر از 8/8 گرم در لیتر ، هنجار آن 1.3-4.3 است).
نشانگرهای ذکر شده در متابولیسم چربی تغییر یافته نه تنها به دلیل کمبود انسولین بلکه در اثر هورمونهای اضافی ضد هورمونی و همچنین عدم وجود لیپوکائین ایجاد می شود. هایپرلیپمی در غیاب لیپوکائین می تواند منجر به کبد چربی شود که با تسهیل می شود:
کاهش گلیکوژن کبد ،
کمبود عوامل لیپوتروپی از جمله لیپوکائین ،
عفونت ها و مسمومیت ها
همین عوامل منجر به کتوز می شود ، با این حال ، علل فوری کتوز به شرح زیر است:
افزایش تجزیه اسیدهای چرب غیرمستقیم در کبد ،
نقض رزین سنتز اسید استئواستریک به اسیدهای چرب بالاتر ،
اکسیداسیون کافی اسید استیواستریک در چرخه کربس ،
افزایش تشکیل استئو استیک اسید در کبد.
تغییرات فوق در متابولیسم چربی منجر به تسریع در پیشرفت آترواسکلروز می شود.
نقض متابولیسم پروتئین. این اختلالات مربوط به افزایش تجزیه پروتئین و ضعف سنتز پروتئین است. مهار سنتز پروتئین پیش شرط لازم برای تشکیل کربوهیدرات ها از اجزای آنها - گلوکونوژنز است که توسط گلوکوکورتیکوئیدها و گلوکاگون تحریک می شود. ترکیب پروتئین پلاسما مختل می شود:
کاهش آلبومین ،
غلظت گلوبولین ها رو به رشد است ،
سطح آلفا -2 گلیکوپروتئین ها را افزایش می دهد.
اتیولوژی. IDDM وراثت چند فاکتور محسوب می شود. عوامل برون زا و درون زا باعث ایجاد IDDM اکنون گفته می شود دیابتوژن ها. فاكتورهای دیابتوژنیك حوادثی هستند كه هر یك از این موارد با میزان مشخصی می تواند باعث ایجاد IDDM در ناقلین ویژگیهای ژنتیك شود. دیابوژنزهای ویروسی و شیمیایی قادر به تحریک سیتولیز خود ایمنی سلولهای کلیو در بدن افراد مستعد ژنتیکی با ویژگیهای ارثی تنظیم پاسخ ایمنی هستند. اثر تحریک آمیز از مهمترین موارد در دوره اولیه و نسبتاً محدود آنتوژنز است. به همین دلیل است که بیماران مبتلا به IDDM در سنین جوانی بیمار می شوند.
ژنتیکISDM. در حال حاضر ، بیش از 20 سایت مختلف در کروموزوم 2 ، 6 ، 10 ، 11 ، 14 ، 16 و 18 وجود دارد که به طور مثبت با این بیماری مرتبط هستند. تطابق دوقلوهای مونزیژوتیک از 30-54٪ تجاوز نمی کند. در کودکان بستگان فوری با IDDM ، فراوانی بیماری نزدیک به 6٪ است. سهم استثنایی در مستعد سازی توسط ژن ژن HCH در بازوی کوتاه کروموزوم 6 بین جایگاه DR ساخته شده است3، DR4، DQ3,2. اعتقاد بر این است که ارتباط جایگاه پروتئین HCGS طبقه دوم و IDDM توسط عملکردهای ایمونولوژیکی پروتئین های HCGS توضیح داده شده است. در بین قفقازها ، تقریباً 95٪ بیماران مبتلا به IDDM حامل آنتی ژنهای MHC DR هستند3، DR4 و / یا ترکیبی از آنها. درصد متوسط جمعیت جهانی حاملان این هاپلوتیپ بیشتر از 4٪ نیست.
با توجه به وجود نشانگرهای ژنتیکی و ویژگیهای تصویر بیماری ، IDDM را می توان به زیرگروههای 1a و 1b تقسیم کرد. زیرگروه 1b با حضور مکرر مجموعه ای از آنتی ژنهای DR در HCCH مشخص می شود3 (د3) -B8-A ، زیرگروه 1a - با حضور ترکیبی از DR4 (د4 ) -B15-A2-CW3. ترکیبی 1b با توسعه ، در برابر پس زمینه IDDM ، یک محبت خاص خود ایمنی سیستمیک از غدد درون ریز ، که در آن یک تحریک عفونی خاص لازم نیست همراه است. حداکثر 15٪ موارد IDDM متعلق به این زیرگروه هستند. تظاهرات خود ایمنی در برابر سلول های are پایدار است ، در حالی که در همان زمان ، یک پاسخ ایمنی برجسته به انسولین وجود ندارد. پلی آدنوکرینوپاتی خود ایمنی از خصوصیات علامت پیچیده 1a نیست و نقش عفونت را می توان در پاتوژنز مشاهده کرد. خود ایمنی در برابر سلولهای كلهوك زودگذر است و پاسخ خود ایمنی به انسولین همیشه به شدت بیان می شود.
همانطور که اشاره شد ، در حال حاضر در مورد دیابتوژن های عفونی و غیر عفونی صحبت می شود. در میان اولین انواع مختلف ویروس وجود دارد: سرخچه ، واکسین اوریون ، اپشتین بار ، انتروو ویروس Coxsackie B4 و نه Coxsackie ، reoviruses ، cytomegaloviruses ، که بر روی مواد بالینی و مدلهای آزمایشگاهی قادر به ایجاد آسیب به سلولهای lets جزایر پانکراس هستند. به عنوان مثال ، تا 40٪ نوزادانی که مادرانی که در سه ماهه سوم به سرخچه مبتلا شده اند ، در سالهای اول زندگی خود از ابتلا به IDDM بیمار می شوند.
بیشتر ویروس های دیابوژنیک باعث سیتولیز خود ایمنی سلولهای جزایر می شوند. عمل آنتی بادی ها علیه آنتی ژن های سیتوپلاسمی و هسته ای سلول های B هدایت می شود. این آنتی بادی ها می توانند ساختارهای سلولی مشابه ویروس های لوزالمعده را به هم متصل کنند. ویروس های لنفوتروپیک به عنوان آغازگرهای پلی کلونال مکانیسم های خود ایمنی (ویروس های اپستین بار و سرخک) یا به عنوان غیرفعال کننده سرکوب کننده های T (رتروویروس) یا محرک کننده T-activators عمل می کنند. در این حالت ، فرآیند اتوآرژیک ممکن است نتیجه کمبود ویروس ناشی از سرکوبگرها و / یا مضرات اضافی باشد. در عین حال ، سیتولیز ایمونولوژیک در دوره عفونت در افراد مستعد ارثی ذاتی است.
نقش تحریک آمیز ویروس ها در پیدایش سیتولیز خود ایمنی از طریق اینترلوکین ها و اینترفرون ها ، به ویژه -اینترفرون ، در صورت آسیب ویروسی به لوزالمعده است. این سیتوکین ها بیان آنتی ژن های MHC را بر روی سلول های клет و القاء خود آنتی ژن های سطح ژنی سطح برای سیتولیز خود ایمنی متعاقب آن ، و همچنین ظهور نئوآنتی ژن ها در ضایعات ویروسی مداوم القا می کنند.
دیابوژنهای شیمیایی شامل آلوکسان ، اسید اوریک ، استرپتوزوسین ، دیتیزون ، واکسن (عوامل کنترل جوندگان) ، آلبومین سرم گاو (بخشی از شیر گاو) ، نیتروسامین ها و نیتروسورا (موجود در محصولات دودی) ، پنتامیدین (درمانی برای پنوموسیستوز) است. ، محصولات حاوی سیانورهای غذایی (هسته زردآلو ، بادام ، محصولات ریشه آفریقایی Kassava ، که حدود 400 میلیون بومی و غیره را تغذیه می کند). استعمال دخانیات و الكل در افزایش سطح سیانید خون ، افزایش تظاهرات خود ایمنی و تقویت بیماری هموکروماتوز و پانكراتیت نقش دارد.
در مقابل با دیابتوژنز ، موادی با خاصیت محافظتی ، به اصطلاح آنتی دیابتوژن توصیف شده است.در میان آنها اسیدهای آمینه حاوی گوگرد نامیده می شود ، کمبود آن باعث افزایش سمیت سیانیدهای غذایی ، آنتی اکسیدان ها ، روی می شود (در رسوب انسولین شرکت می کند) ، ویتامین PP (مهار آپوپتوز و نکروز ، برای درمان IDDM استفاده می شود) ، اسیدهای چرب اشباع نشده از غذاهای دریایی (مهار سنتز IL-1 و TNF-α شناخته شده).
مکانیسم اصلی آسیب شیمیایی به جزایر پانکراس هستند بیان وابسته به اینترلوکین در غشای سلولهای پروتئین DR وجود ندارد ، تغییر خود ایمنی و آلرژیایجاد شده توسط عوامل مؤثر آنتی ژن متقاطع یا متداول ، و پاسخ ایمنی به بیان نئوآنژنبه دلیل از بین رفتن سلولهای در عین حال ، می توان تکثیر سلول های کلیتو را توسط آنتی بادی های ضد سلول و واسطه های التهاب خود ایمنی سرکوب کرد.
با خلاصه موارد فوق در مورد فرآیندهای ایمنی IDDM ، موارد اصلی را برجسته می کنیم. این ، در مرحله اول ، انسولین آلرژیک ناشی از لنفوسیت های سیتوتوکسیک T (نوع آلرژی با واسطه سلولی) به دلیل بیان سلول های سلول بر روی غشای سلول های کلیو است که در پروتئین های DR معمولی وجود ندارد. بیان نئوآنتیژن ها ، محصولات ژنوم پنهان ویروسی و همچنین بیان غیر طبیعی ژن های HCH درجه دوم روی سلول های، ، مستثنی نیست. در مرحله دوم ، نوع هومورال با تخریب سلولهای д ، که توسط سمیت سلولی وابسته به مکمل و آنتی بادی نشان داده شده است (سمیت سلولی ، یا سیتولیتیک ، نوع واکنش آلرژیک). سیتوکین های ترشح شده (IL-1 ، TNF- ، لنفوتوکسین ، -اینترفرون ، فاکتور فعال کننده پلاکت ، پروستاگلاندین ها) حتی قبل از تخریب خود ایمنی سلول های کلوک منجر به مهار ترشح انسولین می شوند. این به ویژه در مورد IL-1 صادق است ، که باعث کاهش حساسیت سلولهای به گلوکز می شود. این سیتوکین ها که توسط لنفوسیت ها و ماکروفاژها ترشح می شوند ، اثرات سمیت سمی ، ضد پرولیفراتیو و ضد عفونی کننده دارند. علاوه بر سیتولیز اتالرژیک ، IDDM با خاموش شدن فعالیت میتوزی سلولهای مشخص می شود.
پاتوژنز IDDM.پیوند کلیدی در پاتوژنز IDDM ، مرگ تدریجی سلولهای جزایر پانکراس است. این منجر به تغییر در روابط هتروسلولی در جزایر ، انسولینوپنی ، اضافی از جزایر و هورمونهای ضد جزیره خارج از جزیره می شود. در نتیجه ، مصرف گلوکز و انواع متابولیسم مختل می شود. اختلالات متابولیک مزمن باعث ایجاد عوارض IDDM می شود که عمده ترین آنها با آنژیوپاتی همراه است.
نقش ویروسی و / یا دیابوژن شیمیایی تحریک آمیز القاء تغییر خود ایمنی است. در 10٪ از بیماران مبتلا به زیرگروه IDDM 1b (در ترکیب با پلی آندرونینوپاتی خود ایمنی سیستمیک) ، تحریک ضروری نیست. در بیماران مبتلا به زیرگروه IDDM 1a ، یک رویداد تحریک آمیز باید در ابتدای تولد یا حتی قبل از تولد رخ دهد ، زیرا IDDM نوعی بیماری با یک پروموتون ایمونولوژیک طولانی و یک دوره جبران سوخت و ساز بدن است. فاصله زمانی از اولین فرآیند خود ایمنی تا شروع عدم تحمل گلوکز 3-4 سال است و طولانی ترین دوره بین اولین تظاهرات کاهش توانایی تولید انسولین و جبران آشکار متابولیک 1 تا 12 سال است. بروز اوج بیماری IDDM در دوره های سنی از بدو تولد تا 3 سال و از 9 تا 13 سال رخ می دهد. پس از 14 سال ، پتانسیل دیابوژن های درون زا برای تحریک تخریب سلول های کلیو کاهش می یابد.
مبنای عملکردی ISDM. در پاسخ به تغییر ایمنی ، جزایر لوزالمعده انسولین ایجاد می کند که با مرگ سلول های کلیت ، تغییرات اگزوداتیو ، نفوذ جزایر توسط لنفوسیت ها ، ماکروفاژها ، ائوزینوفیل ها ، اعوجاج روابط عصبی عروقی و توپوگرافی سلولی و تماس های بین سلولی بروز می یابد. با زمان تشکیل دیابت بالینی مشهود ، وزن لوزالمعده به دو ، وزن توده جزایر - سه برابر و سلول های B - بیش از 850 برابر کاهش می یابد. در عین حال ، نسبت سلولهای A (حداکثر 75٪) و سلولهای δ (تا 25٪) در جزایر بی نظم در حال رشد است. در نتیجه ، نسبت گلوکاگون به انسولین در خون بیماران مبتلا به IDDM ، با پیشرفت بیماری ، به سمت بی نهایت گرایش پیدا می کند.
طبقه بندی دیابت.مترادف دیابت نوع اول: I ، وابسته به انسولین ، هیپوکسولینمیک ، جوان (نوجوان) IDDM) 20٪ از کل موارد ابتلا به دیابت اولیه را تشکیل می دهد. زیرگروهها: Ia - به دلیل ترکیبی از اثرات ژنتیکی و محیطی ، IB - اولیه ، از نظر ژنتیکی و بدون تحریک برون زا ، Ic - با آسیب اولیه سلولهای کلیت بوسیله دیابوژنزهای شیمیایی برون زا و ویروسها.
دیابت نوع دوم اولیه (غیر وابسته به انسولین ، هایپرینسولینمیک ، بزرگسالان ، افراد مسن ، چاق ، NIDDM) 80٪ از کل موارد دیابت را با زیرگروه های زیر تشکیل می دهد:
IIa - NIDDM در بیماران غیر چاق ،
IIb - NIDDM در بیماران چاق ،
IIс - NIDDM در سنین جوانی.
اصطلاحات "IDDM" ، "NIDDM" دوره بالینی (مستعد ابتلا به كتواسیدوز و مقاوم به كتواسیدوز ، جدول 3.1) را توصیف می كنند ، و اصطلاحات "انواع I و II" به مکانیسم های بیماری زای بیماری (نتیجه تسلط بر خود ایمنی یا مکانیسم های دیگر) اشاره دارد.
دیابت ثانویه (اینها سندرم هایپرگلیسمی یا دیابتی هستند که نتیجه بیماریهایی است که بر لوزالمعده یا سیستم تنظیم متابولیسم کربوهیدرات ها تأثیر می گذارد).
دیابت ثانویه ناشی از تخریب غیر خود ایمنی سلولهای کلیوک (پانکراتیت مزمن ، سرطان ، هموکروماتوز ، کیستوز ، تروما) ،
دیابت ثانویه ناشی از اختلالات غدد درون ریز با تولید بیش از حد هورمونهای ضد بارداری (سندرم کوشینگ ، آکرومگالی ، فئوکروموسیتوم ، گلوکاگون ، پرکاری تیروئید ، هیپرپلازی غده پینهال) ،
دیابت یدروژن ثانویه در نتیجه استفاده از داروها (کورتیکواستروئیدها ، ACTH ، داروهای ضدبارداری خوراکی ، پروپرانولول ، داروهای ضد افسردگی ، برخی از دیورتیک ها) ،
دیابت ثانویه در سندرم های تعیین شده ژنتیکی (لیپودیستروفی ، اشکال هیپوتالاموس چاقی ثانویه ، گلیکوژنوز نوع I ، بیماری داون ، شرسفسکی ، کلاینفلتر).
معیارهای اختلاف بین IDDM و NIDDM
کمبود انسولین مطلق
کمبود انسولین نسبی
فرآیند خود ایمنی در برابر سلولهای
هیچ فرآیند خود ایمنی وجود ندارد
عدم مقاومت به انسولین اولیه
خطر بالای كتواسیدوز
کم خطر کتواسیدوز
هیچ ارتباطی با چاقی ندارد
پیوندی به چاقی را ردیابی کنید
مطابقت دوقلوهای یکسان 30-50٪
مطابقت دوقلوهای یکسان 90-100٪
ما یک بار دیگر تأکید می کنیم که پیوند کلیدی در پاتوژنز IDDM مرگ پیشرونده سلولهای کلیوک به دلیل تغییر خودایمنی است. نشانگرهای آنتی ژن IDDM شناسایی شده - این آنتی ژن های MHC DR هستند3، DR4، DQ3.2.
در خانواده هایی که پدر مبتلا به IDDM است ، تعداد فرزندان بیمار 4-5 برابر بیشتر از خانواده هایی است که مادر در آن بیمار است.
درگیری ایمنی بین مادر و جنین در سیستم AB0 و Rh + خطر ابتلا به IDDM را افزایش می دهد.
با این حال ، یک پیشگیری ژنتیکی فقط احتمال بالایی از بیماری را ایجاد می کند. برای اجرا ، عوامل دیابتی عفونی و غیر عفونی مورد نیاز است. مکانیسم عمل دیابتوژنزها با بیان وابسته به اینترلوکین از اتوژن ژنهای سلول همراه است. دلیلی بر این باور است که بخش قابل توجهی از بیماران مبتلا به NIDDM ، افرادی هستند که در مراحل اولیه تکامل دیابت قرار دارند ، اما هنوز انسولین کافی برای جلوگیری از کتواسیدوز دارند. NIDDM در افراد چاق دارای یک مکانیسم پاتوژنتیک قابل توجهی است - تولید چربی پروتئین ضد سیتوکین TNF-. IDDM و NIDDM پیوندهای پاتوژنتیک زیادی دارند ؛ در عین حال ، وجود اشکال مختلط و انتقالی قابل انکار نیست.
شرح دیابت به عنوان یک بیماری غدد درون ریز مستقل در رساله پزشکی "Ebers Papyrus". طبقه بندی دیابت ، علائم و دلایل آن. تشخیص بیماری: تجزیه و تحلیل ادرار ، خون برای قند و هموگلوبین گلیکوزی شده.
| سرفصل | پزشکی |
| مشاهده | چکیده |
| زبان | روسی |
| تاریخ اضافه شد | 23.05.2015 |
| اندازه پرونده | 18.0 K |

ارسال کار خوب خود به پایگاه دانش آسان است. از فرم زیر استفاده کنید
دانشجویان ، دانشجویان فارغ التحصیل ، دانشمندان جوانی که از پایگاه دانش در مطالعات و کار خود استفاده می کنند از شما بسیار سپاسگزار خواهند بود.
ارسال شده در http://www.allbest.ru/
مؤسسه آموزشي دولتي بودجه آموزش حرفه اي بالاتر
"دانشگاه علوم پزشکی شمال غربی
آنها I.I. Mechnikov »از وزارت بهداشت فدراسیون روسیه
موضوع چکیده: "اصول تشخیص وابسته به انسولین
و دیابت غیر وابسته به انسولین "
خگی ملیس دمیتریویچ
حتی پانزده سال قبل از دوران ما ، مصریان باستان در رساله پزشکی خود "Ebers Papyrus" دیابت را یک بیماری مستقل توصیف می کردند. پزشکان بزرگ یونان و روم باستان خستگی ناپذیر درباره این بیماری مرموز فکر می کردند. دکتر آرتائوس با نام "دیابت" آمده است - به زبان یونانی ، "من جریان می یابم." دانشمند سلس معتقد است كه سوء هاضمه مقصر ابتلا به دیابت است و بقراط بزرگ كه با طعم ادرار بیمار تشخیص داده شده است. به هر حال ، چینی های باستان نیز می دانستند که با دیابت ، ادرار شیرین می شود. آنها با استفاده از مگس ها (و زنبورها) به یک روش تشخیصی اصلی رسیدند. اگر مگس ها با ادرار روی یک نعلبکی بنشینند ، ادرار شیرین است و بیمار مریض است.
دیابت قندی یک بیماری غدد درون ریز است که با افزایش مزمن قند خون به دلیل کمبود مطلق یا نسبی انسولین - هورمون پانکراس - مشخص می شود. این بیماری منجر به نقض انواع متابولیسم ، آسیب رساندن به رگ های خونی ، سیستم عصبی و همچنین سایر ارگان ها و سیستم ها می شود.
تشخیص: هموگلوبین غدد درون ریز دیابت قندی
دیابت وابسته به انسولین (دیابت نوع 1) به طور عمده در کودکان و جوانان بروز می کند ،
دیابت وابسته به انسولین (دیابت نوع 2) معمولاً در افراد بالای 40 سال که اضافه وزن دارند ، ایجاد می شود. این شایعترین نوع بیماری است (در 80-85٪ موارد) ،
دیابت ثانویه (یا علامت دار) ،
دیابت سوء تغذیه
در دیابت نوع 1 ، کمبود انسولین مطلق به دلیل نقص عملکرد لوزالمعده وجود دارد.
در دیابت نوع 2 ، کمبود نسبی انسولین ذکر شده است. سلول های لوزالمعده به طور همزمان انسولین کافی تولید می کنند (گاهی اوقات حتی به میزان زیاد). با این وجود تعداد ساختارهایی که از تماس آن با سلول اطمینان می کنند و به گلوکز خون کمک می کنند تا وارد سلول شود ، بر روی سطح سلول مسدود یا کاهش می یابد. کمبود گلوکز سلول علامتی برای تولید انسولین حتی بیشتر است ، اما این هیچ تاثیری ندارد و با گذشت زمان ، تولید انسولین به میزان قابل توجهی کاهش می یابد.
علت اصلی دیابت نوع 1 یک فرآیند خود ایمنی است که در اثر نقص سیستم ایمنی بدن ایجاد می شود ، که در آن آنتی بادی ها در بدن در برابر سلول های لوزالمعده تولید می شود که آنها را از بین می برد. عامل اصلی تحریک بروز دیابت نوع 1 یک عفونت ویروسی (سرخچه ، آبله مرغان ، هپاتیت ، اوریون (اوریون) و غیره) در برابر پیش زمینه ژنتیکی مستعد ابتلا به این بیماری است.
مصرف منظم مکمل های غذایی حاوی سلنیوم خطر ابتلا به دیابت نوع 2 را افزایش می دهد.
عوامل اصلی تحریک توسعه دیابت نوع 2 دو مورد است: چاقی و مستعد ارثی:
چاقی در حضور چاقی ، قاشق غذاخوری می کنم. با مصرف 2 قاشق غذاخوری خطر ابتلا به دیابت 2 برابر افزایش می یابد. - 5 بار ، با هنر III - بیش از 10 بار شکل چاقی شکمی بیشتر با ابتلا به این بیماری همراه است - وقتی چربی در شکم توزیع می شود.
تمایل ارثی. در صورت وجود دیابت در والدین یا خانواده فوری ، خطر ابتلا به این بیماری 2-6 برابر افزایش می یابد.
دیابت غیر وابسته به انسولین به تدریج ایجاد می شود و با شدت متوسط علائم مشخص می شود.
دلایل به اصطلاح دیابت ثانویه می تواند:
1. بیماری پانکراس (پانکراس ، تومور ، برداشتن و غیره) ،
2. بیماریهای هورمونی (سندرم ایتنکو-کوشینگ ، آکرومگالی ، گواتر سمی منتشر ، فئوکروموسیتوم) ،
3. قرار گرفتن در معرض داروها یا مواد شیمیایی ،
4- تغییر در گیرنده های انسولین ،
5- سندرم های ژنتیکی خاصی و غیره
به طور جداگانه ، دیابت زنان باردار و دیابت ناشی از سوء تغذیه جدا شده است.
علاوه بر ارزیابی شکایات موجود و اطلاعات بی حسی ، تشخیص آزمایشگاه الزامی است. تعیین گلوکز ناشتا و همراه با بارهای مختلف ، تشخیص اجسام گلوکز و کتون در ادرار ، مطالعه انسولین ، پپتید C در سرم خون ، تعیین پروتئین های خون گلیکوزیله شده و تیترهای سلولهای پانکراس تولیدکننده انسولین جزایر (در صورت بیماری و آنتی بادی های ضد ویروس) .
آزمایش قند خون
یک روش بسیار آموزنده و مقرون به صرفه یک آزمایش خون برای قند است. صبح به طور جدی روی معده خالی انجام می شود. به طور معمول ، غلظت گلوکز از 3.3 تا 5.5 میلی مول در لیتر است. در طول روز ، میزان قند بسته به رژیم تغییر می کند. تشخیص نیاز به اندازه گیری های متعدد در روزهای مختلف دارد. در بیمار مبتلا به دیابت ، قند خون در خون وریدی بیش از 10 میلی مول در لیتر ، در مویرگی - 11.1 میلی مول در لیتر است. از نوع آزمایشگاهی ، برای تشدید بیماری التهابی ، پس از مداخلات جراحی ، در پس زمینه هورمون درمانی (مثلاً هنگام مصرف هورمونهای تیروئید) استفاده نمی شود.
آزمایش هموگلوبین گلیکوزی شده
هموگلوبین گلیکوزی شده با افزودن گلوکز به پروتئین هموگلوبین ، که در گلبولهای قرمز یافت می شود ، تشکیل می شود. ماده مورد مطالعه برای مطالعه ، خون کامل با ضد انعقاد خون است. این تجزیه و تحلیل برای تشخیص دیابت ، تعیین جبران خسارت ، برای کنترل درمان این بیماری ضروری است. سطح متوسط گلوکز نه در زمان تجزیه و تحلیل بلکه در طی سه ماه گذشته نشان می دهد. هنجار 4-6٪ است ، انحراف از این شاخص تا حد زیادی نشانگر دیابت ، کمبود آهن در بدن است.
تعیین C- پپتید باعث می شود که بین دیابت وابسته به انسولین و غیر وابسته به انسولین تفاوت قائل شویم تا مناسب ترین دوز انسولین تعیین شود. به طور معمول ، محتوای پپتید C 0.5 - 2.0 میکروگرم بر لیتر است. کاهش این مقدار نشانگر کمبود انسولین درون زا ، تشدید دیابت ، افزایش سطح نشانگر نارسایی مزمن کلیه ، انسولینوم است. سوء ظن ها همچنین با کمک آزمایش برای سرکوب تشکیل C- پپتید تأیید می شوند: پس از تجزیه و تحلیل ، انسولین تجویز می شود و یک ساعت بعد مطالعه دوم انجام می شود.
ادرار به عنوان یک اقدام اضافی برای تشخیص بیماری استفاده می شود. تشخیص گلوکز در ادرار علامت بارز یک روند پاتولوژیک محسوب می شود. تشخیص اجسام کتون ، نشانگر ایجاد یک شکل پیچیده است. بوی مداوم استون از حفره دهان نشان دهنده استونوری است.
بیماری غدد درون ریز می تواند بر روی عملکرد سایر اندام های داخلی تأثیر بگذارد ، بنابراین ، تشخیص جامع دیابت توصیه می شود که هدف آن هم تعیین نوع ، مرحله بیماری و هم چنین تشخیص اختلال عملکرد سایر سیستم ها است. پزشک در این مورد بر اساس شکایات بیمار ، مطالعات آزمایشگاهی و ابزاری است.
معیارهای اصلی برای تشخیص دیابت وابسته به انسولین عبارتند از: غلظت قند خون ناشتا بیش از 6.7 میلی مول در لیتر ، وجود اجسام گلوکز و کتون در ادرار ، تیترهای بالای آنتی بادی به سلولهای لوزالمعده ایجاد می شود.اختلالات پنهان سوخت و ساز کربوهیدرات با مطالعه هموگلوبین گلیکوزیله (بیش از 9٪) و فروکتوزامین (بیش از 3 میلی مول در لیتر) و غیره تشخیص داده می شود.
برای دیابت قند غیر وابسته به انسولین ، معیار تشخیصی افزایش سطح گلوکز ناشتا بالاتر از 6.7 میلی مول در لیتر است.
گلوکز افزایش یافته در ادرار معمولاً با مطالعه کسری در وعده های روزانه مشخص می شود. سطح هموگلوبین گلیکوزیله شده و فروکتوزامین نیز بالا می رود. اما سطح انسولین ایمنی و پپتید C از مقادیر طبیعی تجاوز نمی کند.
لازم به ذکر است که تشخیص دیابت بر اساس حداقل تعیین دو برابری گلوکز ناشتا و یا دو برابر بیش از حد غلظت گلوکز در خون 11 میلی مول در لیتر در یک زمان خودسرانه انتخاب می شود.
در عمل ، اغلب مواردی وجود دارد که برای تشخیص دیابت ، لازم است آزمایش با بار گلوکز انجام شود (با این آزمایش ، اختلال در تحمل گلوکز نیز تشخیص داده می شود).
تشخیص دیابت مبتنی بر شاخص های زیر این آزمایش است: روی معده خالی - بیش از 6.7 میلی مول در لیتر ، دو ساعت بعد از بارگیری گلوکز - بیش از 11.1 میلی مول در لیتر. به طور معمول ، این شاخص ها همزمان با اولین تظاهرات بالینی بیماری است.
عوارض دیابت در درجه اول با ایجاد کما ، که در آن به مراقبت های اورژانسی مورد نیاز است خطرناک است. چنین شرایطی شامل کتوآسیدوز و کما دیابتی کتواسیدوتیک ، کما هیپوگلیسمی و همچنین کما هایپراسمولار و لاکتیک کش است. ایجاد این شرایط با اختلالات حاد متابولیک همراه است. شایع ترین کما دیابتی کتواسیدوتیک و کما hypoglycemic.
درمان دیابت با هدف از بین بردن اختلالات متابولیک ناشی از کمبود انسولین و پیشگیری یا از بین بردن ضایعات عروق خونی انجام می شود. بسته به نوع دیابت قندی (وابسته به انسولین یا وابسته به انسولین) ، به بیماران تجویز انسولین یا خوراکی داروهای دارای اثر قند خون تجویز می شود. همه بیماران مبتلا به دیابت باید از رژیم غذایی تعیین شده توسط پزشک متخصص پیروی کنند که ترکیب کمی و کیفی آن نیز بستگی به نوع دیابت دارد. برای حدود 20٪ از بیماران مبتلا به دیابت غیر وابسته به انسولین ، رژیم غذایی قند تنها و روش کاملاً کافی برای دستیابی به جبران است. در بیماران مبتلا به دیابت غیر وابسته به انسولین ، به ویژه در چاقی ، تغذیه درمانی باید با هدف از بین بردن وزن اضافی انجام شود. پس از عادی سازی یا کاهش وزن بدن در چنین بیمارانی ، استفاده از داروهای کاهش دهنده قند کاهش می یابد و بعضا کاملاً از بین می رود.
نسبت پروتئین ها ، چربی ها و کربوهیدرات ها در رژیم غذایی بیمار مبتلا به دیابت باید از نظر فیزیولوژیکی باشد. لازم است که نسبت پروتئین ها 16-20٪ ، کربوهیدرات ها - 50-60٪ ، چربی ها - 24-30٪ باشد. رژیم غذایی بر اساس اصطلاحاً محاسبه می شود. وزن ایده آل یا مطلوب وزن بدن. هر بیمار مبتلا به دیابت باید با رعایت وزن ، قد و ماهیت کارهایی که توسط بیمار و همچنین نوع دیابت انجام می شود ، کاملاً از رژیم غذایی فردی پیروی کند که توسط پزشک متخصص تهیه شده باشد. بنابراین ، اگر هنگام انجام کار بدنی سبک ، بدن باید به ازای هر 1 کیلوگرم وزن ایده آل ، 30-40 کیلو کالری بدست آورد ، پس با وزن واقعی 70 کیلوگرم ، به طور متوسط 35 کیلو کالری به ازای هر کیلوگرم ، یعنی 2500 کیلوکالری لازم است. با دانستن محتوای مواد مغذی موجود در محصولات غذایی ، می توانید تعداد کیلو کالری ها در واحد سطح هر یک از آنها را محاسبه کنید.
به بیمار مبتلا به دیابت توصیه می شود رژیم غذایی معادل کسری (خوردن 5-6 بار در روز) توصیه شود. مقدار کالری و ارزش غذایی روزانه رژیم غذایی در صورت امکان باید یکسان باشد ، زیرا این امر از نوسانات شدید غلظت گلوکز در خون جلوگیری می کند. با این وجود ، باید میزان مصرف انرژی را در نظر گرفت که در روزهای مختلف متفاوت است. ما باید بار دیگر بر اهمیت پیروی شدید از رژیم غذایی تأکید کنیم ، این امر باعث می شود که جبران کامل تری از بیماری به دست بیاید. بیماران قندی مبتلا به دیابت قند و شیرینی های دیگر ، میوه های سرشار از کربوهیدرات های قابل هضم (انگور ، خرمالو ، انجیر ، خربزه) ، ادویه جات ممنوع است. جایگزین های قند (سوربیتول ، زایلیتول و غیره) می توانند در مقادیر بیش از 30 گرم در روز در رژیم غذایی قرار گیرند. بسته به نوع دیابت و وزن بدن بیمار ، مصرف نان از 100 تا 400 گرم در روز ، محصولات آرد - 60-90 گرم در روز است. سیب زمینی به 200-300 گرم در روز ، چربی های حیوانی (کره ، شیر ، چربی گوشت خوک) تا 30-40 گرم محدود می شود ، توصیه می شود با روغن های گیاهی یا مارگارین جایگزین شوند. سبزیجات - کلم سفید ، خیار ، کاهو ، گوجه فرنگی ، کدو سبز تقریباً نامحدود هستند. استفاده از چغندر ، هویج ، سیب و سایر میوه های بدون شیر نباید بیش از 300-400 گرم در روز باشد. انواع کم چربی گوشت و ماهی باید به مقدار بیش از 200 گرم ، شیر و فراورده های لبنی - بیش از 500 گرم ، پنیر لپه -150 گرم ، تخم مرغ - 1-1 ، 5 عدد تخم در روز در رژیم غذایی روزانه قرار نگیرد. محدودیت نمک متوسط (حداکثر 6-10 گرم) مورد نیاز است.
رژیم غذایی روزانه بیماران مبتلا به دیابت قند باید حاوی مقادیر کافی ویتامین ها ، به ویژه ویتامین های A ، C ، B باشد ، هنگام تهیه رژیم غذایی ، باید شرایط بیمار ، وجود بیماریهای همزمان و گشت ، شرایط را در نظر گرفت. با کتواسیدوز ، میزان چربی در رژیم غذایی بیمار کاهش می یابد ؛ پس از از بین بردن کتواسیدوز ، بیمار می تواند دوباره به مجموعه غذاهای روزانه قبلی بازگردد. اهمیت ماهیت پردازش آشپزی محصولات نیز اهمیت کمتری ندارد ، لبه نیز باید با در نظر گرفتن بیماریهای همزمان مانند کولسیستیت ، گاستریت ، بیماری زخم معده و دکتر انجام شود.
ارسال شده در Allbest.ru
اسناد مشابه
مقاله مدت زمان 64.8 K ، اضافه شده 11/27/2013
اپیدمیولوژی دیابت وابسته به انسولین و غیر وابسته به انسولین. طبقه بندی دیابت. عوامل خطر دیابت. ارزیابی بهداشتی مقایسه ای شرایط تأمین آب در کرت های آزمایشی و آزمایشی. ارزیابی تغذیه جمعیت.
مقاله مدت 81.2 K ، اضافه شده 2012/16/16
تعریف و طبقه بندی دیابت قندی - بیماری غدد درون ریز است که به دلیل کمبود هورمون انسولین ایجاد می شود. علل اصلی ، علائم ، درمانگاه ، پاتوژنز دیابت. تشخیص ، درمان و پیشگیری از بیماری.
ارائه 374.7 K ، اضافه شده 12.25.2014
علت بیماری دیابت ، تشخیص زودرس آن. تست تحمل گلوکز. شیوع دیابت در روسیه. پرسشنامه "ارزیابی خطر دیابت". یادداشت پیراپزشکی "تشخیص زودرس دیابت".
مقاله مدت 1.7 M ، افزوده 05/16/2017
توصیف بالینی دیابت به عنوان یکی از شایع ترین بیماریهای جهان. بررسی عوامل خطر و دلایل توسعه. علائم دیابت و تظاهرات آن. سه درجه از شدت بیماری. روشهای تحقیق آزمایشگاهی.
مقاله مدت 179.2 K ، اضافه شده 2014/4/14
عوارض دیابت و نظارت بر آنها. شرایط هیپوگلیسمی ، توضیحات آنها. مطالعه بیوشیمیایی گلوکز خون. معیارهای تشخیص دیابت. بررسی ادرار روزانه گلوکزوزوری. آلبومین در ادرار (میکروآلبومینوری).
مقاله مدت 217.4 K ، اضافه شده 06/18/2015
طبقه بندی دیابت قندی - بیماری غدد درون ریز است که با افزایش مزمن قند خون به دلیل کمبود انسولین مطلق یا نسبی مشخص می شود. علت دیابت ، تشخیص و روشهای دارویی گیاهی.
چکیده 23.7 K ، اضافه شده در 2 دسامبر 2013
مفهوم دیابت به عنوان یک بیماری غدد درون ریز همراه با کمبود انسولین نسبی یا مطلق است. انواع دیابت ، علائم اصلی بالینی آن است. عوارض احتمالی بیماری ، درمان پیچیده بیماران.
ارائه 78.6 K ، اضافه شده 1/20/2016
خصوصیات دیابت به عنوان یک بیماری غدد درون ریز. علل ایجاد دیابت نوع V در دوران بارداری. دیابت حاملگی: عوامل خطر اصلی ، عوارض احتمالی ، تشخیص و کنترل. علائم اصلی کمبود قند خون.
چکیده 28.5 K ، افزوده 02/12/2013
اتیولوژی ، پاتوژنز ، طبقه بندی و معیارهای تشخیص افتراقی دیابت نوع 1 و نوع 2. آمار شیوع دیابت ، دلایل اصلی بیماری است. علائم بیماری دیابت ، معیارهای اصلی تشخیصی.
ارائه 949.8 K ، اضافه شده 2013/3/13
پاتوژنز دیابت غیر وابسته به انسولین (NIDDM)
دیابت قندی غیر وابسته به انسولین (NIDDM) ناشی از اختلال در ترشح انسولین و مقاومت در برابر عمل آن. به طور معمول ، در پاسخ به بار گلوکز ، ترشح اصلی انسولین به صورت ریتمیک رخ می دهد. در بیماران مبتلا به دیابت غیر انسولین وابسته به انسولین (NIDDM) ، ترشح ریتمیک پایه انسولین مختل می شود ، پاسخ به بارگذاری گلوکز ناکافی است ، و سطح پایه انسولین بالا می رود ، اگرچه نسبتاً پایین تر از هایپرگلیسمی است.
ثابت ابتدا ظاهر می شود قند خون و هیپرینسولینمی ، که باعث توسعه دیابت غیر وابسته به انسولین (NIDDM) می شود. قند خون مداوم باعث کاهش حساسیت سلولهای بتای جزایر شده و منجر به کاهش انتشار انسولین برای سطح قند خون مشخص می شود. به طور مشابه ، سطح پایه مزمن انسولین ، گیرنده های انسولین را مهار می کند و باعث افزایش مقاومت به انسولین می شود.
علاوه بر این ، از آنجا که حساسیت به انسولین کاهش و افزایش ترشح گلوکاگون ، در نتیجه گلوکاگون اضافی باعث افزایش ترشح گلوکز از کبد می شود که باعث افزایش قند خون می شود. در پایان ، این چرخه شریر منجر به دیابت غیر وابسته به انسولین می شود.
معمولی دیابت قندی غیر وابسته به انسولین ناشی از ترکیبی از تمایل ژنتیکی و عوامل محیطی است. مشاهدات حمایت از یک پیشگویی ژنتیکی شامل تفاوت در تطابق بین دوقلوهای تک قلو و سرگیجه ، جمع شدن خانواده و تفاوت در شیوع در جمعیت های مختلف است.

اگرچه نوع وراثت در نظر گرفته می شود چند عاملی، شناسایی ژنهای اصلی ، که تحت تأثیر سن ، جنس ، قومیت ، وضعیت جسمی ، رژیم غذایی ، سیگار کشیدن ، چاقی و توزیع چربی قرار گرفته اند ، موفقیتی حاصل شده است.
ژنوم کامل غربالگری نشان داد که در جمعیت ایسلندی با دیابت قند غیر وابسته به انسولین ، آللهای پلی مورفیک تکرارهای پشت سر هم کوتاه در اینترون از فاکتور رونویسی TCF7L2 از نزدیک مرتبط هستند. هتروزیگوت ها (38٪ از جمعیت) و هموزیگوت ها (7٪ از جمعیت) به ترتیب تقریبا 1.5 و 2.5 برابر خطر NIDDM را نسبت به افراد غیر حامل افزایش می دهند.
بلند شده خطر در ناقلین ، TCF7L2 در گروههای بیمار دانمارکی و آمریکایی نیز یافت شد. خطر NIDDM مرتبط با این آلل 21٪ است. TCF7L2 یک فاکتور رونویسی را درگیر در بیان هورمون گلوکاگون ، که غلظت گلوکز خون را افزایش می دهد ، بر خلاف عمل انسولین ، که باعث کاهش سطح قند خون می شود ، رمزگذاری می کند. غربالگری گروههای فنلاندی و مکزیکی پیش بینی دیگری را نشان داد ، جهش Prgo12A1a در ژن PPARG ، که بدیهی است برای این جمعیت خاص است و تا 25٪ از خطر جمعیت NIDDM را فراهم می کند.
مکرر آلل پرولین با فرکانس 85٪ رخ می دهد و باعث افزایش اندک خطر (1.25 برابر) دیابت می شود.
ژن PPARG - عضو خانواده گیرنده هورمون هسته ای است و برای تنظیم عملکرد و تمایز سلول های چربی از اهمیت بالایی برخوردار است.
تصدیق نقش عوامل عوامل محیطی شامل همبستگی کمتر از 100٪ در دوقلوهای مونوزژوت ، تفاوت در توزیع در جمعیت های مشابه ژنتیکی و ارتباط با سبک زندگی ، تغذیه ، چاقی ، بارداری و استرس است. به طور تجربی تأیید شده است که اگرچه یک پیشگیری ژنتیکی یک پیش نیاز برای ایجاد دیابت غیر وابسته به انسولین است ، بیان بالینی دیابت وابسته به انسولین (NIDDM) به میزان زیادی به تأثیر عوامل محیطی بستگی دارد.
فنوتیپ و توسعه دیابت غیر وابسته به انسولین (NIDDM)
معمولاً دیابت قندی غیر وابسته به انسولین (NIDDM) در افراد چاق میانسال یا بالاتر دیده می شود ، اگرچه به دلیل افزایش تعداد چاقی و عدم تحرک کافی در بین جوانان ، تعداد کودکان بیمار و جوانان رو به افزایش است.
دیابت نوع 2 شروع تدریجی دارد و معمولاً با افزایش سطح گلوکز با معاینه استاندارد تشخیص داده می شود. بر خلاف بیماران مبتلا به دیابت نوع 1 ، بیماران مبتلا به دیابت غیر وابسته به انسولین (NIDDM) معمولاً دچار کتواسیدوز نمی شوند. اصولاً ، توسعه دیابت غیر وابسته به انسولین (NIDDM) به سه مرحله بالینی تقسیم می شود.
غلظت گلوکز ابتدا خون با وجود بالا رفتن سطح انسولین طبیعی است ، نشان می دهد که بافتهای هدف انسولین نسبت به مقاومت هورمون نسبتاً مقاوم هستند. سپس ، علی رغم افزایش غلظت انسولین ، قند خون بعد از ورزش ایجاد می شود. سرانجام ، اختلال در ترشح انسولین باعث ایجاد قند خون و گرسنگی و تصویر بالینی دیابت می شود.
علاوه بر قند خون ، متابولیک اختلالاتناشی از اختلال در عملکرد سلولهای بسل و مقاومت به انسولین باعث آترواسکلروز ، نوروپاتی محیطی ، پاتولوژی کلیه ، آب مروارید و رتینوپاتی می شود. در یکی از شش بیمار مبتلا به دیابت غیر انسولین وابسته به انسولین (NIDDM) ، نارسایی کلیوی یا آسیب شناسی شدید عروقی که نیاز به قطع عضو اندام تحتانی دارد ، ایجاد می شود ، از هر پنج بیمار به دلیل ایجاد رتینوپاتی کور می شود.
توسعه اینها عوارض به دلیل پیشینه ژنتیکی و کیفیت کنترل متابولیک. با تعیین سطح هموگلوبین گلیکوزیله (HbA1c) می توان قند خون مزمن را تشخیص داد. سخت ، تا حد ممکن نزدیک به حد نرمال ، حفظ غلظت گلوکز (بیش از 7٪) ، با تعیین سطح HbA1c ، خطر عوارض را 35-75٪ کاهش می دهد و می تواند میانگین امید به زندگی را افزایش دهد ، که در حال حاضر به طور متوسط 17 سال پس از استقرار است. تشخیص برای چند سال
ویژگی های فنوتیپی تظاهرات دیابت غیر وابسته به انسولین - سایپرز ، باشگاه دانش:
• سن شروع: از کودکی تا بزرگسالی
• هایپرگلیسمی
• کمبود نسبی انسولین
• مقاومت به انسولین
• چاقی
• آتانز سیاه شدن پوست
درمان دیابت غیر وابسته به انسولین (NIDDM)
کاهش وزن بدنافزایش فعالیت بدنی و تغییرات رژیم غذایی به بیشتر بیماران مبتلا به دیابت وابسته به انسولین (NIDDM) کمک می کند تا حساسیت به انسولین را به میزان قابل توجهی بهبود بخشد. متأسفانه ، بسیاری از بیماران برای دستیابی به بهبود ، قادر به تغییر زندگی شیوه زندگی خود نیستند و تمایل به درمان با داروهای هیپوگلیسمی خوراکی مانند سولفونیل اوره ها و بیگوانیدها ندارند. کلاس سوم داروها ، تیازولیدین دیون ، با اتصال به PPARG ، مقاومت به انسولین را کاهش می دهد.
همچنین می توانید از چهارمین استفاده کنید دسته مواد مخدر - مهار کننده های α- گلوکزیداز ، با کند شدن جذب روده گلوکز. هر یک از این کلاسهای دارویی به عنوان مونوتراپی برای دیابت غیر وابسته به انسولین (NIDDM) تأیید شده است. اگر یکی از آنها پیشرفت بیماری را متوقف نکند ، می توان یک داروی از کلاس دیگر اضافه کرد.
هیپوگلیسمی دهان مقدمات در دستیابی به کنترل گلوکز به عنوان کاهش وزن ، افزایش فعالیت بدنی و تغییرات رژیم غذایی مؤثر نیست.به منظور دستیابی به کنترل گلوکز و کاهش خطر عوارض ، برخی از بیماران به انسولین درمانی نیاز دارند ، با این وجود مقاومت به انسولین ، افزایش هیپرینسولینمی و چاقی را افزایش می دهد.
خطرات وراثت دیابت غیر وابسته به انسولین (NIDDM)
خطر جمعیت دیابت قندی غیر وابسته به انسولین (NIDDM) به جمعیت مورد مطالعه بسیار وابسته است ، در بیشتر جمعیت این خطر از 1 تا 5٪ است ، اگرچه در ایالات متحده آمریکا 6-7٪ است. اگر بیمار خواهر و برادر مریضی داشته باشد ، خطر تا 10٪ افزایش می یابد ، وجود یک خواهر و برادر مریض و سایر خویشاوند درجه یک خطر را تا 20٪ افزایش می دهد ، اگر دوقلو مونزیگوتیک بیمار باشد ، خطر تا 50-100٪ افزایش می یابد.
علاوه بر این ، از آنجا که برخی از انواع دیابت وابسته به انسولین (NIDDM) با دیابت نوع 1 همپوشانی دارند ، کودکان والدین مبتلا به دیابت غیر وابسته به انسولین (NIDDM) برای ابتلا به دیابت نوع 1 خطر تجربی 1 از 10 دارند.
نمونه ای از دیابت قند غیر وابسته به انسولین. M.P. ، یک مرد 38 ساله سالم ، یک قبیله آمریکایی هندی پیما ، در مورد خطر ابتلا به دیابت غیر وابسته به انسولین (NIDDM) مشاوره می کند. پدر و مادر هر دو مبتلا به دیابت غیر وابسته به انسولین بودند ، پدرش در سن 60 سالگی در اثر انفارکتوس میوکارد و مادرش در 55 سالگی در اثر نارسایی کلیوی درگذشت. پدربزرگ پدری و یکی از خواهران بزرگتر نیز از بیماری دیابت غیر وابسته به انسولین رنج می برند ، اما او و چهار خواهر و برادر کوچکتر وی سالم هستند.
به جز یک فرد خردسال ، داده های امتحان طبیعی بودند چاقی، قند خون ناشتا طبیعی است ، با این حال ، افزایش انسولین و قند خون بعد از بار گلوکز خوراکی مشاهده می شود. این نتایج با تظاهرات اولیه یک وضعیت متابولیکی سازگار است ، که احتمالاً منجر به دیابت غیر وابسته به انسولین می شود. پزشک وی به بیمار توصیه کرد سبک زندگی خود را تغییر دهد ، وزن کم کند و فعالیت بدنی را افزایش دهد. بیمار به شدت مصرف چربی خود را کاهش داد ، دوچرخه سواری را شروع به کار کرد و سه بار در هفته دوید ، وزن بدن 10 کیلوگرم کاهش یافت و تحمل گلوکز و انسولین نیز به حالت عادی بازگشت.
انواع دیابت و خصوصیات اصلی آنها
مهم است که بتوانیم بین انواع آسیب شناسی تمایز قائل شویم. در مورد ویژگی های هر نوع دیابت در زیر بخوانید:
- دیابت نوع 1. این یک بیماری وابسته به انسولین است که در نتیجه نقص ایمنی ، استرس های با تجربه ، تهاجم ویروسی ، مستعد ارثی و شیوه زندگی نادرست شکل گرفته ایجاد می شود. به عنوان یک قاعده ، این بیماری در اوایل کودکی تشخیص داده می شود. در بزرگسالی ، یک نوع دیابت وابسته به انسولین بسیار کمتر اتفاق می افتد. بیمارانی که از چنین دیابت رنج می برند ، باید سطح قند خود را به دقت کنترل کنند و به موقع از تزریق انسولین استفاده کنند تا خود را به حالت اغما ندهند ،
- دیابت نوع 2. این بیماری عمدتاً در افراد مسن و همچنین در افرادی که شیوه زندگی منفعلانه ای را تجربه می کنند یا چاق هستند بروز می یابد. با چنین بیماری ، لوزالمعده مقدار کافی انسولین تولید می کند ، اما به دلیل عدم حساسیت به هورمون ها در سلول ها ، در خون تجمع می یابد ، در نتیجه باعث جذب گلوکز نمی شود. در نتیجه بدن گرسنگی انرژی را تجربه می کند. اعتیاد به انسولین با چنین دیابت بروز نمی کند ،
- دیابت کم فشار. این نوعی پیشگیری دیابت است. در این حالت ، بیمار احساس خوبی می کند و از علائمی رنج نمی برد ، که معمولاً زندگی بیماران وابسته به انسولین را خراب می کند. با دیابت کم فشار میزان گلوکز خون کمی افزایش می یابد. علاوه بر این ، هیچ استون در ادرار چنین بیمارانی وجود ندارد ،

حاملگی. بیشتر اوقات ، این آسیب شناسی در زنان در اواخر بارداری رخ می دهد. دلیل افزایش قند افزایش تولید گلوکز است که برای تحمل کامل جنین ضروری است. معمولاً ، اگر دیابت حاملگی فقط در دوران بارداری ظاهر شود ، آسیب شناسی متعاقباً به خودی خود و بدون هیچگونه اقدامات پزشکی از بین می رود ،- دیابت نهفته. بدون علائم واضح پیش می رود. سطح گلوکز خون طبیعی است ، اما تحمل گلوکز مختل است. اگر اقدامات به موقع انجام نشود ، شکل نهفته ممکن است به یک دیابت تمام عیار تبدیل شود ،
- دیابت نهفته. دیابت نهفته به دلیل نقص سیستم ایمنی بدن ایجاد می شود ، به همین دلیل سلول های لوزالمعده توانایی عملکرد کامل خود را از دست می دهند. درمان دیابت نهفته مشابه درمانی است که برای دیابت نوع 2 استفاده می شود. مهم است که این بیماری کنترل شود.
چگونه می توان 1 یا 2 نوع دیابت را در بیمار تشخیص داد؟



آزمایشات آزمایشگاهی برای تشخیص دقیق دیابت نوع 1 یا نوع 2 لازم است. اما برای پزشک ، اطلاعات به دست آمده هنگام مکالمه با بیمار و همچنین در طول معاینه اهمیت کمتری نخواهد داشت. هر نوع ویژگی های خاص خود را دارد.
ویژگی های زیر می تواند در مورد این واقعیت است که بیمار مبتلا به دیابت نوع 1 می گوید:

- علائم خیلی سریع ظاهر می شوند و طی چند هفته آشکار می شوند ،
- دیابتی های وابسته به انسولین تقریباً هرگز وزن اضافی ندارند. آنها یک جسم نازک یا یک بدن طبیعی دارند ،
- تشنگی شدید و تکرر ادرار ، کاهش وزن با اشتهای خوب ، تحریک پذیری و خواب آلودگی ،
- این بیماری اغلب در کودکانی که مستعد ارثی هستند ، رخ می دهد.
تظاهرات زیر نشانگر دیابت نوع 2 است:

- توسعه بیماری طی چند سال رخ می دهد ، بنابراین علائم ضعیف بیان می شوند ،
- بیماران دارای اضافه وزن یا چاقی هستند ،
- سوزن سوزن شدن روی سطح پوست ، خارش ، بثورات ، بی حسی اندامها ، تشنگی شدید و مراجعه مکرر به توالت ، گرسنگی مداوم با اشتهای خوب ،
- هیچ ارتباطی بین ژنتیک و دیابت نوع 2 مشاهده نشد.
اما با این وجود ، اطلاعات بدست آمده در فرآیند برقراری ارتباط با بیمار ، فقط تشخیص اولیه را ایجاد می کند. برای تشخیص دقیق تر ، آزمایش آزمایشگاهی لازم است.
چه علائمی می تواند بین یک نوع وابسته به انسولین و یک نوع مستقل از انسولین تمایز قایل شود؟
اصلی ترین ویژگی تمایز علائم است.
به عنوان یک قاعده ، بیماران مبتلا به دیابت وابسته به انسولین به عنوان دیابتی وابسته به انسولین از علائم حاد رنج نمی برند.
با توجه به رژیم غذایی و شیوه زندگی خوب ، آنها تقریباً می توانند سطح قند را به طور کامل کنترل کنند. در مورد دیابت نوع 1 ، این کار مؤثر نخواهد بود.
در مراحل بعدی بدن به تنهایی قادر به مقابله با هایپرگلیسمی نخواهد بود ، در نتیجه ممکن است کما رخ دهد.
چگونه می توان نوع دیابت را با قند خون مشخص کرد؟

دیابت از این روش درمانی مانند آتش می ترسد!
شما فقط نیاز به اعمال ...

برای شروع ، آزمایش خون برای قند از نوع طبیعی تجویز می شود. از انگشت یا از رگ گرفته می شود.
در نتیجه ، یک فرد بالغ با رقمی از 3.3 تا 5.5 میلی مول در لیتر (برای خون از انگشت) و 3.7-6.1 mmol / L (برای خون از ورید) تهیه می شود.
اگر این نشانگر از علامت 5.5 میلی مول در لیتر تجاوز کند ، بیمار مبتلا به پیش بینی دیابتی می شود. اگر نتیجه بیش از 6.1 میلی مول در لیتر باشد ، این نشانگر وجود دیابت است.
هرچه این شاخص ها بیشتر باشد ، احتمال ابتلا به دیابت نوع یک نیز بیشتر است. به عنوان مثال ، سطح قند خون 10 میلی مول در لیتر یا بیشتر ، تأیید بارز دیابت نوع 1 خواهد بود.
سایر روشهای تشخیص افتراقی
به عنوان یک قاعده ، حدود 10-20٪ از کل بیماران مبتلا به دیابت وابسته به انسولین رنج می برند. همه دیگران از دیابت غیر وابسته به انسولین رنج می برند.
مطمئناً متخصصان برای کمک به تجزیه و تحلیل این بیماری که از چه نوع بیماری رنج می برد ، به تشخیص افتراقی متوسل می شوند.

برای تعیین نوع آسیب شناسی ، آزمایش خون اضافی انجام می شود:
- خون روی C- پپتید (به تعیین اینکه انسولین لوزالمعده تولید می شود) کمک می کند ،
- آنتی بادی های خود به آنتی ژن های سلولهای بتا لوزالمعده ،
- برای حضور بدن کتون در خون.
علاوه بر گزینه های ذکر شده در بالا ، آزمایش های ژنتیکی نیز می توانند انجام شوند.
فیلم های مرتبط
درباره اینکه چه آزمایشاتی را برای انجام دیابت باید انجام دهید ، در این ویدئو:
برای تشخیص کامل نوع ناهنجاری های دیابتی ، معاینه جامع لازم است. اگر علائم اصلی دیابت را مشاهده کردید ، حتما با پزشک مشورت کنید. اقدام به موقع باعث کنترل بیماری و جلوگیری از عوارض خواهد شد.
اتیولوژی بیماری
دیابت نوع 1 یک بیماری ارثی است ، اما یک پیش بینی ژنتیکی پیشرفت آن را تنها با یک سوم تعیین می کند. احتمال آسیب شناسی در کودک مبتلا به مادر دیابتی بیش از 1-2٪ نخواهد بود ، یک پدر بیمار - از 3 تا 6٪ ، خواهر و برادر - حدود 6٪.
یک یا چند نشانگر هومورال ضایعات لوزالمعده ، که شامل آنتی بادی های جزایر لانگرهانس است ، در 85-90٪ بیماران قابل تشخیص است:
- آنتی بادی های گلوتامات دکربوکسیلاز (GAD) ،
- آنتی بادی های تیروزین فسفاتاز (IA-2 و IA-2 بتا).
در این حالت ، اهمیت اصلی در تخریب سلولهای بتا به عوامل ایمنی سلولی اختصاص دارد. دیابت نوع 1 معمولاً با هاپلوتیپ HLA مانند DQA و DQB همراه است.
اغلب این نوع آسیب شناسی با سایر اختلالات خود ایمنی غدد درون ریز همراه است ، به عنوان مثال بیماری آدیسون ، تیروئیدیت خود ایمنی. اتیولوژی غیر غدد درون ریز نیز نقش مهمی ایفا می کند:
- ویتیلیگو
- آسیب شناسی روماتیسمی ،
- آلوپسی
- بیماری کرون.
پاتوژنز دیابت
 دیابت نوع 1 وقتی یک فرآیند خود ایمنی 80 تا 90 درصد سلولهای بتا لوزالمعده را از بین ببرد ، احساس دیابت می کند. علاوه بر این ، شدت و سرعت این روند پاتولوژیک همیشه متفاوت است. بیشتر اوقات ، در دوره کلاسیک این بیماری در کودکان و جوانان ، سلولها کاملاً سریع از بین می روند و دیابت به سرعت آشکار می شود.
دیابت نوع 1 وقتی یک فرآیند خود ایمنی 80 تا 90 درصد سلولهای بتا لوزالمعده را از بین ببرد ، احساس دیابت می کند. علاوه بر این ، شدت و سرعت این روند پاتولوژیک همیشه متفاوت است. بیشتر اوقات ، در دوره کلاسیک این بیماری در کودکان و جوانان ، سلولها کاملاً سریع از بین می روند و دیابت به سرعت آشکار می شود.
از زمان شروع بیماری و اولین علائم بالینی آن تا بروز کتواسیدوز یا کما کتواسیدوتیک ، بیش از چند هفته نمی تواند بگذرد.
در موارد دیگر ، بسیار نادر ، در بیماران مسن تر از 40 سال ، این بیماری می تواند به طور پنهانی ادامه یابد (دیابت خود ایمنی پنهان نه تنها لادا).
علاوه بر این ، در این شرایط ، پزشکان دیابت نوع 2 را تشخیص داده و به بیماران خود توصیه می کنند که در این روش می توانند کمبود انسولین را با داروهای سولفونیل اوره جبران کنند.
با این حال ، با گذشت زمان ، علائم کمبود هورمون مطلق شروع می شود:
- کتونوریا
- کاهش وزن
- هایپرگلیسمی آشکار در پس زمینه استفاده منظم از قرص ها برای کاهش قند خون.
پاتوژنز دیابت نوع 1 مبتنی بر کمبود مطلق هورمون است. به دلیل عدم امکان دریافت قند در بافتهای وابسته به انسولین (عضله و چربی) ، کمبود انرژی ایجاد می شود و در نتیجه لیپولیز و پروتئولیز شدیدتر می شوند. یک روند مشابه باعث کاهش وزن می شود.
با افزایش قند خون ، هیپراسمولاری رخ می دهد ، همراه با دیورز اسمزی و کم آبی. با کمبود انرژی و هورمون ، انسولین ترشح گلوکاگون ، کورتیزول و هورمون رشد را مهار می کند.
با وجود قند خون در حال رشد ، گلوکونوژنز تحریک می شود. تسریع لیپولیز در بافتهای چربی باعث افزایش چشمگیر در حجم اسیدهای چرب می شود.
اگر کمبود انسولین وجود داشته باشد ، توانایی لیپوسنتز کبد سرکوب می شود و اسیدهای چرب آزاد به طور فعال در کتوژنز دخیل هستند. تجمع کتون ها باعث ایجاد کتوز دیابتی و پیامد آن - کتواسیدوز دیابتی می شود.
در برابر پیش زمینه افزایش تدریجی کم آبی و اسیدوز ، یک اغما ایجاد می شود.
در صورت عدم معالجه (کافی انسولین درمانی و تجویز مجدد) ، تقریباً در 100٪ موارد منجر به مرگ خواهد شد.
روشی برای درمان دیابت

شماره ثبت اختراع: 588982
. برای بیمار خود حمام (شدت خفیف تا متوسط) یا اسکراب ید تجویز می شود. فرم کنترل برای اولین بار 11 در 100- - 150 متر گرم در لیورو از درجه احتقان 00150 چهارم است - 100 در سال -200 8 دقیقه ، ایتونتراسین 100-150 میلی گرم در لیتر ، پروولول 12 دقیقه ، سوم در غلظت کنسانتره / لیتر ، مدت زمان 15 مایل ، حمام هشتم. در copps ntra. میلی گرم در لیتر ، مدت زمان 15 دقیقه ، حمام نهم و دهم 100- مدت زمان 12 0 دقیقه قند بسته به شدت دیابت در مقایسه با سطح اولیه حمام m تعیین می شود که بعد از برهنه تعیین می شود.
روشی برای تشخیص شدت دیابت

شماره ثبت اختراع: 931168
. گلوکز علاوه بر این ، مطالعه ای در مورد محتوای 8 4 در سرم خون ایزومرهای β- گلوکز و گلوکز به روش پیشنهادی ، نسبت محتوای D-گلوکز و β- گلوکز 0.74 ، که مربوط به شدت خفیف دیابت است ، انجام شده است و تشخیص دیابت خفیف 1 توسط دیگران تأیید شده است. مطالعات بیوشیمیایی خون و ادرار ، بویژه آزمایش خون بیوشیمیایی بدون آسیب شناسی ، قند ادرار 23 ، گلوکزوزوری تا 30 گرم فوندوس و سیستم عصبی بدون تغییر دیابتی ، به بیمار تجویز و انجام یک دوره درمانی از جمله اقدامات رژیم غذایی ، بدون تجویز اضافی عوامل کم خون و بخصوص انسولین ، PRI me R 2. بیمار K-va 52 ساله در بخش درمانی بیمارستان بود.
علائم دیابت نوع 1
این نوع آسیب شناسی بسیار نادر است - بیش از 1.5-2 all از کل موارد بیماری. خطر بروز در طول زندگی 0.4٪ خواهد بود. اغلب ، فرد در سن 10 تا 13 سالگی به چنین دیابت مبتلا می شود. بخش عمده ای از تظاهرات آسیب شناسی تا 40 سال رخ می دهد.
اگر مورد معمولی باشد ، به ویژه در کودکان و نوجوانان ، این بیماری به عنوان علائم واضح ظاهر می شود. در چند ماه یا چند هفته می تواند توسعه یابد. عفونت ها و سایر بیماری های همزمان می توانند جلوه دیابت را تحریک کنند.
علائم مشخصه انواع دیابت است:
- پولیوریا
- خارش پوست ،
- پولییدپسی
این علائم به ویژه با بیماری نوع 1 ظاهر می شوند. در طول روز ، بیمار می تواند حداقل 5-10 لیتر مایعات بنوشاند و دفع کند.
خاص برای این نوع بیماری ، کاهش شدید وزن است که طی 1-2 ماه می تواند به 15 کیلوگرم برسد. علاوه بر این ، بیمار از:
- ضعف عضلانی
- خواب آلودگی
- کاهش عملکرد.
 در همان آغاز ، او ممکن است از افزایش غیر منطقی اشتها ناراحت شود ، که با افزایش کتواسیدوز با بی اشتهایی جایگزین می شود. بیمار بوی مشخصه استون از حفره دهان را تجربه می کند (ممکن است بوی میوه ای وجود داشته باشد) ، حالت تهوع و شبه عمل جراحی - درد شکم ، کم آبی شدید ، که می تواند باعث اغما شود.
در همان آغاز ، او ممکن است از افزایش غیر منطقی اشتها ناراحت شود ، که با افزایش کتواسیدوز با بی اشتهایی جایگزین می شود. بیمار بوی مشخصه استون از حفره دهان را تجربه می کند (ممکن است بوی میوه ای وجود داشته باشد) ، حالت تهوع و شبه عمل جراحی - درد شکم ، کم آبی شدید ، که می تواند باعث اغما شود.
در بعضی موارد ، اولین علامت دیابت نوع 1 در کودکان مبتلا به آگاهی با اختلال پیش رونده خواهد بود. می توان آنقدر تلفظ کرد که در پس زمینه آسیب شناسی های همزمان (جراحی یا عفونی) کودک ممکن است در حالت اغما قرار بگیرد.
این نادر است که یک بیمار بالاتر از 35 سال از دیابت رنج می برد (با دیابت خود ایمنی پنهان) ، بیماری ممکن است آنقدر احساس روشن نکند و در طی یک آزمایش معمول قند خون کاملاً تصادفی تشخیص داده شود.
شخص دچار کاهش وزن نخواهد شد ، پولیوریا و پولییدپسی متوسط خواهد بود.
ابتدا پزشک می تواند دیابت نوع 2 را تشخیص داده و با کاهش دارو قند را در قرص ها شروع کند. این امر پس از مدتی جبران قابل قبول بیماری را تضمین می کند. با این وجود ، بعد از گذشت چند سال ، معمولاً بعد از 1 سال ، بیمار علائم ناشی از افزایش کمبود انسولین در کل را نشان می دهد:
- کاهش وزن چشمگیر
- کتوز
- کتواسیدوز
- عدم توانایی در حفظ سطح قند در حد لازم.
معیارهای تشخیص دیابت
با توجه به اینکه نوع 1 این بیماری با علائم واضح مشخص است و یک آسیب شناسی نادر است ، یک مطالعه غربالگری برای تشخیص سطح قند خون انجام نمی شود. احتمال ابتلا به دیابت نوع 1 در بستگان نزدیک حداقل است ، که به همراه عدم وجود روشهای مؤثر برای تشخیص اولیه بیماری ، نامناسب بودن یک مطالعه دقیق از نشانگرهای ایمنی زایای آسیب شناسی در آنها را تعیین می کند.
تشخیص این بیماری در بخش عمده ای از موارد بر اساس تعیین مقدار قابل توجهی از قند خون در بیمارانی که علائم کمبود انسولین مطلق دارند ، خواهد بود.
آزمایش خوراکی برای تشخیص بیماری بسیار نادر است.
آخرین مکان تشخیص افتراقی نیست. تأیید تشخیص در موارد مشکوک ، یعنی تشخیص قند خون متوسط در صورت عدم وجود علائم واضح و واضح دیابت نوع یک ، به ویژه با تظاهر در سنین جوانی ، ضروری است.
هدف از چنین تشخیصی ممکن است تمایز بیماری از سایر انواع دیابت باشد. برای این کار ، روش تعیین سطح پایه پپتید C و 2 ساعت بعد از خوردن غذا استفاده کنید.
معیار ارزش تشخیص غیرمستقیم در موارد مبهم ، تعیین نشانگرهای ایمونولوژیک دیابت نوع 1 است:
- آنتی بادی های مجتمع جزایر پانکراس ،
- دکربوکسیلاز گلوتامات (GAD65) ،
- تیروزین فسفاتاز (IA-2 و IA-2P).
رژیم درمانی
درمان هر نوع دیابت مبتنی بر 3 اصل اساسی خواهد بود:
- کاهش قند خون (در مورد ما ، انسولین درمانی) ،
- رژیم غذایی
- آموزش بیمار
درمان با انسولین برای آسیب شناسی نوع 1 ماهیت جایگزینی دارد. هدف آن به حداکثر رساندن تقلید از ترشح طبیعی انسولین به منظور دستیابی به معیارهای جبران پذیرفته شده است. انسولین درمانی فشرده تولید فیزیولوژیکی هورمون را از نزدیک نزدیک می کند.
نیاز روزانه این هورمون با میزان ترشح پایه آن مطابقت دارد. 2 تزریق یک داروی با میانگین مدت زمان قرار گرفتن در معرض یا 1 تزریق انسولین طولانی گلارژین می تواند انسولین بدن را فراهم کند.
حجم کل هورمون بازال نباید بیش از نیمی از نیاز روزانه دارو باشد.
ترشح انسولین (تغذیه ای) انسولین با تزریق هورمون انسان با مدت زمان کوتاه یا فوق العاده کوتاه در معرض قرار گرفتن قبل از غذا جایگزین می شود. در این حالت ، دوز بر اساس معیارهای زیر محاسبه می شود:
- مقدار کربوهیدرات که قرار است در طول وعده های غذایی مصرف شود ،
- میزان قند خون موجود ، قبل از تزریق انسولین تعیین می شود (اندازه گیری شده با استفاده از گلوکومتر).
بلافاصله پس از تظاهرات دیابت نوع 1 و به محض شروع درمان آن برای مدت زمان کافی ، نیاز به آماده سازی انسولین ممکن است اندک باشد و کمتر از 0.3-0.4 U / kg باشد. این دوره "ماه عسل" یا مرحله بهبودی مداوم نامیده می شود.
پس از مرحله ای از قند خون و کتواسیدوز ، که در آن تولید انسولین با بقای سلول های بتا سرکوب می شود ، نقص هورمونی و متابولیک با تزریق انسولین جبران می شود. این داروها عملکرد سلولهای لوزالمعده را ترمیم می کنند ، که در نتیجه حداقل انسولین ترشح می کنند.
این دوره می تواند از دو هفته تا چند سال ادامه یابد. در نهایت ، با این حال ، به عنوان یک نتیجه از بین رفتن خود ایمنی باقیمانده سلول بتا ، مرحله بهبودی به پایان می رسد و نیاز به درمان جدی است.
دیابت قند غیر وابسته به انسولین (نوع 2)
این نوع آسیب شناسی زمانی ایجاد می شود که بافت های بدن قادر به جذب کافی قند یا انجام آن در حجم ناقص نیستند. یک مشکل مشابه نام دیگری دارد - نارسایی خارج از بدن. علت این پدیده ممکن است متفاوت باشد:
- تغییر در ساختار انسولین با ایجاد چاقی ، پرخوری ، شیوه زندگی بی تحرک ، فشار خون شریانی ، در سن و حضور اعتیاد ،
- نقص در عملکرد گیرنده های انسولین به دلیل نقض تعداد یا ساختار آنها ،
- تولید ناکافی قند توسط بافتهای کبدی ،
- آسیب شناسی داخل سلولی ، که در آن انتقال یک ضربه به اندام های سلولی از گیرنده انسولین دشوار است ،
- تغییر در ترشح انسولین در پانکراس.
طبقه بندی بیماری ها
بسته به شدت دیابت نوع 2 ، به موارد زیر تقسیم می شود:
- درجه خفیف این ویژگی با توانایی جبران کمبود انسولین ، منوط به استفاده از داروها و رژیمهای غذایی است که می تواند قند خون را در مدت زمان کوتاهی کاهش دهد ،
- درجه متوسط شما می توانید تغییرات متابولیکی را جبران کنید به شرطی که حداقل 2-3 دارو برای کاهش گلوکز استفاده شود. در این مرحله ، یک نارسایی متابولیک با آنژیوپاتی همراه خواهد بود ،
- مرحله شدید برای عادی سازی شرایط نیاز به استفاده از چندین وسیله کاهش قند و تزریق انسولین است. بیمار در این مرحله اغلب از عوارض رنج می برد.
دیابت نوع 2 چیست؟
تصویر بالینی کلاسیک دیابت شامل 2 مرحله است:
- مرحله سریع تخلیه فوری انسولین انباشته در پاسخ به گلوکز ،
- مرحله آهسته ترشح انسولین به منظور کاهش قند خون باقیمانده کند است. این کار بلافاصله پس از مرحله سریع شروع به کار می کند ، اما منوط به تثبیت کافی کربوهیدرات ها است.
اگر آسیب شناسی سلولهای بتا وجود داشته باشد که نسبت به اثرات هورمون پانکراس حساس نشوند ، عدم تعادل در میزان کربوهیدرات های خون به تدریج ایجاد می شود. در دیابت نوع 2 ، مرحله سریع به سادگی وجود ندارد ، و مرحله آهسته غالب است. تولید انسولین ناچیز است و به همین دلیل تثبیت فرآیند امکان پذیر نیست.
 هنگامی که عملکرد گیرنده انسولین یا مکانیسم های پس از گیرنده کافی نباشد ، هیپرینسولینمی ایجاد می شود. بدن با داشتن انسولین زیاد در خون ، مکانیسم جبران خسارت خود را شروع می کند که هدف از آن تثبیت تعادل هورمونی است. این علامت مشخصه حتی در همان ابتدای بیماری مشاهده می شود.
هنگامی که عملکرد گیرنده انسولین یا مکانیسم های پس از گیرنده کافی نباشد ، هیپرینسولینمی ایجاد می شود. بدن با داشتن انسولین زیاد در خون ، مکانیسم جبران خسارت خود را شروع می کند که هدف از آن تثبیت تعادل هورمونی است. این علامت مشخصه حتی در همان ابتدای بیماری مشاهده می شود.
تصویری آشکار از آسیب شناسی بعد از چند سال پرکاری قند خون مداوم ایجاد می شود. قند خون بیش از حد بر سلولهای بتا تأثیر منفی می گذارد. این امر به دلیل کاهش تولید و انسولین آنها می شود و باعث کاهش تولید انسولین می شود.
از نظر بالینی ، کمبود انسولین با تغییر در وزن و تشکیل کتواسیدوز آشکار می شود. علاوه بر این ، علائم دیابت از این نوع عبارتند از:
- پولییدپسی و پولیوریا. سندرم متابولیک به دلیل قند خون ، که باعث افزایش فشار خون اسمزی می شود ، ایجاد می شود. برای عادی سازی روند ، بدن شروع به از بین بردن فعالانه آب و الکترولیت ها می کند ،
- خارش پوست. خارش پوست به دلیل افزایش شدید اوره و کتون در خون ،
- اضافه وزن
مقاومت به انسولین باعث ایجاد عوارض زیادی ، اعم از اولیه و ثانویه خواهد شد. بنابراین ، گروه اول پزشکان عبارتند از: هایپرگلیسمی ، کاهش سرعت تولید گلیکوژن ، گلوکزوزوری ، مهار واکنش های بدن.
دسته دوم عوارض شامل موارد زیر است: تحریک ترشح لیپیدها و پروتئین برای تبدیل آنها به کربوهیدرات ها ، جلوگیری از تولید اسیدهای چرب و پروتئین ها ، کاهش تحمل نسبت به کربوهیدراتهای مصرفی ، اختلال در ترشح سریع هورمون پانکراس.
دیابت نوع 2 به اندازه کافی شایع است. به طور کلی ، شاخص های واقعی شیوع بیماری می تواند از حداقل رسمی 2-3 برابر فراتر رود.
علاوه بر این ، بیماران فقط پس از شروع عوارض جدی و خطرناک به دنبال کمک پزشکی هستند. به همین دلیل ، غدد درون ریز اصرار دارند که مهم است که معاینات منظم پزشکی را فراموش نکنید. آنها به شناسایی هر چه سریعتر مشکل کمک می کنند و به سرعت شروع به درمان می کنند.
روشی برای درمان دیابت غیر وابسته به انسولین

شماره ثبت اختراع: 1822767
. قند خون همچنان ادامه داشت ، اگرچه اندکی کاهش یافت: قند خون 8.1 میلی مول در لیتر. به بیمار روش دوره طب سوزنی طبق روش پیشنهادی تجویز شد. بعد از جلسه اول ، قند خون به 5.5 میلی مول در لیتر کاهش یافت. این نتیجه تحریک فعالیت لوزالمعده بود ، همانطور که با افزایش سطح انسولین ایمنی در خون به 130 میلی گرم در میلی لیتر از میلی لیتر از سطح اولیه (قبل از جلسه) -88 mcd / ml ، و محتوای پپتید C از 0.2 ng / ml به 0 مشهود است. 4 نانوگرم در میلی لیتر (بعد از جلسه). خانه ، و به نقاط Zu-san-li - با روش ترمز. گردآوری شده توسط A. Runova Tekhred M. Morgenthal Corrector M. Samborskaya سردبیر S. Kulakova سفارش 2168 امضا. VNIIIPI کمیته دولتی اختراعات و اکتشاف ها تحت کمیته دولتی علوم و فنون اتحاد جماهیر شوروی 113035 ، مسکو ، ژوئیه راوزسکایا.