جزایر لانگرهان لوزالمعده

جزیره لانگرهانس برای اولین بار در سال 1869 توصیف شد. کاشف این سازندهای مهم واقع در لوزالمعده (عمدتا در قسمت نوسانی) دانش آموز جوان رودولف ویرچو - پل لانگرهانس بود. این اولین کسی بود که تحت میکروسکوپ خوشه ای از سلولها را بررسی کرد که در ساختار مورفولوژیکی آنها با سایر بافتهای لوزالمعده تفاوت دارد.
همچنین مشخص شد که جزایر لانگرهان عملکرد غدد درون ریز را انجام می دهند. این کشف توسط K.P. اولسکو-استروگانوا انجام شد. در سال 1889 ، پیوند بین شکست جزایر لانگرهانس و توسعه دیابت قندی برای اولین بار برقرار شد.
جزایر لانگرهان چه می تواند باشد؟
در حال حاضر ، این ساختار قبلاً کاملاً مورد مطالعه قرار گرفته است. اکنون به خوبی شناخته شده است که این سازند دارای انواع مختلفی است. موارد زیر در حال حاضر شناخته شده است:
- سلولهای آلفا
- سلولهای بتا
- سلولهای دلتا
- سلولهای pp
- سلولهای اپسیلون

به لطف این تنوع است که سلولهای جزایر لانگرهان تمام وظایفی را که به آنها محول شده است ، انجام می دهند.
سلولهای آلفا
این تنوع حدود 15-20٪ از کل جزایر موجود لانگرهانس را تشکیل می دهد. وظیفه اصلی سلولهای آلفا تولید گلوکاگون است. این هورمون ماهیت لیپیدی دارد و نوعی آنتاگونیست انسولین است. هنگام آزاد شدن ، گلوکاگون به کبد می رود ، جایی که با تماس با گیرنده های ویژه ، تولید گلوکز را از طریق تجزیه گلیکوژن تنظیم می کند.
سلولهای بتا
جزایر Langerhans از این گونه رایج ترین است. آنها تقریباً 65-80٪ از کل را تشکیل می دهند. اکنون مشخص شده است که عملکرد اصلی آنها تولید یکی از مهمترین هورمون ها - انسولین است. این ماده یک آنتاگونیست گلوکاگون است. این ماده به فعال شدن تشکیل گلیکوژن و ذخیره آن در سلولهای کبدی و ماهیچه ای کمک می کند. در نتیجه این فرایند ، میزان قند خون کاهش می یابد.

سلولهای دلتا
جزایر لوزالمعده پانکراس از این نوع چندان رایج نیست. فقط 2-10٪ از کل وجود دارد. اکنون ویژگی های عملکردی آنها به خوبی شناخته شده است. مشخص شد که این سلول ها سوماتوستاتین را سنتز می کنند. عملکرد این ماده بیولوژیکی فعال سرکوب تولید هورمون رشد ، تیروتروپیک و هورمون آزاد کننده هورمون رشد است. یعنی مستقیماً روی هیپوتالاموس و همچنین غده هیپوفیز قدامی عمل می کند.

هر جزیره از این نوع لانگرهان ها پلی پپتید لوزالمعده را تولید می کنند. تا پایان ، عملکرد آن مورد مطالعه قرار نگرفته است. در حال حاضر ، وی به خواص سرکوب تولید آب لوزالمعده اعتبار می یابد. علاوه بر این ، اثر آن به آرامش عضلات صاف کیسه صفرا کمک می کند. در سال های اخیر ، میزان وابستگی به سطح تولید یک ماده خاص به تشکیل نئوپلاسم های بدخیم کاملاً مورد مطالعه قرار گرفته است. در نتیجه مشخص شد که با پیشرفت آنها ، سطح پلی پپتید لوزالمعده افزایش می یابد. بنابراین این ماده بیولوژیکی فعال می تواند نشانگر خوبی برای نئوپلاسم های بدخیم لوزالمعده در نظر گرفته شود.
سلولهای اپسیلون
چنین جزایر لانگرهان نادرترین هستند. از تعداد کل ، تعداد آنها کمتر از 1٪ است. وظیفه اصلی چنین سلولهایی تولید هورمونی به نام گرلین است. این ماده فعال عملکردهای زیادی دارد ، اما اثر نظارتی آن روی اشتها بیشتر مورد مطالعه قرار گرفته است.
درباره آسیب شناسی جزایر لانگرهانس
شکست این ساختارهای حساس تأثیر منفی بسیار جدی بر بدن دارد. در صورت تولید آنتی بادی های جزایر لانگرهانس ، تعداد دومی به تدریج کاهش می یابد. شکست بیش از 90٪ از سلول ها ، تولید انسولین را به سطح بسیار کمی کاهش می دهد. نتیجه آن ایجاد یک بیماری خطرناک مانند دیابت است. آنتی بادی های سلولهای جزایر لانگرهانس بیشتر در بیماران نسبتاً جوان ظاهر می شود.

پانکراتیت ، یک روند التهابی در لوزالمعده است ، می تواند به طور جدی به جمعیت این سلول های تولید کننده هورمون آسیب برساند.
چگونه سلولهای جزایر را ذخیره کنیم؟
برای این کار ، شما باید از کل لوزالمعده به عنوان یک کل مراقبت کنید. اول از همه ، لازم است از زیاده روی در مشروبات الکلی خودداری شود. واقعیت این است که از بین تمام محصولات غذایی که بیشترین تأثیر منفی بر لوزالمعده دارند ، اینها هستند. در صورت استفاده طولانی مدت از مشروبات الکلی ، فرد دچار پانکراس می شود و پیشرفت می کند ، که با گذشت زمان می تواند منجر به آسیب قابل توجهی به سلول های جزایر شود.
علاوه بر نوشیدنی های الکلی ، مقدار زیادی از مواد غذایی سرشار از چربی های حیوانی تأثیر نسبتاً منفی بر لوزالمعده دارد. در این حالت ، اگر بیمار مدت طولانی قبل از عید چیزی چیزی نخورد ، اوضاع وخیم تر می شود.

در صورتی که در حال حاضر یک روند التهابی مزمن در بافت لوزالمعده وجود داشته باشد ، لازم است با یک متخصص - درمانگر یا متخصص گوارش مشورت کنید. پزشکان این تخصص ها یک دوره منطقی از درمان را برای شما تجویز می کنند که می تواند پیشرفت تغییرات پاتولوژیک را به میزان قابل توجهی کند کند. در آینده ، هر سال ، باید یک سونوگرافی از لوزالمعده معاینه انجام شود ، که بهمراه سایر ارگان های حفره شکمی انجام می شود. علاوه بر این ، لازم است یک آزمایش خون بیوشیمیایی برای محتوای آمیلاز موجود در آن انجام شود.
برای تعیین ابتدای پیشرفت لوزالمعده مزمن ، علاوه بر مطالعات آزمایشگاهی و ابزاری ، این درمانگاه نیز کمک خواهد کرد. علائم اصلی این بیماری بروز درد در هیپوکندری چپ است. در عین حال ، این درد از خصایص حیرت انگیز برخوردار است و بیشتر پس از خوردن مقدار زیادی از مواد غذایی سرشار از چربی های حیوانی رخ می دهد. بعلاوه ممکن است بیمار بعد از خوردن غذا از احساس مداوم سنگینی در معده ناراحت شود. همه این علائم به اندازه کافی سریع او را رها می کنند یا شدت آن را در زمینه مصرف داروهای حاوی پانکراتین کاهش می دهند. در میان آنها ، محبوب ترین داروها کرئون ، مزم و پانکراتین بودند. اگر یک روند التهابی در بافت لوزالمعده اتفاق بیفتد ، بهتر است مصرف الکل را به طور کامل کنار بگذارید. واقعیت این است که حتی مقدار کمی از آن می تواند روند پاتولوژیک را تشدید کند و از این طریق به این اندام آسیب برساند.
جزیره لانگرهان چیست: مقصد
سلولهای غدد درون ریز در سراسر بدن قرار دارند. یکی از مکان های انباشت آنها لوزالمعده است. جزایر لانگرهانس در دم اندام واقع شده است. آنها خوشه های سلولی هستند که مواد فعال بیولوژیکی تولید می کنند - هورمون ها. اهمیت جزایر لانگرهانس بسیار زیاد است. این در تولید مقدار طبیعی هورمونهای لازم برای فرآیندهای متابولیک است. جزایر لوزالمعده پانکراس عملکردهای زیر را دارند:
- کنترل قند خون
- تنظیم فعالیت آنزیم.
- مشارکت در متابولیسم چربی.
به دلیل عملکرد طبیعی دستگاه جزایر ، شرایطی مانند دیابت قندی و هیپوگلیسمی ایجاد نمی شود. آسیب سلول در التهاب حاد و مزمن - پانکراتیت رخ می دهد.
ساختار بافت شناسی جزایر
جزیره لانگرهانس در قرن 19 کشف شد. این غلظت عناصر غدد درون ریز است. در کودکان ، این سازندها حدود 6٪ از کل سطح اندام را اشغال می کنند. در بزرگسالی ، قسمت غدد درون ریز کاهش می یابد و تنها 2٪ است. حدود یک میلیون جزیره لانگرهانس در پارانشیم دم قرار دارد. خون و عصب خون فراوانی دارند. هر جزیره از لوبول ها تشکیل شده است ، که توسط بافت پیوندی پوشیده شده اند. علاوه بر این ، در خارج از سازندهای غدد درون ریز قرار دارد. سلول های داخل جزایر در یک موزائیک چیده شده اند. فعالیت تجمع غدد درون ریز توسط اعصاب واگ و سمپاتیک ارائه می شود. در مرکز لوبول سلولهای عایق وجود دارد. آنها قند خون را پایین می آورند. در قسمت محیطی لوبولها سلولهای آلفا و دلتا قرار دارند. اولین تولید هورمون ضد انحصاری - گلوکاگون. مورد دوم برای تنظیم فعالیت غدد درون ریز و برون گرایانه ضروری است.
سلولهای جزایر لانگرهان چیست؟
در جزایر لانگرهان ، چندین نوع سلول تولید می شود. همه آنها در انتشار مواد فعال بیولوژیکی - پپتیدها و هورمونها نقش دارند. بیشتر جزایر لانگرهان توسط سلولهای بتا نشان داده می شوند. آنها در مرکز هر لوبول قرار دارند. این سلول ها از آنجا که انسولین تولید می کنند بسیار مهم هستند.
دومین سلول مهم آلفا لوزالمعده است. آنها یک چهارم جزیره را اشغال می کنند. سلولهای آلفا برای تولید گلوکاگون ضروری هستند. این هورمون یک آنتاگونیست انسولین است.
در قسمت محیطی جزایر لانگرهان ، سلولهای PP و دلتا تولید می شوند. تعداد نفر اول در حدود 1/20 قسمت است. عملکرد این سازندها تولید یک پلی پپتید لوزالمعده است. سلولهای دلتا برای تولید سوماتوستاتین ضروری هستند. این ماده در تنظیم متابولیسم کربوهیدرات ها نقش دارد.
بازسازی سلولهای جزایر دشوار است. بنابراین ، هنگامی که این سازه ها آسیب دیده ، بازگرداندن عملکرد آنها غیرممکن است.
فعالیت هورمونی جزایر لانگرهانس
با وجود این که جزیره لانگرهانس کوچک است و تنها بخش کوچکی از پانکراس را اشغال می کند ، اهمیت این قطعه بسیار مهم است. در آن ، شکل گیری مهمترین هورمونهای دخیل در فرآیندهای متابولیک. جزایر لانگرهانس انسولین ، گلوکاگون ، سوماتواستاتین و پلی پپتید پانکراس تولید می کنند.
2 هورمون اول برای زندگی ضروری هستند. انسولین باعث تجزیه گلوکز به ترکیبات مولکولی کوچکتر می شود. در نتیجه میزان قند خون کاهش می یابد. بعلاوه ، انسولین در متابولیسم چربی ها نقش دارد. به دلیل عملکرد این هورمون ، گلیکوژن در بافت کبد و ماهیچه جمع می شود. انسولین تأثیر آنابولیک در متابولیسم کلی دارد ، یعنی باعث تسریع در کلیه فرایندها می شود.
گلوکاگون تأثیر متضاد دارد. این هورمون در مقادیر کمتری در مقایسه با انسولین تولید می شود. درگیر در گلوکونوژنز است. قند در بدن ضروری است ، زیرا منبع انرژی است.
سوماتوستاتین تولید آنزیم ها و هورمون های هضم را تنظیم می کند. تحت تأثیر این ماده ، تولید گلوکاگون و انسولین کاهش می یابد. سلولهای PP بسیار کمی در جزایر Langerhans وجود دارد ، اما پلی پپتید پانکراس برای بدن لازم است. وی در تنظیم ترشح غدد گوارشی (کبد ، معده) نقش دارد. با کمبود فعالیت هورمونی ، بیماری های شدید ایجاد می شود.
آسیب به لوزالمعده غدد درون ریز
اختلال در فعالیت سلولهای جزایر به دلایل مختلف می تواند رخ دهد. اغلب عدم موفقیت این ساختارها به ناهنجاری های مادرزادی (آسیب شناسی ژنتیکی) اشاره دارد. ضایعات بدست آمده از جزایر لانگرهان به دلیل عفونت های ویروسی و باکتریایی ، مسمومیت مزمن با الکل ، بیماری های عصبی ایجاد می شود.
کمبود انسولین منجر به دیابت نوع یک می شود. این بیماری در دوران کودکی و جوانی رخ می دهد. افزایش قند خون منجر به آسیب رساندن به رگ های خونی و اعصاب می شود. با کمبود سلولهای جزایر دیگر ، وضعیت هیپوگلیسمی ایجاد می شود و باعث افزایش تولید آبهای گوارشی می شود. افزایش تولید هورمون ها با تومورهای خوش خیم دم لوزالمعده اتفاق می افتد.
پیوند جزایر لانگرهانس
یک روش برای درمان دیابت درمان جایگزینی انسولین است. در سالهای اخیر روشهای جایگزین تدوین شده است. این موارد شامل معرفی لوزالمعده مصنوعی و پیوند سلولهای جزایر است. در عمل مشخص شد که ساختارهای تولید کننده هورمون در بدن جدید ریشه می گیرند. در این حالت ، متابولیسم کربوهیدرات می تواند به طور کامل بهبود یابد. پیوند جزایر لانگرهانس هنوز در عمل کاربردهای گسترده ای نداشته است.
جزایر پانکراس (لانگرهانس)
لوزالمعده از اجزای اگزوکرین و غدد درون ریز تشکیل شده است. قسمت اگزوکرونیک در بخش "اندامهای هضم کننده" توضیح داده شده است. قسمت غدد درون ریز توسط گروههای جزایر لوزالمعده (جزایر لانگرهان) تشکیل می شود ، که توسط خوشه های سلولی سرشار از مویرگها تشکیل می شوند. تعداد کل جزایر بین 1-2 میلیون متغیر است (1-2٪ از جرم کل غده) ، و قطر هر یک از آنها در میکرون است. این دستگاه پیچیده داخل ترشحی داخل رحمی است که از خوشه های بیضی سلولهای غدد درون ریز در انواع مختلف تشکیل شده است: هورمون گلوکاگون ، تنظیم کننده متابولیسم کربوهیدرات و متابولیسم چربی (در دستگاه گوارش نیز تشکیل می شود) در سلول های آلفا تشکیل می شود و انسولین تنظیم کننده متابولیسم کربوهیدرات در سلول های بتا است. متابولیسم پروتئین و متابولیسم چربی ، در سلولهای D (سلولهای قطعی) ، ظاهراً سه هورمون سنتز می شوند - سوماتوستاتین ، پانکراگاسترین و ترشح. سلول های جزایر حاوی بسیاری از گرانول های پوشیده از غشاء هستند. سلولهای بتا (80-60٪) ، سلولهای آلفا 10 تا 30٪) ، سلولهای D- حدود 10٪) غالب هستند.
جزایر لوزالمعده مسئول عملکرد غدد درون ریز آن در سراسر پارانشیم لوزالمعده پراکنده است. هر جزیره بالغ علاوه بر سلولهای آلفا ، بتا و دلتا ، دارای سلولهای PP (تولید پلی پپتید پانکراس) است.
همه انواع سلول ها مقادیر کمی از سایر پپتیدهای بیولوژیکی فعال تولید می کنند.
جزایر در حال توسعه حاوی سلولهای نابالغ هستند که تعدادی از هورمونهای پپتید اضافی از جمله گاسترین ، VIP ، ACTH ترشح می کنند.
تومور ممکن است از هر نوع سلول بروز کند.
تومورهای حاصل از سلولهای جزایر معمولاً یک یا چند هورمون ترشح می کنند و نشانگان مشخصه آن را آشکار می کنند (جدول 95.2).
جزایر لانگرهان چیست
جزایر Langerhans واقع در لوزالمعده انباشت سلولهای غدد درون ریز مسئول تولید هورمون ها است. در اواسط قرن XIX ، دانشمند پاول لانگرهانسک گروههای کاملی از این سلول ها را کشف کرد ، بنابراین خوشه ها به نام او نامگذاری شدند.
در طول روز ، جزایر 2 میلی گرم انسولین تولید می کنند.
سلولهای جزایر عمدتاً در ناحیه کبدی لوزالمعده متمرکز می شوند. جرم آنها 2٪ از کل وزن غده است. تعداد کل جزایر موجود در پارانشیم تقریباً است.
یک واقعیت جالب اینجاست که در نوزادان ، توده جزایر 6٪ از وزن لوزالمعده را اشغال می کند.
با گذشت سالها ، نسبت ساختارهای بدن که فعالیت غدد درون لوزالمعده دارند ، کاهش می یابد. با گذشت 50 سال از وجود انسان ، فقط 1-2٪ از جزایر باقی می مانند
خوشه ها از چه سلول ساخته شده اند؟
جزایر لانگرهانس سلولهایی با عملکرد و مورفولوژی متفاوت دارند.
لوزالمعده غدد درون ریز شامل:
- سلولهای آلفا تولید کننده گلوکاگون. این هورمون یک آنتاگونیست انسولین است و قند خون را افزایش می دهد. سلولهای آلفا 20٪ سلولهای باقیمانده را اشغال می کنند ،
- سلولهای بتا مسئول سنتز آملین و انسولین هستند ، آنها٪ 80 از وزن جزایر را اشغال می کنند ،
- تولید سوماتوستاتین ، که می تواند راز سایر اعضای بدن را مهار کند ، توسط سلولهای دلتا تهیه می شود. جرم آنها از 3 تا 10٪ است ،
- سلولهای PP برای تولید پلی پپتید لوزالمعده ضروری هستند. این هورمون عملکرد ترشحی معده را تقویت کرده و ترشح پارانشیم را سرکوب می کند ،
- گرلین ، که مسئولیت بروز گرسنگی در فرد را بر عهده دارد ، توسط سلولهای اپسیلون تولید می شود.
جزایر چطور چیده شده اند و برای چه مواردی قرار دارند
عملکرد اصلی که جزایر Langerhans انجام می دهد ، حفظ سطح صحیح کربوهیدرات ها در بدن و کنترل سایر اندام های غدد درون ریز است. این جزایر توسط اعصاب دلسوز و واگوس مجذوب می شوند و به وفور با خون تأمین می شوند.
جزایر لانگرهان در لوزالمعده از ساختار پیچیده ای برخوردار است. در حقیقت ، هر یک از آنها یک آموزش عملکردی تمام عیار فعال هستند. ساختار این جزیره مبادله ای بین مواد فعال بیولوژیکی پارانشیم و غدد دیگر ایجاد می کند. این برای ترشح هماهنگ انسولین لازم است.
سلول های جزایر با هم مخلوط می شوند ، یعنی به صورت موزاییک چیده شده اند. جزیره بالغ در لوزالمعده دارای سازماندهی مناسب است. این جزیره از لوبولهایی تشکیل شده است که بافت همبند را محاصره می کنند ، مویرگ های خونی درون سلول ها عبور می کنند.
سلول های بتا در مرکز لوبول ها قرار دارند ، در حالی که سلول های آلفا و دلتا در بخش محیطی قرار دارند. بنابراین ، ساختار جزایر لانگرهانس کاملاً به اندازه آنها بستگی دارد.
چرا آنتی بادی ها علیه جزایر تشکیل می شوند؟ عملکرد غدد درون ریز آنها چیست؟ معلوم می شود که مکانیسم تعامل سلول های جزایر یک مکانیسم بازخورد ایجاد می کند و سپس این سلول ها بر سایر سلول های مستقر در مجاورت تأثیر می گذارند.
- انسولین عملکرد سلولهای بتا را فعال کرده و سلولهای آلفا را مهار می کند.
- سلول های آلفا گلوکاگون را فعال می کنند و بر روی سلول های دلتا عمل می کنند.
- سوماتوستاتین کار سلول های آلفا و بتا را مهار می کند.
مهم! در صورت خراب شدن مکانیسم های ایمنی بدن بدن در مقابل سلول های بتا تشکیل می شود. سلول ها از بین می روند و منجر به بیماری مهیبی به نام دیابت می شوند.
پیوند چیست و چرا مورد نیاز است
یک جایگزین ارزشمند برای پیوند پارانشیم غده ، پیوند دستگاه جزایر است. در این حالت ، نصب اندام مصنوعی لازم نیست. پیوند به دیابتی ها این فرصت را می دهد تا ساختار سلول های بتا را ترمیم کنند و پیوند لوزالمعده به طور کامل لازم نیست.
براساس مطالعات بالینی ، ثابت شد كه در بیماران دیابتی نوع 1 ، كه سلولهای جزایر اهدا كرده اند ، تنظیم سطح كربوهیدرات كاملاً احیا شده است. برای جلوگیری از رد بافت اهدا کننده ، چنین بیمارانی تحت درمان سرکوب کننده سیستم ایمنی قرار گرفته اند.
برای ترمیم جزایر ، ماده دیگری وجود دارد - سلولهای بنیادی. از آنجا که ذخایر سلولهای اهدا کننده نامحدود نیست ، چنین جایگزینی بسیار مهم است.
بازگرداندن حساسیت سیستم ایمنی بدن برای بدن بسیار مهم است ، در غیر این صورت سلولهای تازه پیوند یافته پس از مدتی رد یا نابود می شوند.
امروزه درمان ترمیمی به سرعت در حال پیشرفت است ، در همه زمینه ها تکنیک های جدیدی ارائه می دهد. پیوند زنو نیز نویدبخش است - پیوند انسان از لوزالمعده خوک.
عصاره پارانشیم خوک حتی قبل از کشف انسولین برای درمان دیابت مورد استفاده قرار گرفت. به نظر می رسد که غدد انسان و خوک تنها در یک اسید آمینه متفاوت است.
از آنجا که دیابت در نتیجه صدمه به جزایر لانگرهانس ایجاد می شود ، مطالعه آنها چشم اندازهای خوبی برای درمان موثر بیماری دارد.
عملکردها و آسیب شناسی جزایر لانگرهان: عدم موفقیت هورمونهای ترشح شده
بافت لوزالمعده توسط دو نوع تشکیل سلول تشکیل شده است: acinus ، که آنزیم ها را تولید می کند و در عملکرد دستگاه گوارش شرکت می کند ، و جزایر لانگرهان که عملکرد اصلی آن سنتز هورمون ها است.
جزایر کمی در خود غده وجود دارد: آنها 1-2٪ از کل اعضای بدن را تشکیل می دهند. سلولهای جزایر لانگرهانس از نظر ساختار و عملکرد متفاوت هستند. 5 نوع از آنها وجود دارد. آنها مواد فعال ترشح می کنند که تنظیم کننده سوخت و ساز بدن ، هضم کربوهیدرات ها هستند و می توانند در پاسخ به واکنشهای استرس شرکت کنند.
انواع سلولهای جزایر و عملکرد آنها
سلولهای OL در ساختار مورفولوژیکی ، عملکردهای انجام شده و محلی سازی متفاوت هستند. در داخل جزایر آنها چیدمان موزاییکی دارند. هر جزیره دارای یک سازمان منظم است. در مرکز سلولهایی هستند که انسولین ترشح می کنند. در لبه ها - سلول های محیطی ، که تعداد آنها بستگی به اندازه OL دارد. برخلاف acini ، OL مجاری خود را ندارد - هورمون ها مستقیماً از طریق مویرگ ها وارد جریان خون می شوند.
5 نوع اصلی سلول OL وجود دارد. هریک از آنها نوع خاصی از هورمونها را تنظیم می کند ، هضم ، کربوهیدرات و متابولیسم پروتئین را تنظیم می کند:
جزیره پانکراس لانگرهانس. جزایر لانگرهانس: انواع سلول ، ویژگی ها و ساختار
لوزالمعده یکی از اندامهای حیاتی به حساب می آید. او نه تنها به طور فعال در روند هضم غذا شرکت می کند ، بلکه عملکرد غدد درون ریز نیز دارد. ترشح داخلی به لطف سلولهای ویژه واقع در دم این سازند آناتومیک انجام می شود. مکانی که هورمونهای پانکراس تولید می شود جزیره لانگرهانس نامیده می شود. این شکل گیری آناتومیکی از اهمیت عملکردی زیادی برخوردار است. به لطف آن ، متابولیسم کربوهیدرات تأمین می شود.

چه آسیب شناسی در دستگاه جزایر ایجاد می شود؟
بسیاری از خوانندگان ما پس از شکست در لوزالمعده ، از این تغییر خوشحال هستند! آنچه که گالینا ساوینا می گوید: "تنها درمان مؤثر در برابر پانکراتیت ، یک درمان طبیعی بود: من برای شب دو قاشق غذاخوری درست کردم ..."
شکست سلول های OL منجر به عواقب جدی می شود. با توسعه فرآیند خود ایمنی و ایجاد آنتی بادی (AT) به سلولهای OL ، تعداد همه این عناصر ساختاری به شدت کاهش می یابد. شکست 90٪ سلول ها با کاهش شدید سنتز انسولین همراه است که منجر به دیابت می شود. ایجاد آنتی بادی به سلولهای جزایر پانکراس عمدتا در افراد جوان رخ می دهد.
پانکراتیت ، یک فرآیند التهابی در بافت های لوزالمعده ، در رابطه با آسیب به جزایر منجر به عواقب جدی می شود. غالباً به شکل نکروز لوزالمعده به صورت شدید پیش می رود که در آن مرگ کلی سلول های اندام وجود دارد.
تعیین آنتی بادی های جزایر لانگرهانس
اگر بنا به دلایلی نقص در بدن رخ دهد و تولید فعال آنتی بادی در برابر بافت های خود آغاز شود ، این منجر به عواقب غم انگیز می شود. هنگامی که سلولهای بتا در معرض آنتی بادی ها هستند ، دیابت نوع I با تولید ناکافی انسولین همراه است. هر نوع آنتی بادی تولید شده علیه نوع خاصی از پروتئین عمل می کند. در مورد جزایر Langerhans ، این ساختارهای بتا سلول هستند که مسئول سنتز انسولین هستند. این روند به تدریج پیش می رود ، سلول ها کاملاً می میرند ، متابولیسم کربوهیدرات مختل می شود و با تغذیه طبیعی ، بیمار ممکن است در اثر گرایش های برگشت ناپذیر در اندام ها ، از گرسنگی بمیرد.
روش های تشخیصی برای تعیین وجود آنتی بادی های انسولین در بدن انسان تدوین شده است. نشانه های این مطالعه عبارتند از:
- سابقه خانوادگی چاقی ،
- هرگونه آسیب شناسی از لوزالمعده ، از جمله جراحات ،
- عفونت های شدید: بیشتر ویروسی ، که می تواند باعث ایجاد یک فرآیند خود ایمنی شود ،
- استرس شدید ، استرس روانی.
3 نوع آنتی بادی وجود دارد که به دلیل تشخیص دیابت نوع I:
- دکربوکسیلاز اسید گلوتامیک (یکی از اسیدهای آمینه ضروری در بدن) ،
- برای توسعه انسولین ،
- به سلولهای OL
این نشانگرهای خاص و عجیب و غریب هستند که باید در برنامه معاینه بیماران دارای فاکتورهای خطر موجود درج شوند. از محدوده مطالعات ذکر شده ، شناسایی آنتی بادی های به اسید آمینه گلوتامین آمین یک علامت تشخیصی اولیه دیابت است. آنها هنگامی ظاهر می شوند که علائم بالینی این بیماری هنوز از بین نرود. آنها عمدتا در سنین پایین مشخص می شوند و می توان از آنها برای شناسایی افراد مستعد ابتلا به بیماری استفاده کرد.
پیوند سلولهای جزایر
پیوند سلولهای OL جایگزینی برای پیوند لوزالمعده یا قسمت آن و همچنین نصب اندام مصنوعی است. این به دلیل حساسیت و حساسیت بالای بافت لوزالمعده به هر گونه اثر است: به راحتی آسیب دیده و به سختی عملکردهای خود را بازیابی می کند.
پیوند جزایر امروزه در مواردی که درمان جایگزینی انسولین به حد خود رسیده و ناکارآمد می شود ، درمان دیابت نوع I را امکان پذیر می کند. این روش برای اولین بار توسط متخصصان کانادایی مورد استفاده قرار گرفت و شامل معرفی سلولهای دهنده دهنده غدد درون ریز سالم به ورید پورتال پورتال کبد با استفاده از سوند است. هدف این است که سلولهای بتا خود را نیز فعال کند.
با توجه به عملکرد پیوند ، مقدار انسولین لازم برای حفظ سطح قند خون طبیعی به تدریج سنتز می شود. این اثر به سرعت رخ می دهد: با یک عمل موفقیت آمیز ، پس از دو هفته وضعیت بیمار شروع به بهبود می کند ، درمان جایگزینی از بین می رود ، لوزالمعده شروع به سنتز مستقل انسولین می کند.
خطر جراحی رد سلولهای پیوندی است. از مواد Cadaveric استفاده می شود که مطابق با تمام پارامترهای سازگاری بافت با دقت انتخاب می شوند. از آنجا که حدود 20 چنین معیار وجود دارد ، آنتی بادی های موجود در بدن می توانند به تخریب بافت لوزالمعده منجر شوند. بنابراین ، با استفاده از داروهای مناسب با هدف کاهش پاسخ ایمنی ، نقش مهمی ایفا می کند. داروها به گونه ای انتخاب می شوند که می توانند برخی از آنها را که به تولید آنتی بادی ها کمک می کنند ، به سلولهای جزایر پیوند شده لانگرهان منتقل کنند. این امر خطر لوزالمعده را به حداقل می رساند.
در عمل ، پیوند سلول های پانکراس در دیابت نوع 1 نتایج خوبی را نشان می دهد: هیچ مرگ و میر ثبت نشده پس از چنین عمل جراحی مشاهده نشده است. تعداد معینی از بیماران دوز انسولین را به میزان قابل توجهی کاهش داده اند ، و بخشی از بیماران تحت عمل نیاز به آن متوقف نشده است. سایر عملکردهای آشفته اندام ترمیم شدند و وضعیت سلامتی بهبود یافت. بخش قابل توجهی به یک سبک زندگی عادی برگشته است ، که به ما امکان می دهد تا به یک پیش آگهی مطلوب دیگر امیدوار باشیم.
مانند پیوند اعضای دیگر بدن ، جراحی لوزالمعده علاوه بر رد ، با عوارض جانبی دیگر به دلیل نقض درجات مختلف فعالیت ترشحی لوزالمعده خطرناک است. در موارد شدید ، این منجر به:
- به اسهال لوزالمعده ،
- به حالت تهوع و استفراغ
- به کم آبی شدید ،
- به سایر علائم سوء هاضمه ،
- به فرسودگی عمومی
پس از انجام عمل ، بیمار باید به طور مداوم داروهای سرکوب کننده سیستم ایمنی را در طول زندگی دریافت کند تا از رد سلول های خارجی جلوگیری کند. عمل این داروها با هدف کاهش پاسخ های ایمنی - تولید آنتی بادی ها انجام می شود. به نوبه خود ، عدم ایمنی خطر ابتلا به هر نوع عفونت حتی ساده را افزایش می دهد که می تواند پیچیده باشد و عواقب جدی را به همراه داشته باشد.
تحقیقات در مورد پیوند لوزالمعده از خوک در حال انجام است - زنوگرافت. مشخص است که آناتومی غده و انسولین بز گوشتی نزدیکترین به انسان است و با یک اسید آمینه با آن تفاوت دارد. قبل از کشف انسولین ، از عصاره پانکراس خوک در درمان دیابت شدید استفاده می شد.
چرا پیوند دارند؟
بافت پانکراس آسیب دیده ترمیم نمی شود. در موارد دیابت پیچیده ، وقتی بیمار در دوزهای بالای انسولین قرار دارد ، چنین مداخلات جراحی موجب صرفه جویی در بیمار می شود ، فرصتی برای ترمیم ساختار سلول های بتا فراهم می کند. در تعدادی از مطالعات بالینی ، این سلول ها از اهدا کنندگان پیوند داده می شوند. در نتیجه ، تنظیم متابولیسم کربوهیدرات ترمیم شد. علاوه بر این ، بیماران مجبور به انجام سرکوب کننده سیستم ایمنی قدرتمند هستند تا بافت اهدا کننده رد نشود.
در تمام بیماران مبتلا به دیابت نوع I پیوند سلول ها مشاهده نمی شود. نشانه های دقیق وجود دارد:
- عدم نتیجه درمان محافظه کارانه کاربردی ،
- مقاومت به انسولین
- اختلالات متابولیک در بدن ،
- عوارض شدید بیماری.
عملیات کجا انجام می شود و هزینه آن چقدر است؟
روش جایگزینی جزایر لانگرهانس به طور گسترده در ایالات متحده انجام می شود - بنابراین درمان هر نوع دیابت در مراحل اولیه. این کار توسط یکی از موسسات تحقیقات دیابت در میامی انجام می شود. به طور کامل درمان دیابت از این طریق امکان پذیر نیست ، اما یک اثر درمانی مناسب حاصل می شود و خطرات عوارض جدی به حداقل می رسد.
قیمت چنین مداخله ای در حدود 100 هزار دلار است. توانبخشی بعد از عمل و سرکوب کننده سیستم ایمنی بین 5 تا 20 هزار دلار است. هزینه این درمان بعد از عمل بستگی به واکنش بدن به سلولهای پیوند یافته دارد.
تقریباً بلافاصله پس از دستکاری ، لوزالمعده به طور معمول مستقل عمل می کند و به تدریج کار آن بهبود می یابد. روند بهبود تقریباً 2 ماه طول می کشد.
چگونه برای جلوگیری از پانکراس برای همیشه؟
برای پیشگیری و درمان بیماری های لوزالمعده ، خوانندگان ما چای صومعه را توصیه می کنند. یک ترکیب منحصر به فرد ، که شامل 9 گیاه دارویی مفید برای لوزالمعده است که هر یک از آنها نه تنها مکمل بلکه عملکرد یکدیگر را تقویت می کند. با استفاده از آن ، شما نه تنها تمام علائم التهاب غده را از بین می برید ، بلکه از علت بروز آن برای همیشه خلاص می شوید.
- ترک الکل و سیگار کشیدن ،
- محرومیت از غذای آشغال
- فعالیت بدنی
- به حداقل رساندن استرس حاد و اضافه بار روانی.
بیشترین صدمه به لوزالمعده توسط الکل ایجاد می شود: بافت لوزالمعده را از بین می برد ، منجر به نکروز لوزالمعده می شود - مرگ و میر کلی انواع سلول های اندام که نمی توانند ترمیم شوند.
مصرف بیش از حد غذاهای چرب و سرخ شده منجر به عواقب مشابه می شود ، به خصوص اگر این اتفاق روی معده خالی و به طور مرتب انجام شود. بار لوزالمعده به میزان قابل توجهی افزایش می یابد ، تعداد آنزیم های لازم برای هضم مقدار زیادی چربی افزایش می یابد و اندام را کاهش می دهد. این منجر به فیبروز و تغییر در سلولهای باقیمانده غده می شود.
بنابراین ، در کمترین علامت اختلال عملکرد دستگاه گوارش ، با هدف اصلاح به موقع تغییرات و پیشگیری زودهنگام از عوارض ، توصیه می شود با متخصص گوارش یا درمانگر مشورت کنید.
نادیده گرفتن یا درمان نادرست پانکراس می تواند عواقب وحشتناکی را به همراه داشته باشد:
- دیابت قندی
- نارسایی کبد و کلیه ،
- انکولوژی ، که با برداشتن جزئی یا کامل لوزالمعده تهدید می شود.
ناگفته نماند ، رژیمهای غذایی سخت ، مصرف مداوم آنزیم ها و دوره های تشدید ، وقتی نیرویی برای زندگی وجود ندارد. رئیس کل گوارش فدراسیون روسیه می گوید: "اما فراموش کردن پانکراس برای همیشه ممکن است."
پیشینه تاریخی
پل لانگرهانس ، به عنوان یک دانشجوی پزشکی ، با رودولف ویرچو همکاری داشت ، در سال 1869 خوشه سلولهای لوزالمعده را که از بافت اطراف آن متفاوت بودند ، توصیف کرد و بعداً به نام وی نامگذاری شد. در سال 1881 ، K.P. Ulezko-Stroganova برای اولین بار به نقش غدد درون ریز این سلول ها اشاره کرد. عملکرد افزایشی لوزالمعده در استراسبورگ (آلمان) در کلینیک بزرگترین دیابولوژیست Naunin Mering و Minkowski در سال 1889 به اثبات رسید - دیابت پانکراس کشف شد و نقش لوزالمعده در پاتوژنز آن برای اولین بار اثبات شد.دانشمند روسی L. V. Sobolev (1919-1976) در مقاله خود "در مورد مورفولوژی لوزالمعده با بستن مجرای آن در دیابت و برخی شرایط دیگر" نشان داد که بستن مجرای دفع لوزالمعده منجر به بخش غدد (برون برقی) می شود ، در حالی که جزایر پانکراس دست نخورده باقی مانده است. براساس آزمایشات ، L. V. Sobolev نتیجه گرفت: "عملکرد جزایر لوزالمعده تنظیم متابولیسم کربوهیدرات در بدن است. مرگ جزایر لوزالمعده و از بین رفتن این عملکرد باعث ایجاد یک وضعیت دردناک - دیابت قندی می شود. "
در آینده به لطف تعدادی از مطالعات انجام شده توسط فیزیولوژیست ها و پاتوفیزیولوژیست ها در کشورهای مختلف (پانکراسکتومی ، نکروز انتخابی پانکراس پانکراس پانکراس توسط ترکیب شیمیایی آلوکسان) ، اطلاعات جدیدی درباره عملکرد افزایشی لوزالمعده بدست آمد.
در سال 1907 ، لین و برشلی (دانشگاه شیکاگو) بین دو نوع سلول جزایر که آنها را نوع A (سلول های αفا) و نوع B (سلول های بتا) می نامیدند ، تفاوت نشان دادند.
در سال 1909 ، محقق بلژیکی ژان دو میر پیشنهاد داد تا محصول ترشح سلولهای بتا جزایر انسولین لانگرهانس (از لاتین) باشد. انسول - جزایر). با این حال ، شواهد مستقیم از تولید هورمون که بر متابولیسم کربوهیدرات تأثیر می گذارد ، قابل شناسایی نبودند.
در سال 1921 ، فردریک جراح جوان کانادایی و معاون دانشجویی پزشکی وی چارلز بهترین موفق به جداسازی انسولین در آزمایشگاه فیزیولوژی پروفسور J. Macleod در دانشگاه تورنتو شدند.
در سال 1962 ، مارلین و همكاران دریافتند كه عصاره های آب لوزالمعده می توانند قند خون را افزایش دهند. ماده ای که باعث قند خون می شود "فاکتور گلیکوژنولیتیک قند خون" نامیده شد. گلوکاگون بود - یکی از اصلی ترین آنتاگونیست های انسولین فیزیولوژیکی.
در سال 1967 ، دوناتان اشتاینر و همكاران (دانشگاه شیكاگو) پروتئین پیش ساز انسولین پیش ساز را كشف كردند. آنها نشان دادند که سنتز انسولین توسط سلولهای بتا با تشکیل یک مولکول پروینسولین آغاز می شود ، که از آن پس ، در صورت لزوم ، مولکول C- پپتید و انسولین بریده می شود.
در سال 1973 ، جان انسیک (دانشگاه واشنگتن) و همچنین شماری از دانشمندان آمریکایی و اروپا کارهایی را در زمینه تصفیه و سنتز گلوکاگون و سوماتوستاتین انجام دادند.
در سال 1976 ، گودورث و بوتاگو با کشف دو نوع هورمون: یک عارضه ژنتیکی در یک مولکول انسولین را کشف کردند: طبیعی و غیر طبیعی. دومی آنتاگونیست انسولین طبیعی است.
در سال 1979 به لطف تحقیقات Lacy & Kemp و همكاران ، پیوند جزایر جداگانه و سلولهای بتا امكان پذیر شد ، امكان جدا كردن جزایر از قسمت اگزوكرین لوزالمعده و پیوند در یك آزمایش وجود داشت. در سال 1979-1980 در طول پیوند سلول های بتا ، یک سد خاص گونه بر طرف شد (سلول های حیوانات آزمایشگاهی سالم در یک حیوان بیمار از گونه های مختلف کاشته شدند).
در سال 1990 برای اولین بار پیوند سلولهای جزایر پانکراس برای بیمار مبتلا به دیابت انجام شد.
لوزالمعده چه هورمونی ایجاد می کند؟
لوزالمعده در درجه اول در تولید آبمیوه های گوارشی و متشکل از آنزیم های قدرتمند نقش دارد. آنزیم ها پس از خوردن در روده کوچک رها می شوند تا هضم مواد غذایی را دریافت کنند.
آهن همچنین هورمونهای مختلفی را تولید می کند که سطح گلوکز خون را کنترل می کند.
غده از سلولهای غدد درون ریز هورمون تولید می کند - این سلول ها در خوشه هایی معروف به جزایر لانگرهان جمع می شوند و آنچه را که در خون اتفاق می افتد کنترل می کنند.
سلول ها می توانند در صورت لزوم هورمون ها را مستقیماً درون خون آزاد کنند.
به ویژه ، وقتی قند خون بالا می رود ، سلول ها به خصوص انسولین هورمون تولید می کنند.
بنابراین ، لوزالمعده انسولین هورمون تولید می کند.
این هورمون به بدن کمک می کند سطح قند خون را پایین بیاورد و قند را به چربی ، ماهیچه ، کبد و سایر بافت های بدن هدایت می کند ، جایی که می تواند در صورت نیاز از آن برای تولید انرژی استفاده کند.
سلولهای آلفا در جزایر لانگرهان هورمون مهم دیگری به نام گلوکاگون تولید می کنند. این اثر ضد انسولین دارد و به آزاد شدن انرژی در خون و افزایش قند خون کمک می کند.
گلوکاگون و انسولین برای کنترل تعادل گلوکز در خون با یکدیگر کار می کنند.
ویژگی کلی

کار اصلی پانکراس تولید آنزیم های لوزالمعده است. با کمک آنها فرآیندهای هضم را تنظیم می کند.
آنها به تجزیه پروتئین ها ، چربی ها و کربوهیدرات هایی که همراه با مواد غذایی هستند کمک می کنند. بیش از 97٪ سلولهای غده مسئول تولید آنها هستند.
و فقط حدود 2٪ از حجم آن توسط بافتهای ویژه اشغال شده است ، "جزایر لانگرهان" نامیده می شود. آنها گروههای کوچکی از سلولها هستند که هورمون تولید می کنند.
این خوشه ها به طور مساوی در سراسر پانکراس قرار دارند.
سلولهای غدد درون ریز برخی از هورمونهای مهم را تولید می کنند. آنها ساختار و فیزیولوژی خاصی دارند.
این قسمت های غده ای که جزایر لانگرهان در آن قرار دارند ، مجاری دفع کننده ندارند. فقط بسیاری از رگ های خونی ، جایی که هورمون ها به طور مستقیم دریافت می شوند ، آنها را احاطه کرده اند.
با وجود آسیب شناسی های مختلف لوزالمعده ، این خوشه های سلول های غدد درون ریز غالباً آسیب می بینند. به همین دلیل ممکن است میزان هورمونهای تولید شده کاهش یابد که این امر بر وضعیت عمومی بدن تأثیر منفی می گذارد.
ساختار جزایر لانگرهانس ناهمگن است. دانشمندان تمام سلولهای تشکیل دهنده آنها را به 4 نوع تقسیم کردند و دریافتند که هرکدام هورمونهای خاصی تولید می کنند:
- تقریبا 70٪ از حجم جزایر لانگرهانس توسط سلولهای بتا که سنتز انسولین را تشکیل می دهند ، اشغال شده است ،
- در درجه دوم سلول های آلفا قرار دارند که 20٪ از این بافت ها را تشکیل می دهند ، آنها گلوکاگون تولید می کنند ،
- سلولهای دلتا سوماتواستاتین تولید می کنند ، آنها کمتر از 10٪ مساحت جزایر لانگرهان را تشکیل می دهند ،
- حداقل از همه ، سلولهای PP وجود دارند که وظیفه تولید پلی پپتید لوزالمعده را دارند ،
- علاوه بر این ، در مقدار کمی ، قسمت غدد لوزالمعده هورمونهای دیگر را سنتز می کند: گاسترین ، تیرولبرین ، آمیلین ، پپتید.
مشکلات هورمونی احتمالی
بین وعده های غذایی ، لوزالمعده انسولین تولید نمی کند و این به بدن اجازه می دهد تا به تدریج ذخایر انرژی ذخیره شده را در صورت نیاز به خون بازگرداند.
سطح گلوکز خون در هر زمان بسیار پایدار است و این به بدن اجازه می دهد جریان ثابت انرژی داشته باشد. این انرژی برای متابولیسم ، ورزش و به شکل "سوخت" برای مغز كه بر روی گلوكز كار می كند ، برای او ضروری است.
این تضمین می کند که بدن بین وعده های غذایی گرسنه نشود.
همچنین هورمونهایی که در دوره های استرس حاد مانند آدرنالین آزاد می شوند ، ترشح انسولین را متوقف می کنند و منجر به افزایش قند خون می شوند.
هنگامی که سلولهای لوزالمعده تولید انسولین ناکارآمد می شوند ، یا به طور کلی متوقف می شوند و انسولین کافی تولید نمی کنند ، باعث دیابت می شود.
این اصلی ترین هورمون پانکراس است که تأثیر جدی بر متابولیسم کربوهیدرات در بدن دارد. این مسئولیت عادی سازی سطح گلوکز و میزان جذب آن توسط سلول های مختلف است. بعید نیست که یک فرد عادی ، به دور از پزشکی ، بداند که لوزالمعده چه هورمونی تولید می کند ، اما همه از نقش انسولین اطلاع دارند.

این هورمون توسط سلولهای بتا تولید می شود که در جزایر لانگرهان کاملاً زیاد است. در هیچ کجای بدن بدن تولید نمی شود. و با افزایش سن ، این سلول ها به تدریج می میرند ، بنابراین مقدار انسولین کاهش می یابد. این می تواند واقعیت این باشد که تعداد مبتلایان به دیابت با افزایش سن افزایش می یابد.
انسولین هورمون یک ترکیب پروتئین است - یک پلی پپتید کوتاه. به طور مداوم به همین روش تولید نمی شود.
این امر باعث افزایش تولید قند در خون می شود. در واقع ، بدون انسولین ، گلوکز نمی تواند توسط سلولهای بیشتر ارگانها جذب شود.
و کارکردهای اصلی آن دقیقاً به منظور تسریع در انتقال مولکول های گلوکز به سلول ها است. این یک فرآیند کاملاً پیچیده است ، به منظور اطمینان از عدم وجود گلوکز در خون ، اما برای اطمینان از عملکرد سلولها به جائی که واقعاً لازم است ، جریان می یابد.
نقش هورمون ها
انسولین ، هورمون اصلی لوزالمعده ، به منظور تنظیم تعادل در مصرف مواد غذایی و نیازهای متابولیکی بدن ، در بدن سالم انسان محکم تنظیم می شود.
انسولین سوخت و ساز بدن را تنظیم می کند و باعث جذب کربوهیدرات ها می شود. گلوکز جذب شده توسط بافت ها از طریق لیپوژنز به گلیکوژن ها یا به چربی ها (تری گلیسیرید) تبدیل می شود.
عمل هورمون در سطح متابولیسم انسانی شامل موارد زیر است:
- افزایش مصرف سلولی برخی از مواد ، که قابل توجه ترین در جذب گلوکز توسط عضلات و بافت چربی است (حدود دو سوم کل سلول های بدن) ،
- تکثیر DNA و سنتز پروتئین با کنترل جذب اسید آمینه ،
- تغییرات در فعالیت آنزیم های بیشمار
اقدامات انسولین ، مستقیم و غیرمستقیم:
- تحریک جذب گلوکز - انسولین باعث کاهش غلظت گلوکز در خون به دلیل القای جذب گلوکز توسط سلول ،
- سنتز گلیکوژن را القا می کند - وقتی سطح گلوکز زیاد باشد ، انسولین با فعال کردن آنزیم هگزوکیناز باعث تشکیل گلیکوژن می شود. علاوه بر این ، انسولین آنزیم های فسفوکروسوکیناز و سنتز گلیکوژن ، که وظیفه سنتز گلیکوژن را بر عهده دارند ، فعال می کند ،
- افزایش جذب پتاسیم - تحریک سلول ها برای افزایش محتوای آب داخل سلولی ،
- کاهش در گلوکونوژنز و گلیکوژنولیز ، که باعث کاهش تولید گلوکز از لایه های غیر کربوهیدرات ، به طور عمده در کبد ،
- افزایش سنتز چربی - انسولین باعث می شود سلولهای چربی قند خون را بگیرند ، که به تری گلیسیرید تبدیل می شود ، کاهش انسولین باعث اثر متضاد می شود ،
- افزایش استری شدن اسیدهای چرب - تحریک بافت چربی برای سنتز چربی های خنثی (به عنوان مثال ، تری گلیسیرید) ، کاهش انسولین باعث اثر متضاد ،
- کاهش لیپولیز - روند تقسیم چربی ها به اسیدهای چرب تشکیل دهنده آنها با عمل آنزیم لیپاز ،
- کاهش پروتئولیز - کاهش تجزیه پروتئین ،
- کاهش اتوفاژی - کاهش سطح تخریب ارگانهای آسیب دیده ،
- افزایش جذب اسیدهای آمینه - باعث تحریک سلول ها برای جذب اسیدهای آمینه در گردش ، کاهش انسولین مانع از جذب می شود ،
- تقویت عضله شریانی - عضلات دیواره شریان را وادار به آرامش می کند ، جریان خون را افزایش می دهد ، به ویژه در میکرو شریان ها ، کاهش انسولین باعث می شود که عضلات منقبض شوند ،
- ترشح اسید هیدروکلریک از سلولهای پارتیال در معده ،
- کاهش دفع کلیوی سدیم.

انسولین همچنین بر عملکردهای دیگر بدن مانند رعایت عروق و توانایی شناختی تأثیر می گذارد. با ورود انسولین به مغز انسان ، یادگیری و فواید حافظه کلامی انسان را بهبود می بخشد.
این هورمون همچنین تأثیر تحریکی در ترشح هورمون گنادوتروپین از هیپوتالاموس دارد که باعث تقویت عملکرد تولید مثل می شود.
پلی پپتید پانکراس لوزالمعده و سوماتواستاتین تولید شده توسط پانکراس ظاهراً در تنظیم و تنظیم دقیق انسولین و سلولهای تولید کننده گلوکاگون نقش دارند.
این دومین هورمون مهم پانکراس است. سلولهای آلفا تولید می کند که حدود 22٪ از حجم جزایر لانگرهان را اشغال می کند. از نظر ساختاری ، مشابه انسولین است - همچنین یک پلی پپتید کوتاه است. اما عملکرد دقیقاً برعکس عمل می کند. این ماده کاهش نمی یابد ، اما سطح گلوکز خون را افزایش می دهد و باعث تحریک خروج آن از محل های ذخیره می شود.
لوزالمعده هنگام کاهش مقدار گلوکز در خون ، گلوکاگون را ترشح می کند. از این گذشته ، آن به همراه انسولین ، مانع از تولید آن می شود. علاوه بر این ، در صورت وجود عفونت در خون یا افزایش سطح کورتیزول ، با افزایش فعالیت بدنی یا افزایش در مقدار پروتئین ، سنتز گلوکاگون افزایش می یابد.
پلی پپتید پانکراس
حتی هورمونهای لوزالمعده از اهمیت کمتری نیز برخوردار هستند که تولید آنها بسیار اندک است. یکی از آنها پلی پپتید لوزالمعده است.
اخیراً کشف شده است ، بنابراین عملکردهای آن هنوز کاملاً درک نشده اند. این هورمون فقط توسط لوزالمعده - سلولهای PP آن و همچنین در مجاری تولید می شود.

او هنگام خوردن مقدار زیادی غذای پروتئین یا چربی ، با افزایش فشار جسمی ، گرسنگی و همچنین با هیپوگلیسمی شدید ، آن را ترشح می کند.
هنگامی که این هورمون وارد جریان خون می شود ، تولید آنزیم های لوزالمعده مسدود می شود ، آزاد سازی صفرا ، تریپسین و بیلی روبین کاهش می یابد و همچنین آرامش عضلات کیسه صفرا. به نظر می رسد که پلی پپتید پانکراس آنزیم ها را ذخیره کرده و از از بین رفتن صفرا جلوگیری می کند.
علاوه بر این ، میزان گلیکوژن موجود در کبد را تنظیم می کند. خاطرنشان می شود که با چاقی و برخی آسیب های متابولیکی دیگر ، کمبود این هورمون مشاهده می شود.
و افزایش سطح آن ممکن است نشانه دیابت قندی یا تومورهای وابسته به هورمون باشد.
اختلال عملکرد هورمون
فرآیندهای التهابی و سایر بیماریهای پانکراس می توانند به سلولهایی که در آنها هورمون تولید می شود آسیب برساند. این منجر به بروز آسیب شناسی های مختلف مرتبط با اختلالات متابولیک می شود. بیشتر اوقات ، با عملکرد سلولهای غدد درون ریز ، کمبود انسولین مشاهده می شود و دیابت قندی ایجاد می شود. به همین دلیل ، میزان گلوکز خون بالا می رود و نمی تواند سلول ها را جذب کند.
برای تشخیص آسیب شناسی پانکراس غدد درون ریز از آزمایش خون و ادرار برای گلوکز استفاده می شود. مشاوره با پزشک برای معاینه با کمترین سوء ظن در مورد اختلال عملکرد این عضو بسیار مهم است ، زیرا در مراحل اولیه درمان هرگونه آسیب شناسی آسان تر است.
تعیین ساده میزان گلوکز در خون ، همیشه نشان دهنده ابتلا به دیابت نیست. در صورت مشکوک بودن این بیماری ، آزمایش بیوشیمی ، آزمایش تحمل گلوکز و سایرین انجام می شود.
اما وجود گلوکز در ادرار نشانه دوره شدید دیابت است.
فقدان سایر هورمونهای لوزالمعده کمتر دیده می شود. اغلب این اتفاق در صورت وجود تومورهای وابسته به هورمون یا مرگ تعداد زیادی از سلولهای غدد درون ریز اتفاق می افتد.
لوزالمعده عملکردهای بسیار مهمی در بدن انجام می دهد. این نه تنها هضم طبیعی را فراهم می کند. هورمونهای تولید شده توسط سلولهای آن برای عادی سازی مقدار گلوکز و اطمینان از متابولیسم کربوهیدرات لازم است.
در این مقاله به شما خواهیم گفت که کدام سلولها جزء جزایر لوزالمعده هستند؟ عملکرد آنها چیست و چه هورمونی ترشح می کنند؟
کمی آناتومی
در بافت لوزالمعده نه تنها acini وجود دارد ، بلکه جزایر لانگرهان نیز وجود دارد. سلولهای این سازندها آنزیمی تولید نمی کنند. عملکرد اصلی آنها تولید هورمون است.
این سلولهای غدد درون ریز برای اولین بار در قرن 19 کشف شد. دانشمندی که به احترام او از این موجودات نامگذاری شده بود ، پس از آن هنوز دانشجو بود.
در خود آهن جزایر زیادی وجود ندارد. در بین کل توده اندام ها ، مناطق لانگرهانس 1-2٪ تشکیل شده است. با این حال ، نقش آنها عالی است. سلولهای بخش غدد درون ریز غده 5 نوع هورمون تولید می کنند که هضم ، متابولیسم کربوهیدرات و پاسخ به واکنشهای استرس را تنظیم می کند. با آسیب شناسی این مناطق فعال ، یکی از شایع ترین بیماری های قرن بیست و یکم در حال توسعه است - دیابت. علاوه بر این ، آسیب شناسی این سلول ها باعث سندرم زولینجر-الیسون ، انسولین ، گلوکوژانما و سایر بیماری های نادر می شود.
امروزه مشخص شده است که جزایر لوزالمعده دارای 5 نوع سلول است. در زیر در مورد عملکردهای آنها بیشتر صحبت خواهیم کرد.
جزایر کدام سلول ها هستند؟
جزایر پانکراس تجمع ساختارهای سلولی یکسان نیست ، آنها شامل سلولهایی هستند که از نظر عملکرد و مورفولوژی متفاوت هستند. لوزالمعده غدد درون ریز از سلولهای بتا تشکیل شده است ، که وزن آن در کل حدود 80٪ است ، آنها آملین و انسولین ترشح می کنند.
سلولهای آلفا لوزالمعده باعث ایجاد گلوکاگون می شوند. این ماده به عنوان یک آنتاگونیست انسولین عمل می کند ، به افزایش قند خون در سیستم گردش خون کمک می کند. آنها حدود 20٪ نسبت به کل توده اشغال می کنند.
 گلوکاگون از قابلیت های گسترده ای برخوردار است. این ماده بر تولید گلوکز در کبد تأثیر می گذارد ، تجزیه بافت چربی را تحریک می کند ، غلظت کلسترول را در بدن کاهش می دهد.
گلوکاگون از قابلیت های گسترده ای برخوردار است. این ماده بر تولید گلوکز در کبد تأثیر می گذارد ، تجزیه بافت چربی را تحریک می کند ، غلظت کلسترول را در بدن کاهش می دهد.
همچنین ، این ماده باعث بازسازی سلولهای کبدی ، انسولین در ترك بدن می شود و گردش خون در كلیه ها را تقویت می كند. انسولین و گلوکاگون کارکردهای متفاوتی و متضاد دارند. مواد دیگری مانند آدرنالین ، هورمون رشد ، کورتیزول به تنظیم این وضعیت کمک می کند.
سلول های لانگرهان لوزالمعده از خوشه های زیر تشکیل شده است:
- تجمع "دلتا" ترشح سوماتواستاتین را فراهم می کند ، که می تواند مانع تولید سایر اجزا شود. از کل جرم این ماده هورمونی حدود 3-10٪ است ،
- سلولهای PP قادر به ترشح پپتید پانکراس هستند که ترشح معده را تقویت کرده و فعالیت بیش از حد ارگان دستگاه گوارش را سرکوب می کند ،
- خوشه اپسیلون ماده خاصی را تولید می کند که احساس گرسنگی می کند.
جزایر لانگرهانس یک میکروارگانیسم پیچیده و چند منظوره است که اندازه ، شکل و توزیع مشخصی از اجزای غدد درون ریز دارد.
این معماری سلولی است که بر اتصالات بین سلولی و تنظیم پاراکرین تأثیر می گذارد ، و این به انسولین کمک می کند.
ساختار و عملکرد جزایر پانکراس
لوزالمعده از نظر ساختار یک اندام نسبتاً ساده است ، اما عملکرد آن بسیار گسترده است. اندام داخلی هورمون انسولین تولید می کند ، که قند خون را تنظیم می کند. اگر نارسایی نسبی یا مطلق آن مشاهده شود ، پس آسیب شناسی تشخیص داده می شود - دیابت نوع 1.
از آنجا که لوزالمعده متعلق به دستگاه گوارش است ، در ساخت آنزیم های لوزالمعده که به تجزیه کربوهیدرات ها ، چربی ها و پروتئین ها از مواد غذایی کمک می کند ، نقش موثری را بر عهده می گیرد. با نقض این عملکرد ، پانکراتیت تشخیص داده می شود.
عملکرد اصلی جزایر پانکراس ، حفظ غلظت مورد نیاز کربوهیدرات ها و کنترل سایر اندام های داخلی است. تجمع سلولها به وفور با خون تأمین می شود ، در اثر عصب سمپاتیک و واگ در آنها مجذوب می شود.
ساختار جزایر کاملاً پیچیده است. می توان گفت که هر تجمع سلول ها با عملکردی خاص خود تشکیل کاملی دارند. به لطف این ساختار ، تبادل بین اجزای پارانشیم و غدد دیگر تأمین می شود.
سلولهای جزایر به شکل موزاییک مرتب شده اند ، یعنی بصورت تصادفی. جزیره بالغ با سازماندهی مناسب مشخص می شود. از لوبول ها تشکیل شده است ، آنها توسط بافت همبند احاطه شده اند ، کوچکترین رگ های خونی در داخل عبور می کنند. سلول های بتا در مرکز لوبول ها قرار دارند ؛ بقیه در حاشیه واقع شده اند. اندازه جزایر به اندازه آخرین خوشه ها بستگی دارد.
هنگامی که اجزای جزایر شروع به تعامل با یکدیگر می کنند ، این در سلول های دیگری که در این نزدیکی قرار دارند منعکس می شود. این را می توان با تفاوتهای زیر توصیف کرد:
- انسولین باعث افزایش فعالیت ترشحی سلولهای بتا می شود ، اما در عین حال مانع از کارکرد خوشه های آلفا می شود.
- سلولهای آلفا به نوبه خود "گلوکوناگون" می کنند و بر روی سلول های دلتا عمل می کنند.
- سوماتوستاتین به همان اندازه عملکرد سلولهای بتا و آلفا را مهار می کند.
اگر در ماهیت ذاتی زنجیره نقصی مشاهده شود که همراه با اختلالات ایمنی باشد ، به سلولهای بتا توسط ایمنی خود مورد حمله قرار می گیرند.
آنها شروع به فروپاشی می کنند ، که یک بیماری جدی و خطرناک را تحریک می کند - دیابت.
پیوند سلول
یک بیماری مزمن و غیر قابل درمان است. غدد درون ریز راهی برای درمان فرد برای همیشه پیدا نکرده است. با استفاده از داروها و شیوه زندگی سالم می توانید به یک جبران پایدار بیماری برسید ، اما نه بیشتر.
سلولهای بتا توانایی ترمیم ندارند. با این حال ، در دنیای مدرن ، روش های خاصی وجود دارد که به آنها کمک می کند تا "بازیابی" کنند - جایگزینی. در کنار پیوند لوزالمعده یا ایجاد یک اندام داخلی مصنوعی ، سلول های پانکراس پیوند می خورند.
این تنها فرصتی است که دیابتی ها می توانند ساختار جزایر ویران شده را بازیابی کنند. آزمایش های علمی زیادی انجام شده است که طی آن سلول های بتا از یک اهدا کننده به دیابتی های دیابت نوع 1 پیوند داده می شوند.
نتایج مطالعات نشان داده است که مداخله جراحی به بازگرداندن غلظت کربوهیدرات ها در بدن انسان کمک می کند. به عبارت دیگر ، یک راه حل برای مشکل وجود دارد ، که یک نکته بزرگ است. با این حال ، سرکوب کننده سیستم ایمنی مادام العمر منهای است - استفاده از داروهایی که از رد مواد بیولوژیکی دهنده جلوگیری می کنند.
به عنوان جایگزین برای منبع دهنده ، سلولهای بنیادی مجاز هستند. این گزینه کاملاً مناسب است ، زیرا جزایر لوزالمعده اهدا کنندگان دارای ذخیره خاصی هستند.
داروی ترمیمی با مراحل سریع توسعه می یابد ، اما شما باید یاد بگیرید که چگونه نه تنها پیوند سلول ها انجام شود بلکه باید از تخریب بعدی آنها نیز جلوگیری شود ، که در هر صورت در بدن افراد دیابتی اتفاق می افتد.
در پیوند پزشکی لوزالمعده از خوک یک چشم انداز مشخص وجود دارد. قبل از کشف انسولین ، از عصاره هایی از غده حیوانات استفاده می شد. همانطور که می دانید تفاوت بین انسولین انسان و بز در تنها یک اسید آمینه است.
مطالعه ساختار و عملکرد جزایر لوزالمعده با چشم اندازهای زیادی مشخص می شود ، زیرا بیماری "شیرین" در نتیجه آسیب به ساختار آنها بوجود می آید.
در این مقاله لوزالمعده در فیلم توضیح داده شده است.
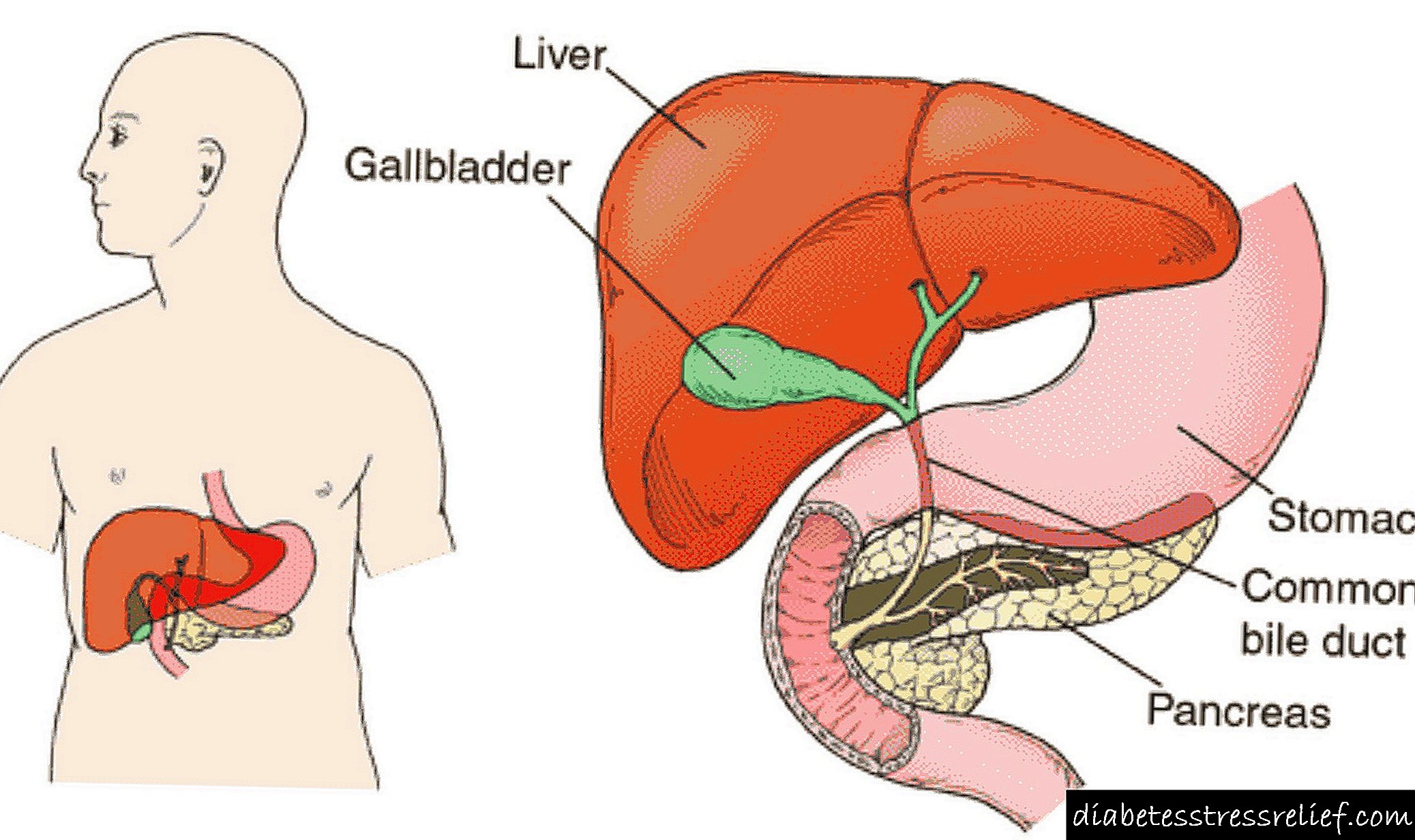
جزایر لوزالمعده ، که جزایر لانگرهان نیز نامیده می شوند ، خوشه های کوچکی از سلول ها هستند که به طور گسترده در لوزالمعده پراکنده شده اند. لوزالمعده ارگاني است با شكل طولي 15-20 سانتيمتر كه در قسمت پشتي معده قرار دارد.
جزایر لوزالمعده شامل چندین نوع سلول از جمله سلولهای بتا است که هورمون انسولین را تولید می کنند. لوزالمعده همچنین آنزیمی را ایجاد می کند که به بدن کمک می کند تا هضم و جذب مواد غذایی شود.
هنگامی که سطح قند خون بعد از خوردن غذا بالا می رود ، پانکراس با آزاد کردن انسولین به جریان خون پاسخ می دهد. انسولین به سلولها در بدن کمک می کند تا گلوکز خون را جذب کنند و از آن برای تولید انرژی استفاده کنند.
دیابت قندی وقتی ایجاد می شود که لوزالمعده انسولین کافی تولید نمی کند ، سلول های بدن از این هورمون با راندمان کافی یا به هر دو دلیل استفاده نمی کنند. در نتیجه گلوکز در خون تجمع می یابد و توسط سلول های بدن از آن جذب نمی شود.
در دیابت نوع 1 ، سلولهای بتا لوزالمعده تولید انسولین را متوقف می کنند ، زیرا سیستم ایمنی بدن به آنها حمله می کند و آنها را از بین می برد. سیستم ایمنی بدن با شناسایی و از بین بردن باکتری ها ، ویروس ها و سایر مواد خطرناک خارجی که در معرض خطر قرار دارد ، افراد را از عفونت ها محافظت می کند. مبتلایان به دیابت نوع 1 باید روزانه انسولین مصرف کنند تا برای زندگی مفید باشد.
دیابت نوع 2 معمولاً با شرایطی به نام مقاومت به انسولین شروع می شود ، که در آن بدن قادر به استفاده مؤثر از انسولین نیست. با گذشت زمان ، تولید این هورمون نیز کاهش می یابد ، بنابراین بسیاری از بیماران مبتلا به دیابت نوع 2 در نهایت مجبور به انسولین می شوند.
پیوند جزایر پانکراس چیست؟
دو نوع پیوند (پیوند) جزایر پانکراس وجود دارد:
تخصیص پیوند جزایر لانگرهان روشی است که طی آن جزایر از لوزالمعده یک اهدا کننده متوفی تمیز ، پردازش و پیوند داده می شود. در حال حاضر ، تخصیص پیوند جزایر پانکراس یک روش آزمایشی محسوب می شود ، زیرا فناوری پیوند آنها هنوز به اندازه کافی موفقیت آمیز نیست.
دانشمندان برای هر نوع انتقال جزایر لوزالمعده ، از آنزیم های تخصصی استفاده می كنند تا آنها را از لوزالمعده یك اهدا كننده متوفی خارج كنند. سپس جزایر در آزمایشگاه تمیز و شمارش می شوند.
به طور معمول ، گیرندگان دو تزریق دریافت می کنند که هرکدام حاوی 400000 تا 500000 جزیره است. پس از کاشت ، سلولهای بتا این جزایر شروع به تولید و ترشح انسولین می کنند.
انتقال اختصاصی جزایر لانگرهانس برای بیمارانی که مبتلا به دیابت نوع 1 هستند و سطح قند خون کنترل نشده ای دارند ، انجام می شود. هدف از پیوند این است که به این بیماران کمک کند که سطح نسبتاً نرمال قند خون را با یا بدون تزریق انسولین روزانه به دست آورند.
خطر ابتلا به هیپوگلیسمی ناخودآگاه را کاهش یا از بین ببرید (وضعیت خطرناکی که در آن بیمار علائم هیپوگلیسمی را احساس نمی کند). هنگامی که فرد رویکرد هیپوگلیسمی را احساس می کند ، می تواند اقداماتی را برای بالا بردن سطح گلوکز خون به مقادیر طبیعی برای او انجام دهد.
تخصیص پیوند جزایر پانکراس فقط در بیمارستانهایی انجام می شود که مجوز آزمایش های بالینی این روش درمانی را دریافت کرده اند. پیوند اغلب توسط رادیولوژیست ها انجام می شود - پزشکان متخصص در تصویربرداری پزشکی. رادیولوژیست از اشعه ایکس و سونوگرافی برای هدایت درج یک سوند قابل انعطاف از طریق برش کوچک در دیواره فوقانی شکم به ورید پورتال کبد استفاده می کند.
ورید پورتال رگ خونی بزرگی است که خون را به کبد منتقل می کند. این جزایر به آرامی از طریق کاتتر وارد شده در ورید پورتال به داخل کبد وارد می شوند. به عنوان یک قاعده ، این روش تحت بی حسی موضعی یا عمومی انجام می شود.
بیماران اغلب به دو یا چند پیوند نیاز دارند تا بتوانند به اندازه کافی عملکرد جزایر را کاهش دهند یا نیاز انسولین را کاهش دهند.
انتقال خودکار جزایر لوزالمعده پس از لوزالمعده کامل - برداشتن جراحی از کل لوزالمعده - در بیماران مبتلا به پانکراتیت مزمن یا طولانی مدت شدید انجام می شود ، که قابل استفاده با سایر روش های درمانی نیست. این روش آزمایشی محسوب نمی شود. انتقال خودکار پیوند جزایر Langenhans در بیماران مبتلا به دیابت نوع 1 انجام نمی شود.
این عمل در بیمارستان تحت بیهوشی عمومی انجام می شود. ابتدا جراح لوزالمعده را جدا می کند ، که از آن جزایر پانکراس خارج می شود. طی یک ساعت ، جزایر خالص شده از طریق سوند به داخل کبد بیمار وارد می شود. هدف از انجام چنین پیوندی تهیه جزایر لانگرهانس به اندازه کافی بدن برای تولید انسولین است.
بعد از پیوند جزایر پانکراس چه اتفاقی می افتد؟
جزایر لانگرهان اندکی پس از پیوند ، انسولین را آزاد می کنند. با این حال ، عملکرد کامل و رشد رگ های خونی جدید زمان می برد.
دریافت کنندگان باید قبل از شروع کار کامل جزایر پیوند شده ، تزریق انسولین را ادامه دهند. آنها همچنین می توانند آماده سازی ویژه قبل و بعد از پیوند را انجام دهند که به پیوند موفقیت آمیز و عملکرد طولانی مدت جزایر لانگرهان کمک می کند.
با این حال ، یک پاسخ خود ایمنی که سلولهای بتا خود بیمار را از بین می برد ، می تواند دوباره به جزایر پیوند شده حمله کند. اگرچه کبد مکانی سنتی برای تزریق جزایر اهداکننده است ، دانشمندان در حال تحقیق در مورد مکان های جایگزین از جمله بافت ماهیچه ها و اندام های دیگر هستند.
جزایر لانگرهانس: عملکرد غدد درون ریز و آنتی بادی های سلولهای لوزالمعده
 همانطور که می دانید ، وظیفه اصلی جزایر پانکراس لانگرهانس تحقق عملکرد غدد درون ریز لوزالمعده است. اول از همه ، این ترشح هورمونهای اصلی به نام انسولین و گلوکاگون است که هدف آن کنترل سطح قند خون است. بنابراین ، انسولین اگر شاخص ها از حد نرمال فراتر رود ، مقدار آن را کاهش می دهد و برعکس ، گلوکاگون افزایش می یابد.
همانطور که می دانید ، وظیفه اصلی جزایر پانکراس لانگرهانس تحقق عملکرد غدد درون ریز لوزالمعده است. اول از همه ، این ترشح هورمونهای اصلی به نام انسولین و گلوکاگون است که هدف آن کنترل سطح قند خون است. بنابراین ، انسولین اگر شاخص ها از حد نرمال فراتر رود ، مقدار آن را کاهش می دهد و برعکس ، گلوکاگون افزایش می یابد.
شایان ذکر است در صورتی که سلولهای غدد درون ریز جزایر لوزالمعده به طور کامل با کار مقابله نکنند ، و بر این اساس ، هورمونهای مورد نیاز بدن به مقدار مناسب ترشح نمی شوند ، بنابراین دیابت به احتمال زیاد بروز می کند. این بیماری به دلیل وجود قند زیاد در بدن رخ می دهد و برای درمان آن ، تجویز مداوم انسولین لازم است. نوع 1 این بیماری به ویژه خطرناک است ، زیرا در این حالت سلولهای غدد درون ریز لوزالمعده به طور انبوه از بین می روند و بر این اساس ، وضعیت بیمار بتدریج ، بلکه به سرعت ، بدتر نمی شود و نیاز به درمان فوری و مداوم دارد. دلایل زیادی برای این امر وجود دارد ، به عنوان مثال ، تولید آنتی بادی توسط بدن در برابر بیماری های ایمنی.
نکته مهم ، روشی برای درمان و ترمیم عملکردهای غدد درون ریز لوزالمعده با پیوند سلولهای جزایر لانگرهانس است. اما در این حالت ، لازم است ابتدا آنالیز آنتی بادی بر روی سلولهای غدد درون ریز لوزالمعده انجام شود ، زیرا تکنیک پیوند فقط برای نوع خاصی از دیابت مؤثر خواهد بود. اما با وجود سرطان یا سایر بیماری های لوزالمعده نتیجه مطلوبی نمی دهد.
پیوند سلول جزایر لانگرهانس با دیابت نوع 1
امروزه جزایر لانگرهان به لطف پیوند آنها فرصتی برای درمان دیابت نوع 1 فراهم می کند. این روش نه چندی پیش توسط متخصصان کانادایی کشف شد ، و گرچه به هزینه های مالی بسیار چشمگیری نیاز دارد و خود این روش بسیار پیچیده و پرخطر است ، اما کاملاً واقعی است و فرصتی برای ترمیم تدریجی عملکرد غدد درون ریز لوزالمعده ، و بر این اساس ، یک نجات احتمالی برای بیماران از یک بیماری خطرناک
ماهیت پیوند این است که سلولهای غدد درون ریز سالم که از یک اهدا کننده دریافت می شوند با استفاده از سوند به بدن فرد مبتلا به دیابت نوع 1 وارد می شوند ، در نتیجه با توجه به تأثیر آنها ، میزان انسولین لازم برای حفظ گلوکز در خون شروع می شود. در حد طبیعی درک این نکته ضروری است که جزایر لانگرهانس برای پیوند توسط بیمار مبتلا به دیابت ، فقط از جسد خارج می شود که کاملاً تمام پارامترهای مورد نیاز را برآورده می کند ، و این باعث کاهش خطر رد می شود ، به خصوص که آنتی بادی های موجود در بدن با هدف از بین بردن اجسام خارجی انجام می شود. آنچه مهم است پیوند سلولهای غدد درون ریز جزایر لوزالمعده بسیار سریع اثر می بخشد ، اما به دلیل اینكه بعد از چند هفته وضعیت بیمار مبتلا به دیابت نوع 1 به سرعت در حال بهبود است.
 درک این نکته ضروری است که پیوند جزایر لانگرهانس این خطر را دارد که آنتی بادی در بدن بیمار مبتلا به دیابت منجر به رد شدن غده لوزالمعده شود. به همین دلیل است که در موفقیت روش ، مهمترین نقش توسط دارو درمانی انجام می شود ، با هدف مسدود کردن موقت عمل برخی از واکنش های ایمنی و آنتی بادی های خاص ، که می تواند به تخریب بافت منجر شود.علاوه بر این ، داروهایی برای معالجه بیمار به گونه ای انتخاب می شود که به طور کامل انجام نشود ، بلکه فقط برخی از واکنش های ایمنی را بطور جزئی مسدود می کنید ، به ویژه آنهایی که تولید کننده آنتی بادی در سلول های جزایر لانگرهانس هستند و این امر باعث می شود تا خطر عملکرد پانکراس غدد درون ریز به حداقل برسد.
درک این نکته ضروری است که پیوند جزایر لانگرهانس این خطر را دارد که آنتی بادی در بدن بیمار مبتلا به دیابت منجر به رد شدن غده لوزالمعده شود. به همین دلیل است که در موفقیت روش ، مهمترین نقش توسط دارو درمانی انجام می شود ، با هدف مسدود کردن موقت عمل برخی از واکنش های ایمنی و آنتی بادی های خاص ، که می تواند به تخریب بافت منجر شود.علاوه بر این ، داروهایی برای معالجه بیمار به گونه ای انتخاب می شود که به طور کامل انجام نشود ، بلکه فقط برخی از واکنش های ایمنی را بطور جزئی مسدود می کنید ، به ویژه آنهایی که تولید کننده آنتی بادی در سلول های جزایر لانگرهانس هستند و این امر باعث می شود تا خطر عملکرد پانکراس غدد درون ریز به حداقل برسد.
در عمل ، این روش نتایج کاملاً خوبی را برای بیماران نشان داد ، به خصوص که هیچ تلفاتی به دلیل پیوند سلول های غده لوزالمعده و رد بعدی آنها تحت تأثیر آنتی بادی ها وجود ندارد. همچنین تعداد معینی از بیماران بیمار به هیچ وجه به تجویز انسولین احتیاج ندارند ، در حالی که برخی هنوز به آن نیاز داشتند ، اما بیشتر شاخص ها در مورد عملکرد غدد درون ریز لوزالمعده به میزان قابل توجهی بهبود یافته است ، که باعث می شود در آینده امید به پیش آگهی بسیار مطلوب داشته باشیم.
با این وجود شایان ذکر است که در این مورد معایب خاصی وجود دارد که باید مورد توجه قرار گیرد. بنابراین ، تحت تأثیر آنتی بادی های جزایر لانگرهانس ، خطر ابتلا به انواع عوارض جانبی در بیماران وجود دارد ، یعنی اختلالات در تولید آب لوزالمعده ، اسهال ، کم آبی و همچنین عوارض جدی تر. علاوه بر این ، حتی پس از انجام عمل ، در طول زندگی لازم است به طور مداوم از آن دسته داروهای لازم استفاده شود تا رد سلولهای پیوندی در بدن شروع نشود. و با توجه به این واقعیت که این داروها با هدف مسدود کردن واکنش های ایمنی ، به ویژه آنتی بادی های خاص ، مصرف آنها باعث افزایش خطر انواع عفونت ها می شود.
بنابراین ، جزایر پانکراس عملکرد غدد درون ریز را برای کل بدن مهم انجام می دهد ، تولید هورمون های لازم برای سوخت و ساز بدن و کنترل سطح قند خون را فراهم می کند. به همین دلیل است که برای بیماران مبتلا به دیابت نوع 1 ، در بعضی موارد پیوند سلول های غدد درون ریز ممکن است مرتبط باشد که به تدریج کار بدن را عادی می کند و بر این اساس ، انسولین بسیار مورد نیاز در مقدار مناسب تولید می شود.
مزایا و مضرات تخصیص پیوند جزایر پانکراس چیست؟
از مزایای تخصیص پیوند جزایر لانگرهان می توان به بهبود کنترل قند خون ، کاهش یا از بین بردن تزریق انسولین برای دیابت و پیشگیری از هیپوگلیسمی اشاره کرد. یک جایگزین برای پیوند جزایر پانکراس پیوند کل لوزالمعده است ، که اغلب با پیوند کلیه انجام می شود.
مزایای پیوند کل لوزالمعده وابستگی کمتری به انسولین و عملکرد طولانی تر اعضای بدن دارد. ضرر اصلی پیوند لوزالمعده این است که یک عمل بسیار پیچیده با خطر زیاد عوارض و حتی مرگ است.
آلتراسپانس جزایر پانکراس همچنین می تواند به جلوگیری از هیپوگلیسمی ناخودآگاه کمک کند. مطالعات علمی نشان داده اند که حتی جزایر با عملکرد جزئی پس از پیوند می توانند از این وضعیت خطرناک جلوگیری کنند.
بهبود كنترل قند خون از طريق تخصيص انتقال جزاير نيز مي تواند باعث كاهش يا جلوگيري از پيشرفت مشكلات مرتبط با ديابت مانند بيماري هاي قلبي و كليه ، آسيب هاي عصبي و چشم شود. تحقیقات برای بررسی این احتمال ادامه دارد.
مضرات تخصیص پیوند جزایر لوزالمعده شامل خطرات مرتبط با خود عمل - بخصوص خونریزی یا ترومبوز است. جزایر پیوند شده ممکن است تا حدی یا کاملاً متوقف شوند. سایر خطرات با عوارض جانبی داروهای سرکوب کننده سیستم ایمنی که بیماران برای جلوگیری از رد سیستم ایمنی بدن جزایر پیوند شده مجبور به مصرف آن هستند ، همراه است.
اگر بیمار در حال حاضر کلیه پیوند یافته و در حال حاضر داروهای سرکوب کننده سیستم ایمنی بدن استفاده کند ، تنها خطرات آنفلوآنزای جزایر و عوارض جانبی داروهای سرکوب کننده سیستم ایمنی است که در حین انتقال خون اجرا می شود. این داروها برای انجام عمل پیوند مورد نیاز نیستند ، زیرا سلولهای معرفی شده از بدن خود بیمار گرفته می شوند.
اثر پیوند جزایر لانگرهانس چیست؟
از سال 1999 تا 2009 در آمریكا ، تخصیص پیوند جزایر لوزالمعده روی 571 بیمار انجام شد. در برخی موارد ، این روش در رابطه با پیوند کلیه انجام شد. اکثر بیماران یک یا دو تزریق جزیره دریافت کردند. در پایان دهه ، میانگین تعداد جزایر به دست آمده در طی یک تزریق واحد 463000 بود.
طبق آمار ، طی یک سال پس از پیوند ، حدود 60٪ از گیرندگان استقلال از انسولین دریافت کرده اند ، این به معنای توقف تزریق انسولین برای حداقل 14 روز است.
در پایان سال دوم پس از پیوند ، 50٪ از گیرندگان می توانند حداقل 14 روز تزریق را متوقف کنند. با این حال ، استقلال طولانی مدت انسولین t دشوار است و در نهایت بیشتر بیماران مجبور به مصرف مجدد انسولین شدند.
عوامل مرتبط با بهترین نتایج آلوگرافت مشخص شد:
- سن - 35 سال و بالاتر.
- قبل از پیوند تری گلیسیرید خون را کاهش دهید.
- دوزهای پایین انسولین قبل از پیوند.
با این حال ، شواهد علمی نشان می دهد که حتی جزایر پیوند شده لانگرهان حتی تا حدی عملکردی می تواند کنترل قند خون و دوزهای پایین انسولین را بهبود بخشد.
نقش سرکوب کننده های سیستم ایمنی چیست؟
داروهای سرکوب کننده سیستم ایمنی برای جلوگیری از رد ، یک مشکل شایع در هر پیوند ضروری است.
دانشمندان در سالهای اخیر در زمینه پیوند جزایر لانگرهان موفقیت های زیادی کسب کرده اند. در سال 2000 دانشمندان کانادایی پروتکل پیوند خود را منتشر کردند (پروتکل ادمونتون) که توسط مراکز پزشکی و پژوهشی در سراسر جهان تطبیق یافته و همچنان در حال پیشرفت است.
پروتکل ادمونتون استفاده از ترکیب جدیدی از داروهای سرکوب کننده سیستم ایمنی ، از جمله daclizumab ، sirolimus و تاکرولیموس را معرفی می کند. دانشمندان به توسعه و مطالعه اصلاحات در مورد این پروتكل ، از جمله بهبود رژیم های درمانی كه به افزایش موفقیت پیوند كمك می كند ، ادامه می دهند. این طرح ها در مراکز مختلف ممکن است متفاوت باشد.
نمونه هایی از دیگر سرکوب کننده های سیستم ایمنی مورد استفاده در پیوند جزایر لنگرهانس عبارتند از گلبولین آنتی بادی ، گلوبولین ، اتیانپس ، آلمتوزوماب ، بازالیکسیماب ، اورئولیموس و مایکوفنولت مفتیل. دانشمندان همچنین در حال کشف داروهایی هستند که به گروه داروهای سرکوب کننده سیستم ایمنی مانند اگزناتید و sitagliptin تعلق ندارند.
داروهای سرکوب کننده سیستم ایمنی اثرات جانبی جدی دارند و هنوز اثرات طولانی مدت آنها کاملاً درک نشده است. عوارض جانبی فوری شامل زخمهای دهانی و مشکلات گوارشی (مانند ناراحتی معده و اسهال) است. بیماران همچنین ممکن است ایجاد شوند:
- افزایش کلسترول خون.
- فشار خون بالا.
- کم خونی (کاهش تعداد گلبول های قرمز و هموگلوبین در خون).
- خستگی
- تعداد گلبولهای سفید خون کاهش یافته است.
- اختلال در عملکرد کلیه.
- افزایش حساسیت به عفونت های باکتریایی و ویروسی.
مصرف داروهای سرکوب کننده سیستم ایمنی نیز خطر ابتلا به انواع خاصی از تومورها و سرطان را افزایش می دهد.
دانشمندان همچنان به دنبال راه هایی برای دستیابی به تحمل سیستم ایمنی بدن در جزایر پیوند یافته هستند ، که در آن سیستم ایمنی بدن آنها را بیگانه نمی شناسد.
تحمل ایمنی عملکرد جزایر پیوند شده را بدون مصرف داروهای سرکوب کننده سیستم ایمنی تقویت می کند. برای مثال ، یک روش پیوند جزایر محصور شده در یک پوشش ویژه است که می تواند به جلوگیری از واکنش رد کمک کند.
موانع پیش روی تخصیص پیوند جزایر پانکراس چیست؟
فقدان اهداكنندگان مناسب ، مهمترين مانع در استفاده گسترده از پيوند كاشت جزاير لانگرهانس است. علاوه بر این ، همه لوزالمعده های اهدا کننده برای استخراج جزایر مناسب نیستند ، زیرا تمام معیارهای انتخاب را برآورده نمی کنند.
همچنین باید در نظر داشت که در هنگام تهیه جزایر برای پیوند ، آنها اغلب آسیب می بینند. بنابراین ، هر سال پیوند بسیار کمی انجام می شود.
دانشمندان برای حل این مشکل روشهای مختلفی را مطالعه می کنند. به عنوان مثال ، تنها بخشی از لوزالمعده از یک اهدا کننده زنده استفاده می شود ؛ جزایر پانکراس خوک ها استفاده می شوند.
دانشمندان جزایر خوک ها را به حیوانات دیگر ، از جمله میمون ها پیوند می دهند ، آنها را در یک پوشش مخصوص یا با استفاده از دارو برای جلوگیری از رد کردن ، محاصره می کنند. روش دیگر ایجاد جزایر از سلولهای دیگر - به عنوان مثال ، از سلولهای بنیادی است.
علاوه بر این ، موانع مالی مانع از انتقال گسترده جزایر می شود. به عنوان مثال ، در ایالات متحده ، فناوری پیوند تجربی محسوب می شود ، بنابراین از بودجه تحقیقاتی تأمین می شود ، زیرا بیمه چنین روش هایی را پوشش نمی دهد.
تغذیه و رژیم غذایی
فردی که تحت پیوند جزایر لوزالمعده قرار دارد باید رژیم غذایی را که توسط پزشکان و متخصصان تغذیه تهیه شده است ، دنبال کند. داروهای سرکوب کننده سیستم ایمنی که بعد از پیوند مصرف می شوند می توانند باعث افزایش وزن شوند. یک رژیم غذایی سالم برای کنترل وزن بدن ، فشار خون ، کلسترول خون و سطح قند خون بسیار مهم است.
ما سعی می کنیم مناسب ترین و مفیدترین اطلاعات را برای شما و سلامتی خود در اختیار شما قرار دهیم. مطالب موجود در این صفحه برای اهداف اطلاعاتی است و برای اهداف آموزشی در نظر گرفته شده است. بازدید کنندگان وب سایت نباید از آنها به عنوان توصیه پزشکی استفاده کنند. تعیین تشخیص و انتخاب روشهای درمانی همچنان حق انحصاری پزشک شما است! ما مسئول هیچ عواقب منفی ناشی از استفاده از اطلاعات ارسال شده در وب سایت نیستیم